
| A. | 人体缺碘,可通过食用加碘盐补碘 | |
| B. | 缺铁性贫血,可通过食用铁强化酱油预防 | |
| C. | 锌摄入量过多,也会引起缺铁性贫血 | |
| D. | 为了防止龋齿,人人都适合使用含氟牙膏 |
分析 A.人体缺碘,可通过食用加碘盐补碘;
B.铁强化酱油可以为人体补铁;
C.锌与缺铁性贫血无关;
D.儿童不能使用含氟牙膏.
解答 解:A.碘是甲状腺素的重要成分,人体缺碘,可通过食用加碘盐补碘,故A正确;
B.铁强化酱油可以为人体补铁,所以缺铁性贫血,可通过食用铁强化酱油预防,故B正确;
C.锌影响身体发育,缺乏会引起食欲不振,生长迟缓,发育不良,与缺铁性贫血无关,故C错误;
D.含氟的牙膏有利于预防龋齿,但是儿童不能使用含氟牙膏,故D错误.
故选CD.
点评 本题考查微量元素对人体健康的重要作用,难度不大,化学来源于生产生活,也服务于生产生活,因此在近年的考试中,与生产生活实际相关的情景题已渐渐成为新宠.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 g]
g]查看答案和解析>>
科目:高中化学 来源: 题型:解答题
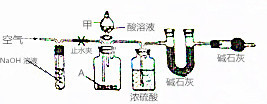 碱式碳酸盐A可用作胃药,其组成可表示为Al2Mg6(OH)x(CO3)y•zH2O.某校化学兴趣小组欲测定其化学式,实验设计如下:
碱式碳酸盐A可用作胃药,其组成可表示为Al2Mg6(OH)x(CO3)y•zH2O.某校化学兴趣小组欲测定其化学式,实验设计如下:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含有较多钙、镁离子的水叫做硬水 | |
| B. | 软水中不含有钙、镁离子 | |
| C. | 可以采取加热煮沸法和离子交接法软化硬水 | |
| D. | 硬水会降低肥皂的洗涤效果 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③⑦ | B. | ②⑥⑦ | C. | ①④⑧ | D. | ④⑥⑧ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com