
| A | B | C | D |
| 将二氧化硫通入到一定量氯水中 | 将氯化铝溶液滴入到一定量NaOH溶液中 | NaOH溶液加入AlCl3、Mg(NO3)2、HNO3溶液 | 将铁粉加入到一 定量氯化铁溶液中 |
 |  |  |  |
| A. | A | B. | B | C. | C | D. | D |
分析 A、二氧化硫与氯气反应生成硫酸和盐酸,酸性增强,pH减小;
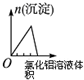
B、将氯化铝溶液滴入到一定量NaOH溶液中开始无沉淀,将氢氧根转化为偏铝根离子,然后滴入氯化铝产生沉淀;
C、NaOH溶液加入AlCl3、Mg(NO3)2、HNO3溶液,氢氧化钠首先与硝酸反应,然后与镁离子和铝离子反应生成氢氧化铝和氢氧化镁沉淀,随后氢氧化铝溶解,最后只有氢氧化镁沉淀;
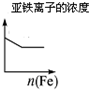
D、铁与铁离子发生氧化还原反应生成亚铁离子.
解答 解:A、SO2+Cl2+2H2O=2HCl+H2SO4,生成物酸性增强,pH减小,故A正确;
B、将氯化铝溶液滴入到一定量NaOH溶液中开始无沉淀,将氢氧根转化为偏铝根离子,然后滴入氯化铝产生沉淀,后然后沉淀逐渐增加,直到偏铝酸根离子完全沉淀,沉淀量达到最大值,最后不变,图象不符合,故B错误;
C、NaOH溶液加入AlCl3、Mg(NO3)2、HNO3溶液,氢氧化钠首先与硝酸反应,然后与镁离子和铝离子反应生成氢氧化铝和氢氧化镁沉淀,随后氢氧化铝溶解,最后只有氢氧化镁沉淀,所以无中间平衡于横坐标的一条线段,故C错误;
D、铁与铁离子发生氧化还原反应生成亚铁离子,所以亚铁离子的浓度增大,而不是减小,故D错误;
故选A.
点评 本题考查了元素化合物的性质,题目难度不大,题目涉及铝的化合物、氯水、二氧化硫、铁离子等物质,侧重于基础知识的考查.


 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,每生成2.24L O2,转移的电子数一定为0.4NA | |
| B. | 常温下,7.8g苯中所含C-H数位0.6NA | |
| C. | 常温常压下,1.8g甲基(-CD3)中含有的中子数为NA | |
| D. | 25℃时,1.0L PH=13的Ba(OH)2溶液中含有的OH-数目为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 化学式 | CO(g) | H2(g) | CH3OH(l) | CH4(g) |
| △H/(kJ/mol) | -283.0 | -285.8 | -726.5 | -890.3 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com