
| A、冰箱中使用的含氟制冷剂泄露后,会增加空气中的PM2.5 |
| B、浓硫酸具有强腐蚀性,可用浓硫酸刻蚀石英制艺术品 |
| C、施肥时,农家肥草木灰(有效成分K2CO3)不能与氮肥NH4Cl混合使用 |
| D、氯气和活性炭均可作为漂白剂,若同时使用,漂白效果会明显加强 |


 小学教材完全解读系列答案
小学教材完全解读系列答案科目:高中化学 来源: 题型:
| 操作 | 实验现象 | 结论 | |
| A | 某气体通入溴水中 | 溴水褪色 | 该气体一定是C2H4 |
| B | 向浓度均为0.1mol?L-1NaCl和NaI混合溶液中,滴加几滴AgNO3溶液 | 出现黄色沉淀 | Ksp(AgCl)<Ksp(AgI) |
| C | 苯酚钠溶液中通入CO2气体 | 溶液变浑浊 | 碳酸酸性比苯酚强 |
| D | 分别向H2O和乙醇中加入少量Na | Na与水反应更加剧烈 | 水比乙醇易电离H+ |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
 研究CO2的利用对促进低碳社会的构建具有重要的意义.
研究CO2的利用对促进低碳社会的构建具有重要的意义.| n(H2) |
| n(CO2) |
2- 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
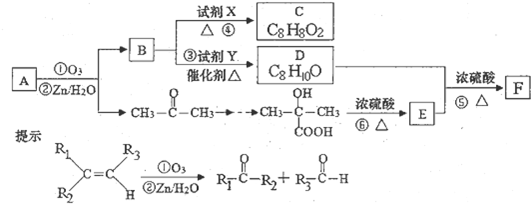
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
 常温下,取一定量的PbI2固体配成饱和溶液,T时刻改变某一条件,离子的浓度变化如图所示,(注:第一次平衡时c(I-)=2×10-3mol/L,c(Pb2+)=2×10-3mol/L)下列有关说法正确的是( )
常温下,取一定量的PbI2固体配成饱和溶液,T时刻改变某一条件,离子的浓度变化如图所示,(注:第一次平衡时c(I-)=2×10-3mol/L,c(Pb2+)=2×10-3mol/L)下列有关说法正确的是( )| A、常温下,Ksp=2×10-6 |
| B、温度不变,向PbI2饱和溶液中加入少量硝酸铅浓溶液,PbI2的溶解度不变,c(Pb2+)不变 |
| C、T时刻改变的条件是升高温度,PbI2的,Ksp 增大 |
| D、常温下Ksp[PbS]=8×10-28,向PbI2的悬浊液中加入Na2S溶液,PbI2(s)+S2-(aq)?PbS(s)+2I-(aq)反应的化学平衡常数为5×1018 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 将盛有12mLNO2和O2混合气体的量筒倒立于水槽中,充分反应后,还剩余2mL无色气体,则原混合气体中O2的体积可能是( )
将盛有12mLNO2和O2混合气体的量筒倒立于水槽中,充分反应后,还剩余2mL无色气体,则原混合气体中O2的体积可能是( )| A、2.1mL | B、2.4mL |
| C、3.6mL | D、4mL |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
A、
| ||
B、
| ||
C、
| ||
D、
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com