
科目:高中化学 来源: 题型:实验题
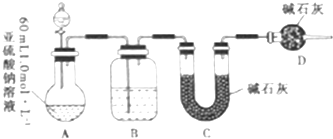
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
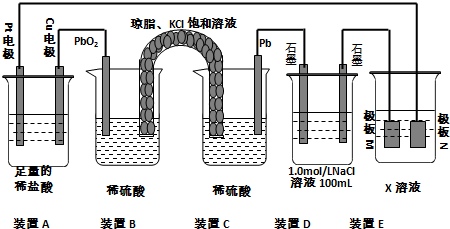
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
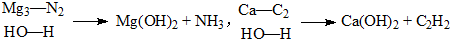
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Br2+2NaI=2NaBr+I2 | |
| B. | 2P+8H2O+5Br2=2H3PO4+10HBr↑ | |
| C. | 3Br2+3Na2CO3=5NaBr+NaBrO3+3CO2↑ | |
| D. | SO2+2H2O+Br2=H2SO4+2HBr |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验室制取氯气 | B. | 实验室制取氧气 | ||
| C. | 实验室制取二氧化碳 | D. | 实验室制取氨气 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
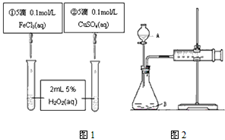 为比较Fe3+和Cu2+对H2O2分解反应的催化效果,甲乙两组同学分别设计了如图1、图2所示的实验.请回答下列问题
为比较Fe3+和Cu2+对H2O2分解反应的催化效果,甲乙两组同学分别设计了如图1、图2所示的实验.请回答下列问题查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com