

分析 淡黄色粉末为Na2O2,生成气体为氧气,则单质A为Na或氧气,固体为碳酸钠,由氧气和单质B反应生成黑色固体,加入稀硫酸溶解得到蓝色溶液可知B为Cu,反应Ⅲ为碳酸钠与氢氧化钙的反应,生成沉淀为碳酸钙,溶液为氢氧化钠溶液,则与硫酸铜反应生成氢氧化铜沉淀,以此解答该题.
解答 解:淡黄色粉末为Na2O2,生成气体为氧气,固体为碳酸钠,由氧气和X反应的产物以及与硫酸反应后的溶液的颜色可知X为Cu,反应Ⅱ为碳酸钠与氢氧化钙的反应,生成沉淀为碳酸钙,溶液为氢氧化钠溶液,则与硫酸铜反应生成氢氧化铜沉淀,
(1)由以上分析可知,黑色固体为CuO,淡黄色粉末为Na2O2,名称为过氧化钠,故答案为:CuO;过氧化钠;
(2)反应(Ⅰ)是钠和氧气加热反应生成过氧化钠,反应的化学方程式为:2Na+O2$\frac{\underline{\;\;△\;\;}}{\;}$Na2O2,
故答案为:2Na+O2$\frac{\underline{\;\;△\;\;}}{\;}$Na2O2;
(3)反应(Ⅱ)为过氧化钠与二氧化碳的反应,生成碳酸钠和氧气,反应的化学方程式为2Na2O2+2CO2=2Na2CO3+O2,
故答案为:2Na2O2+2CO2=2Na2CO3+O2;
(4)反应Ⅲ为碳酸钠与氢氧化钙的反应,生成碳酸钙和氢氧化钠,反应的化学方程式为Na2CO3+Ca(OH)2=CaCO3↓+2NaOH,
故答案为:Na2CO3+Ca(OH)2=CaCO3↓+2NaOH.
(5)把单质A投到蓝色溶液反应钠和水反应生成氢氧化钠和氢气,2Na+2H2O=2NaOH+H2↑,氢氧化钠和硫酸铜反应生成氢氧化铜和硫酸钠,CuSO4+2NaOH=Cu(OH)2↓+Na2SO4,总反应的化学方程式为:2Na+2H2O+CuSO4=Cu(OH)2↓+Na2SO4+H2↑,
故答案为:2Na+2H2O+CuSO4=Cu(OH)2↓+Na2SO4+H2↑;
点评 本题考查无机物的推断,侧重于学生的分析能力和元素化合物知识的综合应用,难度中等,注意把握物质的颜色,为解答该题的关键.


科目:高中化学 来源: 题型:选择题
| A. | CuO | B. | Cu20 | C. | Cu | D. | Cu(OH)2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 将稀硫酸改用浓硫酸 | B. | 向稀硫酸中加入少量硫酸铜溶液 | ||
| C. | 向稀硫酸中加入硫酸钠固体 | D. | 给装置中发生反应的部分加热 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一个D2O分子所含的中子数为8 | B. | CO2的电子式::O::C::O: | ||
| C. | 水的结构简式:H-O-H | D. | HCl的电子式: |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
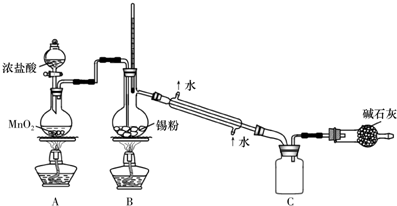
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
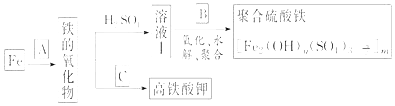
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4 L CCl4含有4NA个Cl原子 | |
| B. | 16gO2和O3组成的混合气体中含有的原子数为NA | |
| C. | 1 mol Na2O2与足量H2O完全反应,转移电子数为2 NA | |
| D. | 78g Na2O2所含的阴离子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
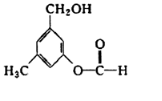 有机物A的结构简式如图所示,某同学对其可能具有的化学性质进行了如下预测,其中正确的是( )
有机物A的结构简式如图所示,某同学对其可能具有的化学性质进行了如下预测,其中正确的是( )| A. | ①②③ | B. | ①③⑤ | C. | ①②④ | D. | ③④⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com