
����Ŀ������п��һ����Ҫ�Ĺ�ҵԭ�ϣ��㷺����ũҵ����������Ƶ���ҵ����ҵ����п������Ҫ�ɷ�ΪZnO��FeO��CuO��PbO�ȣ��ȹ�ҵ��������ZnSO4��7H2O���������£�
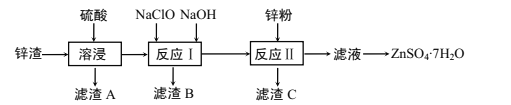
(1)���ܽ��������У�ѡ����п��������ѡ������п��۵�ԭ����______���ò����в���ͨ�����ˮ������Ŀ����________��
(2)������A������Ҫ�ɷ���________��
(3)����Ӧ�����У�����NaClO��Ӧ�����ӷ���ʽΪ___��
(4)����Ӧ�����У��ټ���NaOH����pHԼΪ4.5����������B������Ҫ�ɷ���_____���ѧʽ������Ksp[Zn(OH)2]=3��10-17��Ksp[Cu(OH)2]=2.2��10-20��Ksp[Fe(OH)3]=2.8��10-39��
(5)����Ӧ�����У������п����������ϡ���ᴦ����ԭ����_________��
(6)ȡ28.7gZnSO4��7H2O��������ͬ�¶ȣ�ʣ�������������±���
�¶�/�� | 100 | 250 | 680 | 930 |
����/g | 17.90 | 16.10 | 13.43 | 8.10 |
��680��ʱ���ù���Ļ�ѧʽΪ_________(����ĸ���)��
A.ZnO B.Zn3O(SO4)2 C.ZnSO4 D.ZnSO4��H2O
���𰸡����������ɱ����ۺ�������Դ ��ʹ��ӦҺ���¶����ߣ���ʹ��Ӧ���ֻ�ϣ��Լӿ췴Ӧ���� PbSO4 2Fe2++ClO-+2H+=2Fe3++Cl-+H2O Fe(OH)3 ��ȥп�۱��������Ĥ B
��������
п������Ҫ�ɷ�ΪZnO��FeO��CuO��PbO�ȣ������м���ϡ���������ZnOת��ΪZnSO4��FeOת��ΪFeSO4��CuOת��ΪCuSO4������Һ����PbO�������ᷴӦ���������Ե�PbSO4������ͨ�����ˣ��õ�������A�к���PbSO4����Һ�к���ZnSO4��FeSO4��CuSO4�������Һ�м���NaClO�����Խ���Һ��Fe2+����ΪFe3+������NaOH��Һ����pH��ʹFe3+ת��ΪFe(OH)3������������B�У���Һ�м���Zn�ۣ�Cu2+��Zn�����û���Ӧ����Cu���ʣ�������Zn��������Cu��������C�У���Һ�к���ZnSO4������Һ����Ũ������ȴ�ᾧ�����γ���ZnSO4��7H2O���壬�ݴ˷������
(1)п���к���ZnO�������ܽ��������У�ѡ����п��������ѡ������п��۵�ԭ���ǽ��������ɱ����ۺ�������Դ���ò����в���ͨ�����ˮ������Ŀ���ǿ�ʹ��ӦҺ���¶����ߣ���ʹ��Ӧ���ֻ�ϣ��Լӿ췴Ӧ���ʣ�
(2)��������������֪������A������Ҫ�ɷ���PbSO4��
(3) ����Ӧ�����У��������ǿ�����Ե�NaClO�����Խ���Һ�е�Fe2+����ΪFe3+����Ӧ�����ӷ���ʽΪ2Fe2++ClO-+2H+=2Fe3++Cl-+H2O��
(4) ����Ӧ�����У��ټ���NaOH����pHԼΪ4.5��Fe3+��OH-ת��ΪFe(OH)3��������������B������Ҫ�ɷ���Fe(OH)3��
(5)����Ӧ�����У������п����������ϡ���ᴦ������������Zn���ױ������е�O2��������ZnO��Ĥ��ʹ��������Գ�ȥп�۱��������Ĥ��
(6)n(ZnSO4��7H2O)=28.70g��287g/mol=0.1mol������ZnԪ���غ��֪����ZnO��ZnSO4��ZnSO4��H2O��Ϊ0.1mol������Zn3O(SO4)2ʱ���ʵ���Ϊ![]() ��0.1mol��
��0.1mol��
����ZnSO4H2O������Ϊ17.90g(�ֽ��¶�Ϊ100��)������ZnSO4������Ϊ16.10g(�ֽ��¶�Ϊ250��)������ZnO������Ϊ8.10g(�ֽ��¶�Ϊ930��)���ݴ�ͨ���ų���ȷ��680��ʱ���ù���Ļ�ѧʽΪZn3O(SO4)2���ʺ���ѡ����B��


 һ����ʦ�����Ծ�ϵ�д�
һ����ʦ�����Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�л�����ṹ��ʽΪ![]() �����ڸ��л�������������ȷ����
�����ڸ��л�������������ȷ����
A. ����ʹ����KMnO4��Һ��ɫ
B. ����ʹ��ˮ��ɫ
C. �ڼ��Ⱥʹ��������£�����ܺ�4 mol H2��Ӧ
D. ������ˮ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�¶��£�![]() ��
��![]() �ĵ��볣���ֱ�Ϊ
�ĵ��볣���ֱ�Ϊ![]() ��
��![]() ����
����![]() ���������ͬ����������Һ�ֱ�ϡ�ͣ���
���������ͬ����������Һ�ֱ�ϡ�ͣ���![]() ���ˮ����ı仯��ͼ��ʾ������������ȷ���ǣ� ��
���ˮ����ı仯��ͼ��ʾ������������ȷ���ǣ� ��

A. ����������![]() ��Һ
��Һ
B. ��Һ��ˮ�ĵ���̶ȣ�b�㣾c��
C. ��c�㵽d�㣬��Һ��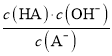 ���ֲ��䣨����
���ֲ��䣨����![]() ��
��![]() �ֱ������Ӧ�����������ӣ�
�ֱ������Ӧ�����������ӣ�
D. ��ͬ���a�������Һ�ֱ���![]() ǡ���кͺ���Һ��
ǡ���кͺ���Һ��![]() ��ͬ
��ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���״���һ����Ҫ���Լ��������Ͷ�����̼��һ�������¿ɺϳɼ״���CO2(g)+3H2 (g) ![]() CH3 OH(g)+H2O(g)�����ܱ������г���3mol������1mol������̼����û�������м״�������������¶ȵĹ�ϵ��ͼA��ʾ��
CH3 OH(g)+H2O(g)�����ܱ������г���3mol������1mol������̼����û�������м״�������������¶ȵĹ�ϵ��ͼA��ʾ��
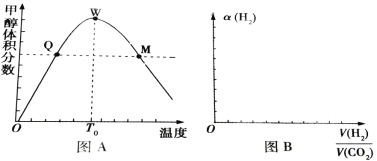
�Իش��������⣺
��1���÷�Ӧ��______(��������������������)��Ӧ���÷�Ӧƽ�ⳣ���ı���ʽ�ǣ�______��Ϊ�˽��ͺϳɼ״��ijɱ��ɲ��õĴ�ʩ��______(����дһ�������Ľ���)
��2������0~T0�ڣ��״�����������仯���ƣ�______��
��3��������Q���ת����______(��������������С������������������ͬ)������W���ת����______������������ͬ���״���Q�������Ӧ����______�״���M�������Ӧ���ʡ�
��4��ͼB��ʾ����ת������(H2)��Ͷ�ϱ�![]() �Ĺ�ϵ������ͼB�л��������仯���߲�������߶�Ӧ���������������߶�Ӧ�������ֱ�Ϊ��һ�����߶�Ӧ��ѹǿ��1.01��105Pa����һ�����߶�Ӧ��ѹǿ��3.03��105Pa(����������ͬ)
�Ĺ�ϵ������ͼB�л��������仯���߲�������߶�Ӧ���������������߶�Ӧ�������ֱ�Ϊ��һ�����߶�Ӧ��ѹǿ��1.01��105Pa����һ�����߶�Ӧ��ѹǿ��3.03��105Pa(����������ͬ)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ʯ��ʯī��Ϊ̼��ͬ�������壬��������������ʱȼ������һ����̼�����ȼ�����ɶ�����̼����Ӧ�зų���������ͼ��ʾ������˵����ȷ����( )
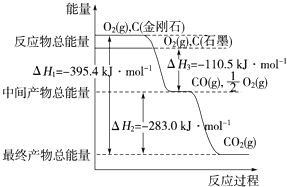
A.�������Ľ��ʯ��ʯī��ȫȼ�գ�ʯī�ų�����������
B.��ͨ��״���£����ʯ��ʯī��ȣ����ʯ���ȶ�
C.��ʾʯīȼ���ȵ��Ȼ�ѧ����ʽΪC(ʯī��s)��O2(g)===CO2(g) ��H����393.5 kJ��mol��1
D.36 gʯīת���ɽ��ʯ���ų�������Ϊ5.7 kJ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӷ���ʽ����ȷ����
A.��ϡ��������⣺Fe2O3+6H+=2Fe3++3H2O
B.Cl2ͨ��ˮ�У�Cl2+H2OH++Cl-+HClO
C.ͭ��Ũ���ᷴӦ���ɺ���ɫ���壺3Cu+8H++2NO3-=3Cu2++2NO2��+4H2O
D.ʵ������MnO2��Ũ������Cl2��MnO2+4H++2Cl-![]() Mn2++Cl2��+2H2O
Mn2++Cl2��+2H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���к͵ζ������Ҫ��С��0.1%������20.00 mL0.2000mol��L��1����ζ�20mL0.2000mol��L��1NaOH��Һ�����к͵ζ������з���ͻ��ʱ��pH��Χ��(lg2��0.3)�� ��
A. 4.3��9.7B. 3.7��10.3C. 4.0��10.0D. ��ȷ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������(V)���仯�������Ź㷺����;����ش��������⣺
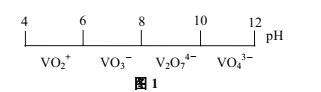
(1)������Һ�е���Ҫ�ۺ�״̬����Һ��pH��ϵ��ͼ1��ʾ��V2O74-��VԪ�صĻ��ϼ���________����Һ��VO3-ת��ΪV2O74-�����ӷ���ʽΪ________��
(2)ƫ�����������ͨ�ķ����Σ���V2O5����̼������Һ�У����������ɣ���Ȼ������Ȼ�泥��������ƫ�����(NH4VO3)���ù����ܷ�Ӧ�Ļ�ѧ����ʽΪ________����pH����8.0ʱƫ����炙ᷢ��ת������ԭ������Һ�е�VO3-ת��ΪV2O74-��________(����д��һ��ԭ��)��
(3)NH4VO3�ڸ����·ֽ������V2O5����Ϊ���Ṥҵ��2SO2(g)+O2(g)![]() 2SO3(g)��H=pkJ/mol��Ӧ�Ĵ��������ԭ����ͼ2��ʾ��
2SO3(g)��H=pkJ/mol��Ӧ�Ĵ��������ԭ����ͼ2��ʾ��
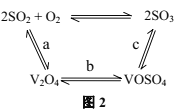
�ٹ���a����b���Ȼ�ѧ����ʽΪ
V2O5(s)+SO2(g)=V2O4(s)+SO3(g) ��H=qkJ/mol
V2O4(s)+O2(g)+2SO2(g)=2VOSO4(s) ��H=rkJ/mol
�����c���Ȼ�ѧ����ʽΪ_________��
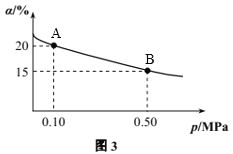
��T��ʱ��Ӧ2SO3(g)![]() 2SO2(g)+O2(g) ��H>0��SO3��ת����(��)����ϵ��ѹǿ(p)�Ĺ�ϵ��ͼ3��ʾ��T��ʱ����2molSO3����10L�ܱ������У���Ӧ�ﵽƽ�����ϵ��ѹǿΪ0.10MPa����T��ʱB��Ļ�ѧƽ�ⳣ��Kc=_________��
2SO2(g)+O2(g) ��H>0��SO3��ת����(��)����ϵ��ѹǿ(p)�Ĺ�ϵ��ͼ3��ʾ��T��ʱ����2molSO3����10L�ܱ������У���Ӧ�ﵽƽ�����ϵ��ѹǿΪ0.10MPa����T��ʱB��Ļ�ѧƽ�ⳣ��Kc=_________��
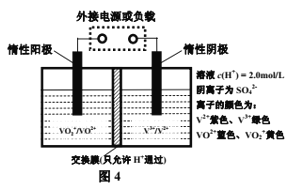
(4)ȫ��Һ�����ܵ�������ò�ͬ��̬���ӶԵ�������ԭ��Ӧ��ʵ�ֻ�ѧ�ܺ͵����ת����װ�ã���ԭ����ͼ4��ʾ��
�ٳ������У��Ҳ���Һ��ɫ����________ɫ��Ϊ________ɫ��
�ڳ��ʱ��ת�Ƶĵ�����ΪNA�����������Һ��n(H+)�ı仯��Ϊ______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������úΪԭ���Ʊ���һЩ������Ʒǰ���ֱ����á���ͼ������AΪԭ������������ë�ĺϳ�·�ߡ�����˵����ȷ����
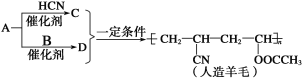
A.A����C�ķ�Ӧ���ڼӳɷ�ӦB.�ϳ�������ë�ķ�Ӧ�������۷�Ӧ
C.A����D�ķ�Ӧ����ȡ����ӦD.��A�Ľṹ��ʽΪCH2=CH2
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com