
���� �Ҵ�ȼ�շų�������ͬʱ���ɶ�����̼��ˮ���ݴ���д�Ȼ�ѧ����ʽ��n��C2H5OH��=$\frac{46g}{46g/mol}$=1mol������C��Hԭ���غ����������ʵ������ٸ���m=nM�������������
��� �⣺�Ҵ�ȼ�շų�������ͬʱ���ɶ�����̼��Һ̬ˮ���ݴ���д�Ȼ�ѧ����ʽΪC2H5OH��l��+3O2��g���T2CO2��g��+3H2O��l����H��0��
n��C2H5OH��=$\frac{46g}{46g/mol}$=1mol������C��Hԭ���غ��n��CO2��=2n��C2H5OH��=2��1mol=2mol��n��H2O��=3n��C2H5OH��=3��1mol=3mol����m��CO2��=2mol��44g/mol=88g��n��H2O��=3mol��18g/mol=54g��
���Ҵ�ȼ���Ȼ�ѧ����ʽΪΪC2H5OH��l��+3O2��g���T2CO2��g��+3H2O��l����H��0��������̼����Ϊ88g��ˮ��������54g��
���� ���⿼�黯ѧ����ʽ�йؼ��㣬Ϊ��Ƶ���㣬���Ը��ݷ���ʽ���м��㣬Ҳ���Ը���ԭ���غ���м��㣬ע��ԭ���غ��������ã���Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���������ܷų�H2����Һ�У�Na+��Cl-��SO42-��Mg2+ | |
| B�� | 0.1mol/L FeCl3��Һ�У�H+��K+��SCN-��I- | |
| C�� | �ӷ�̪������Һ�У�Na+��Ba2+��Cl-��Br- | |
| D�� | ʹ��ɫʯ����Һ������Һ�У�Ca2+��Na+��HCO3-��Cl- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
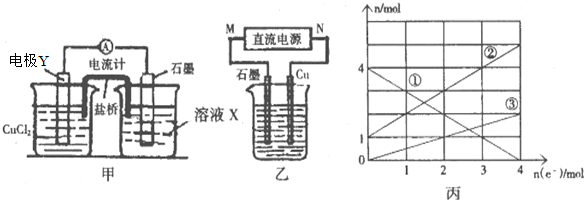
 �ס��ҡ�����X����ѧ��ѧ�г�����4�����ʣ���ת����ϵ������ͼ��ʾ��ϵ�����м�X�����ǣ�������
�ס��ҡ�����X����ѧ��ѧ�г�����4�����ʣ���ת����ϵ������ͼ��ʾ��ϵ�����м�X�����ǣ�������| A�� | ��ΪC��XΪO2 | B�� | ��ΪFe��XΪCl2 | C�� | ��ΪN2��XΪO2 | D�� | ��ΪNaOH��XΪSO2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 3.0mol•L-1 | B�� | 3.5mol•L-1 | C�� | 4.0mol•L-1 | D�� | 8.0mol•L-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 50��ʱ����ˮ��C��H+����C��OH-�� | B�� | Kw���¶����߶����� | ||
| C�� | ˮ�ĵ�������Ƿ��ȹ��� | D�� | ˮ��ǿ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
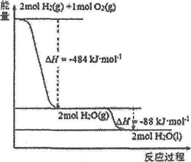 ��֪��H-H��O=O�ļ��ֱܷ���436kJ•mol-1��496kJ•mol-1������ͼ����H-O�ļ����ǣ�������
��֪��H-H��O=O�ļ��ֱܷ���436kJ•mol-1��496kJ•mol-1������ͼ����H-O�ļ����ǣ�������| A�� | 926 kJ•mol-1 | B�� | 485 kJ•mol-1 | C�� | 463 kJ•mol-1 | D�� | 221 kJ•moI-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ƺͼصĺϽ�����ڿ����ӷ�Ӧ�����Ƚ����� | |
| B�� | þ��ͭ�����Ƚ����γɵĺϽ�����������������ɻ������� | |
| C�� | ����ӡˢ��·��ʱ������FeCl3��Һ��ʴCu | |
| D�� | �����ж�����������ҩ��ĺϳ� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com