
【题目】减少氮的氧化物和碳的氧化物在大气中的排放是环境保护的重要内容之一。合理应用和处理碳、氮及其化合物,在生产生活中有重要意义。
(1)对温室气体二氧化碳的研究一直是科技界关注的重点。在催化剂存在下用H2还原CO2 是解决溫室效应的重要手段之一,相关反应如下:
已知H2 和CH4的燃烧热分别为285.5kJ/mol 和890.0kJ/mol。
H2O(1) =H2O(g) △H= +44 kJ/mol
试写出H2 还原CO2 生成CH4和H2O(g)的热化学方程式_____________。
(2)CO2在Cu-ZnO催化下,可同时发生如下的反应I、II,其可作为解决温室效应及能源短缺的重要手段。
I.CO2(g) +3H2(g)![]() CH3OH(g) +H2O(g) △H1=-57.8 kJ/mol
CH3OH(g) +H2O(g) △H1=-57.8 kJ/mol
II.CO2(g) +H2(g)![]() CO(g) + H2O(g) △H2 = +41.2 kJ/mol
CO(g) + H2O(g) △H2 = +41.2 kJ/mol
①某温度时,若反应I的速度v1大于反应II的速度以v2,则下列反应过程的能量变化正确的是_______(填选项)。
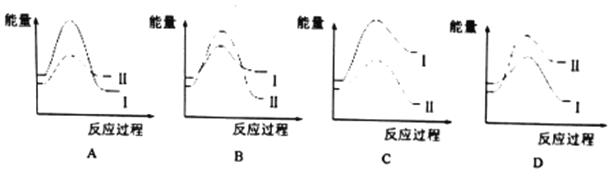
②对于气体参加的反应,,表示平衡常数Kp时,用气体组分(B)的平衡分压p(B)代替该气体物质的量浓度c(B)。
已知:气体各组分的分压p(B),等于总压乘以其体积分数。
在Cu-ZnO存在的条件下,保持温度T时,在容积不变的密闭容器中,充入一定量的CO2 及H2,起始及达平衡时,容器内各气体物质的量如下表:
CO2 | H2 | CH3OH | CO | H2O(g) | 总压/kPa | |
起始/mol | 5.0 | 7.0 | 0 | 0 | 0 | p0 |
平衡/mol | n1 | n2 | p |
若反应I、II均达平衡时,P0=1.2p,则表中n1=____;若此时
(3)汽车尾气是雾霾形成的原因之一。研究氮氧化物的处理方法可有效减少雾霾的形成,可采用氧化还原法脱硝:
4NO(g) +4NH3(g) +O2(g) ![]() 4N2(g) +6H2O(g) △H <0
4N2(g) +6H2O(g) △H <0
根据下图判断提高脱硝效率的最佳条件是________;氨氮比一定时,在400℃时,脱硝效率最大,其可能的原因是______________。
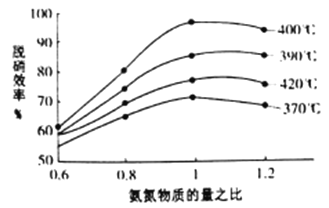
(4)用活性炭还原法也可以处理氮氧化物,某研究小组向某密闭容器加入一定量的活性炭和NO,发生反应:C(s) +2NO(g)![]() N2(g) +CO2(g) △H>0
N2(g) +CO2(g) △H>0
在T℃时,反应进行到不同时间测得各物质的量浓度如下:
时间/min 浓度/(mol/L) | 0 | 10 | 20 | 30 | 40 | 50 |
NO | 1.0 | 0.58 | 0.40 | 0.40 | 0.48 | 0.48 |
N2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
CO2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
30min后,只改变某一条件,根据上表的数据判断改变的条件可能是_______。
A.通入一定量的CO2 B.加入合适的催化剂 C.适当缩小容器的体积
D.通入一定量的NO E.加入一定量的活性炭 F.适当升高温度
【答案】 CO2(g)+4H2(g)=CH4(g)+2H2O(g) △H=-164.0kJ·mol-1 D 1.0 ![]() 温度 400℃,氨氮物质的量之比为 1 在 400℃时催化剂的活性最好, 催化效率高, 同时 400℃温度较高,反应速率快 CD
温度 400℃,氨氮物质的量之比为 1 在 400℃时催化剂的活性最好, 催化效率高, 同时 400℃温度较高,反应速率快 CD
【解析】(1)考查热化学反应方程式的计算,①H2(g)+1/2O2(g)=H2O(l) △H=-285.5kJ·mol-1,②CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H=-890.0kJ·mol-1,③H2O(l)=H2O(g) △H=+44kJ·mol-1,氢气还原CO2的反应是4H2+CO2=CH4+2H2O(g),因此有①×4-②+③×2得出:CO2(g)+4H2(g)=CH4(g)+2H2O(g) △H=-164.0kJ·mol-1;(2)考查化学平衡计算,①反应I是放热反应,反应物的总能量大于生成物的总能量,反应II是吸热反应,反应物的总能量小于生成物的总能量,因为反应I的速度快于反应II,因此反应I的活化能低于反应II,故D正确;②设体系中生成CH3OH的物质的量xmol,反应II反应前后气体系数之和相等,因此容器中气体总物质的量为(12-2x)mol,根据压强之比等于物质的量之比,因此有12/(12-2x)=p0/p,解得x=1mol,即n1=1mol,CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
变化:1 3 1 1
平衡: 1 1
CO2(g)+H2(g)![]() CO(g)+H2O(g)
CO(g)+H2O(g)
变化: 2 2 2 2
平衡: 2 2,根据n1的分析,体系中气体总物质的量为10mol,p(H2O)=3p/10,p(CH3OH)=p/10,消耗CO2的物质的量为3mol,则平衡是CO2的物质的量为2mol,即p(CO2)=2p/10,同理p(H2)=2p/10,反应I的平衡常数Kp= =
=![]() ;(3)本题考查反应条件的控制,根据图像,在氨氮物质的量之比为1,温度在400℃时,脱硝效率最大,原因是在400℃时催化剂的活性最好,催化效率最高,同时400℃温度较高,反应速率快;(4)考查影响化学平衡移动的因素,A、40min的数值都增大,通入一定量的CO2,CO2浓度增大,NO和N2浓度应不变,故A错误;B、催化剂对浓度无影响,故B错误;C、适当缩小容器的体积,组分浓度增大,故C正确;D、C为固体,通入一定量的NO,相当于在原来的基础上增大压强,体积缩小,浓度增大,故D正确;E、C为固体,加入一定量的活性炭,对平衡无影响,对组分浓度无影响,故E错误;F、此反应是吸热反应,升高温度,平衡向正反应方向移动,NO浓度降低,故F错误。
;(3)本题考查反应条件的控制,根据图像,在氨氮物质的量之比为1,温度在400℃时,脱硝效率最大,原因是在400℃时催化剂的活性最好,催化效率最高,同时400℃温度较高,反应速率快;(4)考查影响化学平衡移动的因素,A、40min的数值都增大,通入一定量的CO2,CO2浓度增大,NO和N2浓度应不变,故A错误;B、催化剂对浓度无影响,故B错误;C、适当缩小容器的体积,组分浓度增大,故C正确;D、C为固体,通入一定量的NO,相当于在原来的基础上增大压强,体积缩小,浓度增大,故D正确;E、C为固体,加入一定量的活性炭,对平衡无影响,对组分浓度无影响,故E错误;F、此反应是吸热反应,升高温度,平衡向正反应方向移动,NO浓度降低,故F错误。


科目:高中化学 来源: 题型:
【题目】对工业废气物进行脱硫(SO2)处理并加以利用,不仅可防止大气污染,还能实现一定经济效益。回答下列问题:
(1)热化学碘硫循环脱硫,涉及以下三个反应:
bunsen反应:SO2(g)+I2(g)+2H2O(l)═2HI (g)+H2SO4(l) △H
硫酸分解反应:2H2SO4(l)=2SO2(g)+O2(g)+2H2O(l) △H=+462kJ·mol-1
碘化氢分解反应:2HI(g)=H2(g)+I2(g)△H=+10kJ·mol-1
已知氢气的燃烧热为286kJ·mol-1,则bunsen反应的△H=_________kJ·mol-1。
(2)在活性炭催化下,SO2与Cl2发生反应:SO2(g)+Cl2(g)![]() SO2Cl2(g)△H<0。在定温定压条件下,容器体积为10L的容器中加入等物质的量的SO2和Cl2,充分混合(二者物质的量均为nmol)后,达到平衡后容器体积为8L。
SO2Cl2(g)△H<0。在定温定压条件下,容器体积为10L的容器中加入等物质的量的SO2和Cl2,充分混合(二者物质的量均为nmol)后,达到平衡后容器体积为8L。
①SO2Cl2能与水发生非氧化还原反应,生成两种酸,则这两种酸的化学式为_________。
②下列事实中,不能作为判断硫元素和氯元素非金属性强弱的依据是_________(填字母)。
A.硫化氢的分解温度为300℃左右,氯化氢1500℃才分解
B.氢硫酸(H2S的水溶液)是一种弱酸,盐酸是强酸
C.将氯气通入氢硫酸中,溶液中产生黄色浑浊
D.高氯酸在无机含氧酸中酸性最强
③该温度下,SO2的平衡转化率α1=_________,反应的平衡常数K=_________(列式并计算)。
④下列措施中不能进一步提高氯气的平衡转化率的是_________。
A.平衡后将容器的体积压缩为4L B.增大二氧化硫的浓度
C.升高温度 D.将SO2Cl2(g)液化分离
⑤若向该容器中初始投入SO2和Cl2的物质的量均为0.5nmol,则达到平衡时SO2的平衡转化率:α2_________填“>”“<”或“=”)α1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无色透明的酸性溶液中能大量共存的是( )
A.Na+、K+、Cu2+、SO42-B.NH4+、Na+、NO3-、Cl-
C.K+、Ca2+、HCO3-、Cl-D.Mg2+、Fe3+、Cl-、OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数的值,下列说法正确的是
A. 标准状况下,2.24L乙烷与2.24L苯含C-H键数均为0.6NA
B. 16.8gFe与足量的水蒸气加热充分反应,转移电子数为0.8NA
C. 25C时,1LpH=7的CH3COONH4溶液中含NH4+数一定为1.0×10-7NA
D. 0.2molCO2与0.1molC在密闭容器中充分反应生成CO分子数为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸苯甲酯可提高花或果的芳香气味,故常用于化妆品工业和食品工业。乙酸苯甲酯可以用下面的设计方案合成:
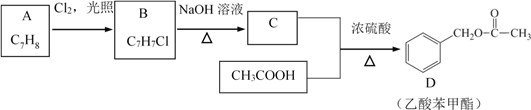
请回答:
(1)乙酸苯甲酯中官能团的名称是________。
(2)A到B的反应类型是________。
(3)由C生成D的反应方程式为________。
(4)满足下列条件的D的同分异构体为________。(写出一种即可)
① 与FeCl3溶液反应显紫色
② 1mol D可以与4mol H2发生加成反应
③ D的核磁共振氢谱有四组峰,峰面积比为6:2:1:1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com