
【题目】短周期元素W,X,Y,Z在元素周期表中的位置如图所示.下列说法中,正确的是( ) 
A.W的最高价氧化物对应的水化物是强酸
B.Y的原子半径在同周期主族元素中最大
C.W的非金属性比Z的弱
D.Z的气态氢化物的稳定性在同主族元素中最强
【答案】A
【解析】解:由元素所在周期表中的位置可知X为He,Y为F,W为Cl,Z为S,则
A.W为Cl,非金属性较强,对应的最高价氧化物对应的水化物为HClO4 , 为酸性最强的含氧酸,故A正确;
B.同周期元素从左到右原子半径逐渐减小,则Y的原子半径在同周期主族元素中最小,故B错误;
C.同周期元素从左到右,元素的非金属性逐渐增强,则W的非金属性比Z的强,故C错误;
D.同主族元素从上到下,元素的非金属性逐渐增强,对应的元素的非金属性越强,对应的氢化物越稳定,W为S,同主族元素中O对应的氢化物的稳定性最强,故D错误.
故选A.
由元素所在周期表中的位置可知X为He,Y为F,W为Cl,Z为S,结合元素周期律的递变规律判断元素对应单质、化合物的性质.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列关于物质水解的说法正确的是 ( )
A.纤维素属于营养物质,可被人体水解
B.油脂、糖类和蛋白质都能发生水解反应
C.淀粉水解液加碘水,可检测是否发生水解
D.淀粉和纤维素水解的最终产物均为葡萄糖
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化钠(Na3N)是科学家制备的一种重要的化合物,它与水作用可产生NH3 . 请回答下列问题:
(1)Na3N的电子式是 , 该化合物由键形成.
(2)Na3N与盐酸反应生成种盐,其电子式分别是 , .
(3)Na3N与水的反应属于(填基本反应类型)反应.
(4)比较Na3N中两种粒子的半径:r(Na+)(填“>”“=”“<”) r(N3﹣).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)某同学用托盘天平称量烧杯的质量,天平平衡后的状态如图1所示。由图中可以看出,该同学在操作时的一个错误是___________________,烧杯的实际质量为__________ g。
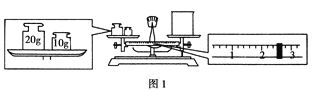
(2)需配制150 mL 0.2 mol·L-1 NaCl溶液,该同学转移溶液的示意图如图2所示。指出实验中存在的两个错误:_________________________________。
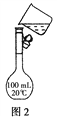
(3)用质量分数为98%密度为1.84 g·cm-3的浓硫酸配制1 000 mL 0.1 mol·L-1的稀硫酸。
①应用量筒量取浓硫酸________ mL;
②配制硫酸时需用到的仪器有量筒、小烧杯、玻璃棒、_______________________;
③下列操作使所配制溶液的物质的量浓度偏高的是________(填序号)。
A.称量时用了生锈的砝码 B.将NaOH放在纸张上称量
C.定容时俯视刻度线 D.往容量瓶中转移时,有少量液体溅出
E.未洗涤溶解NaOH的烧杯 F.定容时仰视刻度线
G.容量瓶未干燥即用来配制溶液H.定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】《太平惠民和剂局方》中对精制蜡过程有如下记载:.....先将蜡六两熔化作汁,以重绵滤去滓,以好酒一升,于银石器内煮蜡熔,数沸倾出,候酒冷,其蜡自浮,取蜡称用。”文中涉及的操作方法是( )
A. 蒸馏 B. 升华 C. 干馏 D. 蒸发
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定的温度下,将一定量的氢气和氮气的混合气体充入等压密闭容器中进行反应,达到平衡时维持温度不变,测得混合气体的密度是反应前密度的1.25倍,则达到平衡时,氨气的体积分数为
A. 25% B. 27.5 % C. 30% D. 37.5%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com