
 .
. .
.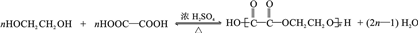 .
. 为原料制
为原料制 的合成路线流程图(无机试剂任用),在方框中填出相应的物质,并在括号注明反应条件.合成路线流程图示例如下:
的合成路线流程图(无机试剂任用),在方框中填出相应的物质,并在括号注明反应条件.合成路线流程图示例如下: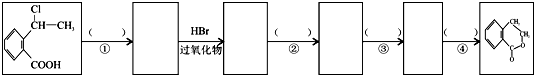
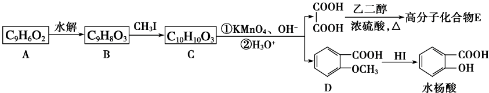
分析 C被高锰酸钾氧化生成乙二酸和D,结合题给信息及C的分子式知,C的结构简式为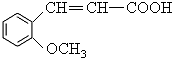 ,B和CH3I发生取代反应生成C,则B的结构简式为:
,B和CH3I发生取代反应生成C,则B的结构简式为: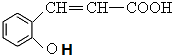 ,A水解生成B,且A的分子式为C9H6O2,A和B相对分子质量相差18,所以A的结构简式为:
,A水解生成B,且A的分子式为C9H6O2,A和B相对分子质量相差18,所以A的结构简式为: ,D在HI条件下发生取代反应生成水杨酸.(5)中
,D在HI条件下发生取代反应生成水杨酸.(5)中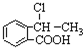 在氢氧化钠的醇溶液、加热条件下发生消去反应生成
在氢氧化钠的醇溶液、加热条件下发生消去反应生成 ,
, 与HBr发生加成反应生成
与HBr发生加成反应生成 ,
, 在氢氧化钠的水溶液、加热条件下发生取代反应生成
在氢氧化钠的水溶液、加热条件下发生取代反应生成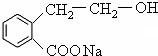 ,
,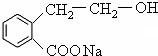 在浓硫酸加热条件下发生酯化反应生成
在浓硫酸加热条件下发生酯化反应生成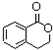 .
.
解答 解:(1)由上述分析可知,A的结构简式为 ,故答案为:
,故答案为: ;
;
(2)B的结构简式为: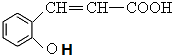 ,含氧官能团有羧基、酚羟基;B和CH3I发生取代反应生成C,故答案为:羧基、酚羟基;取代反应;
,含氧官能团有羧基、酚羟基;B和CH3I发生取代反应生成C,故答案为:羧基、酚羟基;取代反应;
(3)由于C→D转化过程发生氧化反应,可以氧化酚羟基,故反应步骤B→C的目的是:B生成C的目的是保护酚羟基,使之不被氧化,
故答案为:保护酚羟基,使之不被氧化;
(4)据ABC的结构简式可知,
a、C中有8种不同环境的氢原子,故a正确;
b、据ABC的结构简式可知,都有碳碳双键,能够发生加聚反应,故b正确;
c、A的结构简式为: ,1molA能够与4mol氢气加成,故c错误;
,1molA能够与4mol氢气加成,故c错误;
d、B中有酚羟基,能够与溴发生取代反应,故d正确;
故答案为:c;
(5)能够水解,说明含有酯基,水解生成的产物之一能发生银镜反应,说明是甲酸酯,其苯的对二取代物有: ,
,
故答案为: ;
;
(6)乙二酸和乙二醇通过酯化反应合成高分子化合物的化学方程式为: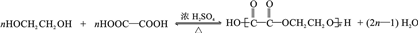 ,
,
故答案为: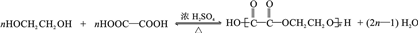 ;
;
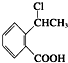
(7)以 为原料制
为原料制 时,首先在NaOH的乙醇溶液中消去,再与HBr加成,再水解生成醇,酯化生成酯,合成路线流程图为:
时,首先在NaOH的乙醇溶液中消去,再与HBr加成,再水解生成醇,酯化生成酯,合成路线流程图为: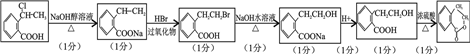 ,
,
故答案为: .
.
点评 本题考查有机物推断和合成,难点是推断D的同分异构体,注意水解生成的产物之一能发生银镜反应,说明是甲酸酯,难度较大


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案科目:高中化学 来源: 题型:解答题
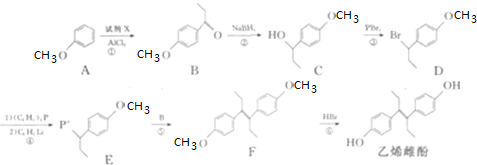
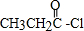 ;
;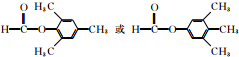 (任写一种).
(任写一种).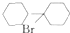 可由
可由 经五步反应合成:
经五步反应合成: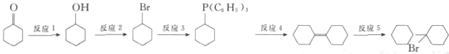
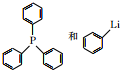 (写结构简式);
(写结构简式);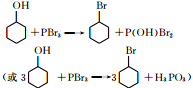 ;
;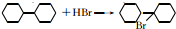 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含HS-溶液中:K+、Cu2+ NO3-、SO42- | |
| B. | 某无色透明的溶液:Mg2+、ClO-、SiO32- Na+ | |
| C. | 加入(NH4)2CO3后加热,有气体产生的溶液:Na+ K+、NO3- HCO3- | |
| D. | pH=0:Na+ Ca2+ Fe3+ NO3- Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
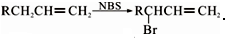 .醇酸树脂是一种成膜性良好的树脂,下面是一种醇酸树脂的合成线路:
.醇酸树脂是一种成膜性良好的树脂,下面是一种醇酸树脂的合成线路: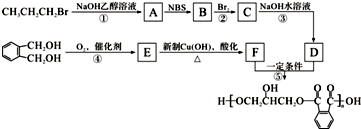
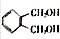
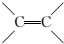 ,C的名称是1,2,3-三溴丙烷.
,C的名称是1,2,3-三溴丙烷.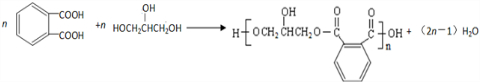 .
. 的同分异构体中同时符合下列条件的芳香族化合物共有6种.
的同分异构体中同时符合下列条件的芳香族化合物共有6种.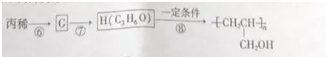
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2与D2 | B. | T2O与H2O | ||
| C. | ${\;}_{19}^{40}$K与${\;}_{19}^{39}$K | D. | 金刚石与石墨 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
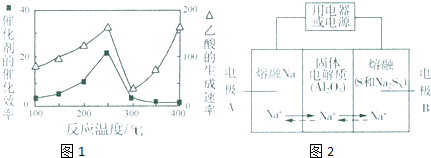
| 物质 | Na | S | Al2O3 |
| 熔点/℃ | 97.8 | 115 | 2050 |
| 沸点/℃ | 892 | 444.6 | 2980 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com