
【题目】随着科技的进步,合理利用资源、保护环境成为当今社会关注的焦点
(1)氨氮是造成水体富营养化的重要因素之一,用次氯酸钠水解生成的次氯酸将水中的氨氮(用NH3表示)转化为氮气除去,其相关反应的主要热化学方程式如下:
反应①:NH3(aq)+HClO(aq)= NH2Cl(aq)+H2O(l)△H1= akJmol﹣1
反应②:NH2Cl(aq)+HClO(aq)= NHCl2(aq)+H2O(I)△H2= bkJmol﹣1
反应③:2NHCl2(aq)+H2O(l)= N2(g)+HClO(aq)+3HCl(aq)△H3= ckJmol﹣1
① 2NH3(aq)+3HClO(aq)= N2(g)+3H2O(I)+3HCl(aq)的△H=______。
② 溶液pH对次氯酸钠去除氨氮有较大的影响(如图1所示)。在pH较低时溶液中有无色无味的气体生成,氨氮去除效率较低,其原因是_________________。
③ 用电化学法也可以去除废水中氨氮.在蒸馏水中加入硫酸铵用惰性电极直接电解发现氨氮去除效率极低,但在溶液中再加入一定量的氯化钠后,去除效率可以大大提高。反应装置如图2所示,b为电极__极,电解时阴极的电极反应式为_____________。

(2)“低碳经济”正成为科学家研究的主要课题。
① 以二氧化钛表面覆盖Cu2Al2O4 为催化剂,可以将CO2 和CH4 直接转化成乙酸。在不同温度下催化剂的催化效率与乙酸的生成速率如右图所示。250~300 ℃时,温度升高而乙酸的生成速率降低的原因是__________________。
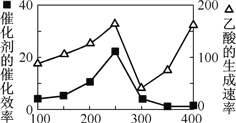
② 为了提高该反应中CO2的转化率,可以采取的措施是_____________。(写一条即可)
【答案】(2a+2b+c)kJmol﹣1HCl与NaClO反应生成HClO,HClO分解生成O2,与氨氮反应的HClO减少正极2H2O+2NH4++2e-=2NH3H2O+H2↑ 或 2H++2e-=H2↑温度超过250℃时,催化剂的催化效率降低增大反应压强或增大CO2的浓度
【解析】试题分析:以资源合理利用、环境保护为载体,考查盖斯定律的应用、电解原理、溶液的酸碱性对化学反应的影响、化学反应速率、化学平衡等知识,考查学生的读图能力和对图标的分析能力。
解析:(1)①根据盖斯定律,待计算的反应=2×①+2×②+③,所以反应的△H=(2a+2b+c)kJmol-1 。答案:(2a+2b+c)kJmol-1 。
②从图中可以看出,溶液pH较小时,次氯酸钠对氨氮去除率下降,而此时溶液中c(HClO)应当较pH大时更高,所以溶液中HClO一定参与了其它反应,结合溶液的组成及HClO的性质,HClO可能分解也可能与HCl反应生成Cl2,题目中已经说明“有无色无味的气体生成”,则应当是HClO的分解。答案:HCl与NaClO反应生成HClO,HClO分解生成O2,与氨氮反应的HClO减少。
③用惰性电极直接电解硫酸铵溶液相当于电解水,两极分别生成H2和O2,溶液中的氨氮不会直接消耗,也不会与产生的H2或O2反应,所以效率一定很差。加入NaCl后,电解仍然无法直接消耗氨氮,但是生成的氯气可以转变成HClO从而去除氨氮,因此Cl气必须从溶液下方产生,然后因此水充分接触得到HClO。所以a为电源负极,b为正极,阴极反应为2H++2e-=H2↑,溶液中H+主要来源于NH4+水解,则电极反应无也可以认为是NH4+和H2O。答案:正极 2H2O+2NH4++2e-=2NH3H2O+H2↑ 或 2H++2e-=H2↑
(2) ①读图可知,250~300 ℃时,不但乙酸的生成速率较低,而且催化剂的催化效率也很低,在其他条件不变的情况下,产生乙酸生成速率降低的原因是催化剂催化效率降低。答案:温度超过250℃时,催化剂的催化效率降低
②转化反应为CO2(g)+CH4(g)→CH3COOH(g),提高CO2的转化率可以是其他条件不变时设法使化学平衡正向移动,此处只能是加压。而若单从提高CO2转化率角度看,加入过量的CH4也可以实现这一目标。答案: 增大反应体系压强或充入更多的CH4。


 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案 芒果教辅暑假天地重庆出版社系列答案
芒果教辅暑假天地重庆出版社系列答案科目:高中化学 来源: 题型:
【题目】在一定条件下,短周期元素R所形成的离子![]() 与R2可发生如下反应:
与R2可发生如下反应: ![]() +2R2+6H+==3R+3H2O,下列关于元素R的叙述中一定正确的是( )
+2R2+6H+==3R+3H2O,下列关于元素R的叙述中一定正确的是( )
A. R原子的最外层上可能有4个电子
B. ![]() 中的R只能被还原
中的R只能被还原
C. R可能是碳元素
D. R最高价氧化物对应水化物为强酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列变化或数据与氢键无关的是 ( )
A. 氟化氢的沸点比氯化氢的沸点高
B. 氨分子与水分子形成一水合氨
C. 乙醇能跟水以任意比混溶
D. SbH3的沸点比PH3高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)分别用一种试剂除去下列各物质中的杂质(括号内为杂质),并写出离子方程式。
①Mg(Al)
试剂:________;离子方程式:_____________________。
②CO2(HCl)
试剂:________;离子方程式:_____________________。
(2)把下列离子方程式改写成化学方程式。
①2H++CO![]() CO2↑+H2O_____________________。
CO2↑+H2O_____________________。
②Al3++3OH—Al(OH)3↓_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【福建省龙岩市2017届高三5月综合能力测试(二)】2017年我国自主产权“全球首套煤基乙醇工业化项目”投产成功。“煤基乙醇”就是以煤为原料制备乙醇。乙醇能做燃料,可以添加到汽油中。下列说法错误的是
A. 煤制乙醇,有利于保护环境,实现能源充分利用
B. 煤制乙醇可缓解靠发酵产生乙醇导致的“与人类争粮”的局面
C. 等物质的量的乙醇、汽油完全燃烧,乙醇放出的热量多
D. 乙醇是世界公认的优良汽油添加剂,可有效改善汽油品质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对下列烯烃的命名,正确的是( )
A. 2-甲基-2-丁烯 B. 2,2-二甲基-1,3-丁二烯
C. 2-甲基-3-戊烯 D. 2-乙基-1-丙烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.质子数为6,中子数为7的原子的元素符号可表示为C
B.H2、SO2、CO三种气体都可用浓硫酸干燥
C.共价化合物溶于水,共价键被破坏,单质溶于水,共价键不被破坏
D.陶瓷、玻璃、水泥、大理石的主要成分都是硅酸盐
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼及其化合物在工业上有许多用途。以铁硼矿(主要成分为Mg2B2O5·H2O和Fe3O4,还有少量Fe2O3、FeO、CaO、Al2O3和SiO2等)为原料制备硼酸(H3BO3)的工艺流程如图所示:

回答下列问题:
(1)写出Mg2B2O5·H2O与硫酸反应的化学方程式_____________。为提高浸出速率,除适当增加硫酸浓度浓度外,还可采取的措施有_________(写出两条)。
(2)利用 的磁性,可将其从“浸渣”中分离。“浸渣”中还剩余的物质是______(写化学式)。
(3)“净化除杂”需先加H2O2溶液,作用是_______。 然后再调节溶液的pH约为5,目的是________。
(4)“粗硼酸”中的主要杂质是 (填名称)。
(5)以硼酸为原料可制得硼氢化钠(NaBH4),它是有机合成中的重要还原剂,其电子式为_______。
(6)单质硼可用于生成具有优良抗冲击性能硼钢。以硼酸和金属镁为原料可制备单质硼,用化学方程式表示制备过程___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】格林太太镶有两颗假牙:第一个是黄金的,第二颗是不锈钢的.令人百思不解的是,自从镶上假牙后,格林太太经常头疼、夜间失眠、心情烦躁某同学提出以下几种方案来治疗格林太太的“疾病”,理论上可行的是( )
A.把不锈钢牙都换成铝质假牙
B.把金质假牙换成铝质假牙
C.把不锈钢假牙换成金质假牙
D.在不锈钢假牙表面镀上一层金
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com