
| A. | Na2O2可用作呼吸面具中的供氧剂 | |
| B. | 氨气可做制冷剂 | |
| C. | Al(OH)3可作治疗胃酸过多的一种药剂 | |
| D. | 包装食品里常有硅胶、生石灰、还原铁粉等,其作用相同 |
分析 A.过氧化钠与二氧化碳反应生成氧气;
B.液态氨气汽化吸收大量的热;
C.氢氧化铝能够与盐酸反应,消耗氢离子;
D.硅胶、生石灰具有吸水性,还原铁粉具有还原性.
解答 解:A.过氧化钠与二氧化碳反应生成氧气,可用作供氧剂,故A正确;
B.液态氨气汽化吸收大量的热,可以做制冷剂,故B正确;
C.氢氧化铝能够与胃酸中的盐酸反应,消耗氢离子,所以可以治疗胃酸过多,故C正确;
D.包装食品里常有硅胶、生石灰为干燥剂,还原铁粉具有还原性为放氧化变质剂,其作用不相同,故D错误;
故选:D.
点评 本题多角度考查物质的性质及应用,侧重于化学与生活的考查,明确物质的性质是解题关键,注意对基础知识的积累.


科目:高中化学 来源: 题型:选择题
| A. | 往碳酸镁中滴加稀盐酸:CO32-+2H+═CO2↑+H2O | |
| B. | 浓烧碱溶液中加入铝片:Al+2OH-═AlO2-+H2↑ | |
| C. | 氯化钙与碳酸氢钾溶液混合:Ca2++CO32-═CaCO3↓ | |
| D. | 用惰性电极电解氯化镁溶液:Mg2++2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$Cl2↑+H2↑+Mg(OH)2↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X元素可以组成多种单质 | |
| B. | Y和Z可能在同一周期 | |
| C. | X与W形成的化合物和Z与W形成的化合物的化学键类型不同 | |
| D. | 元素X、Y、W的最高价氧化物对应水化物的酸性强弱:X<Y<W |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
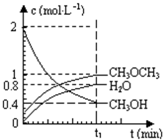 已知二甲醚是一种重要的清洁燃料,可以通过CH3OH分子间脱水制得:2CH3OH(g)?CH3OCH3(g)+H2O(g)△H=23.5kJ•mol-1.在T1℃,恒容密闭容器中建立上述平衡,体系中各组分浓度随时间变化如图所示.请回答下列问题:
已知二甲醚是一种重要的清洁燃料,可以通过CH3OH分子间脱水制得:2CH3OH(g)?CH3OCH3(g)+H2O(g)△H=23.5kJ•mol-1.在T1℃,恒容密闭容器中建立上述平衡,体系中各组分浓度随时间变化如图所示.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 能使潮湿的有色布条褪色 | |
| B. | 钠在氯气中燃烧,生成白色的烟 | |
| C. | 纯净的H2在Cl2中安静地燃烧,发出苍白色火焰,集气瓶口呈现白色烟雾 | |
| D. | 氯气能与水反应生成次氯酸和盐酸,久置氯水最终变为稀盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 举行“地球一小时”熄灯活动 | B. | 露天焚烧稻草和秸秆 | ||
| C. | 夏天将空调的温度设置在26℃以上 | D. | 生活垃圾分类回收处理 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
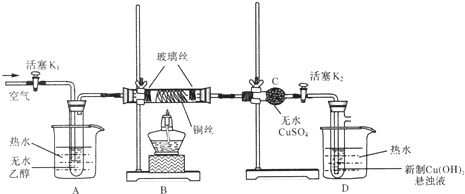
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com