
高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,不会造成二次污染。
己知高铁酸盐热稳定性差,工业上用湿法制备高铁酸钾的基本流程如下图所示:
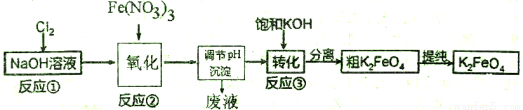
(1)①上述氧化过程中,发生反应的离子方程式是__________,在实际生产中一般控制反应温度30℃以下,其原因是__________。
②沉淀过程中加入浓KOH溶液可析出高铁酸钾(K2FeO4 ),这说明__________。
③在提纯K2FeO4中采用重结晶、洗涤、低温烘干的方法,沉淀洗涤方法是__________。
④某温度下,将C12通入NaOH溶液中,反应后得到NaCl,NaC1O,NaClO3的混合溶液,经测定ClO-与C1O3-离子的物质的量之比是1: 2,则C12与氢氧化钠反应时,被还原的氯元素和被氧化的氯元素的物质的量之比为__________。
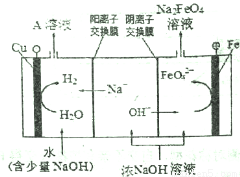
(2)工业上还可用通过电解浓NaOH溶液制备Na2FeO4,其工作原理如下图所示:阳极的电极反应式为__________,其中可循环使用的物质是__________。
(3)CO2可转化为碳酸盐,其中Na2CO3是一种用途广泛的碳酸盐.己知:25℃时,几种酸的电离平衡常数如下表所示。

25℃时,向一定浓度的Na2CO3溶液中分别滴入等物质的量浓度的下列溶液至过量:
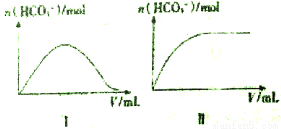
①NaHSO3②HNO3③HC1O,溶液中的n (HCO3-)与所加入溶液体积(V)的关系如上图所示。其中符合曲线Ⅱ的溶液为__________。
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源:2015-2016学年江西省高二下期中化学试卷(解析版) 题型:填空题
在下列事实中,什么因素影响了化学反应的速率?
(1)集气瓶中有H2和Cl2的混合气体,在瓶外点燃镁条时发生爆炸 。
(2)黄铁矿煅烧时要粉碎成细小的矿粒 。
(3)熔化的KClO3放出气泡很慢,撒入少量MnO2后很快产生气体 。
(4)同浓度、同体积的盐酸中放入体积同样大小的锌粒和镁块,产生气体有快有慢 。
(5)完全相同的石灰石分别在0.1 mol/L的盐酸和1 mol/L的盐酸中反应速率不同 。
(6)夏天的食品易变霉,冬天就不易发生该现象 。
查看答案和解析>>
科目:高中化学 来源:2016届海南省高三高考考前模拟十二化学试卷(解析版) 题型:选择题
现有三种常见治疗胃病药品的标签:

药品中所含的物质均能中和胃里过量的盐酸,下列关于三种药片中和胃酸的能力比较,正确的是( )
A.①=②=③ B.①>②>③
C.③>②>① D.②>③>①
查看答案和解析>>
科目:高中化学 来源:2016届福建省高三下学期周考五理科综合化学试卷(解析版) 题型:实验题
次磷酸钠(NaH2PO2)是化学镀镍的重要原料,工业上制备NaH2PO2·H2O的流程如下:
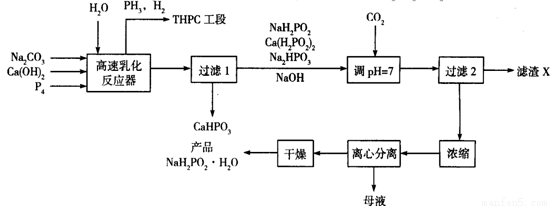
回答下列问题:
(1)NaH2PO2·H2O中磷元素的化合价为_________________。
(2)在反应器中加入乳化剂并高速搅拌的目的是______________________________。
(3)在反应器中发生多个反应,其中Ca(OH)2与P4反应生成次磷酸钙及磷化氢的化学方程式为________________________________________________________________。
(4)流程中通入CO2的目的是______________________________________________,滤渣X的化学式为______________________。
(5)流程中母液中的溶质除NaH2PO2外,还有的一种主要成分为___________________。
(6)含磷化氢的尾气可合成阻燃剂THPC{[P(CH2OH)4]Cl}。含PH3的废气可用NaClO和NaOH的混合溶液处理将其转化为磷酸盐,该反应的离子方程式为__________。
查看答案和解析>>
科目:高中化学 来源:2016届福建省高三下学期周考五理科综合化学试卷(解析版) 题型:选择题
能正确表示下列反应的离子方程式是( )
A.Fe2O3溶于过量氢碘酸溶液中:Fe2O3+6H++2I-═2Fe2++I2+3H2O
B.0.1mol/LNH4Al(SO4)2溶液与0.2mol/LBa(OH)2溶液等体积混合:
Al3++2SO42-+2Ba2++4OH-═2BaSO4↓+AlO2-+2H2O
C.用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:
2MnO4-+6H++5H2O2═2Mn2++5O2↑+8H2O
D.向次氯酸钠溶液中通入足量SO2气体:ClO-+SO2+H2O═HClO+HSO3-
查看答案和解析>>
科目:高中化学 来源:2016届安徽省六安市高三下综合训练十理综化学试卷(解析版) 题型:选择题
下列实验方案设计不合理的是
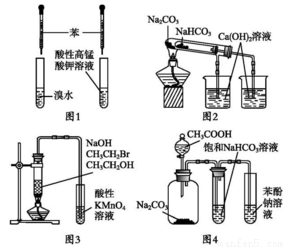
A.图1:验证苯中是否有碳碳双键
B.图2:验证NaHCO3和Na2CO3的热稳定性
C.图3:验证溴乙烷发生消去反应生成烯烃
D.图4:验证酸性CH3COOH>H2CO3>C6H5OH
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁鞍山一中高二下期中化学试卷(解析版) 题型:填空题
现有前四周期T、X、Y、Z、W、M六种元素,已知W、Z、X、T、Y五种非金属元素原子半径依次减小,其中W原子的s电子总数等于p电子总数的2倍.M原子的M能层上有4个未成对电子。请完成下列问题:
(1)写出W、Z、X、T四种元素第一电离能由大到小的顺序(用元素符号表示)________。
(2)M原子的基态电子排布式为________。
(3)根据VESPR理论,推断出由W与X两元素组成的最简单二价阴离子的空间构型为________,W原子的杂化类型为________。
(4)Y与T、X、Z、W所形成的最简单化合物的沸点由高到低顺序为(用化学式表示):________。
(5)WX2晶体的晶胞中最近的两微粒之间的距离(设晶胞棱长为a)是________。
(6)某蓝色晶体,其特征是M2+、M3+离子分别占据立方体互不相邻的顶点,而立方体的每条棱上均有一个WZ-。第三周期与冷水可以反应的金属元素R的离子位于立方体的恰当位置上。
①根据特征可知该晶体的化学式(用最简整数表示)为:________。
②该立方体________(填“是”或“否”)属于该物质的晶胞,R的离子在晶体中的位置是________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁鞍山一中高二下期中化学试卷(解析版) 题型:选择题
关于化学式[TiCl(H2O)5]Cl2•H2O的配合物的下列说法中正确的是( )
A.配位体是Cl-和H2O,配位数是9
B.中心离子是Ti4+,配离子是[TiCl(H2O)5]2+
C.内界和外界中的Cl-的数目比是1:2
D.加入足量AgNO3溶液,所有Cl-均被完全沉淀
查看答案和解析>>
科目:高中化学 来源:2015-2016学年甘肃会宁一中高一下期中文科化学试卷(解析版) 题型:选择题
将铜棒和锌棒用导线连接后插入稀硫酸溶液中,下列叙述中正确的是( )
A.该装置能形成原电池,其中锌是负极 B.该装置能形成原电池,其中铜是负极
C.该装置不能形成原电池 D.以上说法均不正确
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com