
| t/s | 0 | 5 | 15 | 25 | 35 |
| n(A)/mol | 1.0 | 0.85 | 0.81 | 0.80 | 0.80 |
| A. | 反应在前5s的平均速率v(A)=0.17mol•L-1•s-1 | |
| B. | 保持其他条件不变,升高温度,平衡时c(A)=0.41mol•L-1,则反应的△H>0 | |
| C. | 相同温度下,起始时向容器中充入2.0mol C,达到平衡时,C的转化率大于80% | |
| D. | 相同温度下,起始时向容器中充入0.20mol A、0.20mol B和1.0mol C,反应达到平衡前v(正)<v(逆) |
分析 某温度下,向2L恒容密闭容器中充入1.0mol A和1.0mol B,25min时处于平衡状态,平衡时A的物质的量为0.8mol,则:
A(g)+B(g)?C(g)
起始量(mol):1 1 0
变化量(mol):0.2 0.2 0.2
平衡量(mol):0.8 0.8 0.2
A.反应在前5s内消耗的A为(1-0.85)mol=0.15mol,根据v=$\frac{△c}{△t}$计算v(A);
B.平衡时A的浓度为0.4mol/L,保持其他条件不变,升高温度,新平衡时c(A)=0.41mol•L-1>0.4mol/L,说明升高温度平衡逆向移动;
C.相同温度下,起始时向容器中充入2.0mol C等效为开始加入2molA、2molB,进一步等效为在原平衡的基础上压强增大一倍,与原平衡相比,平衡正向移动,平衡时C的物质的量大于0.4mol,故开始通入2molC到达平衡时转化的C的物质的量小于(2-0.4)mol=1.6mol;
D.温度相同,平衡常数不变,根据K=$\frac{c(C)}{c(A)×c(B)}$计算平衡常数,再计算浓度商Qc,与平衡常数相比判断反应进行方向,进而确定反应达到平衡前v(正)、v(逆)相等大小.
解答 解:某温度下,向2L恒容密闭容器中充入1.0mol A和1.0mol B,25min时处于平衡状态,平衡时A的物质的量为0.8mol,则:
A(g)+B(g)?C(g)
起始量(mol):1 1 0
变化量(mol):0.2 0.2 0.2
平衡量(mol):0.8 0.8 0.2
A.反应在前5s内消耗的A为(1-0.85)mol=0.15mol,则v(A)=$\frac{\frac{0.15mol}{2L}}{5s}$=0.015mol/(L.s),故A错误;
B.平衡时A的浓度为0.4mol/L,保持其他条件不变,升高温度,新平衡时c(A)=0.41mol•L-1>0.4mol/L,说明升高温度平衡逆向移动,则正反应为放热反应,则反应的△H<0,故B错误;
C.相同温度下,起始时向容器中充入2.0mol C等效为开始加入2molA、2molB,进一步等效为在原平衡的基础上压强增大一倍,与原平衡相比,平衡正向移动,平衡时C的物质的量大于0.4mol,故开始通入2molC到达平衡时转化的C的物质的量小于(2-0.4)mol=1.6mol,则C的转化率小于$\frac{1.6mol}{2mol}$=80%,故C错误;
D.温度相同,平衡常数不变,该温度下平衡常数K=$\frac{c(C)}{c(A)×c(B)}$=$\frac{\frac{0.2}{2}}{\frac{0.8}{2}×\frac{0.8}{2}}$=0.625,起始时向容器中充入0.20mol A、0.20mol B和1.0mol C,此时浓度商Qc=$\frac{\frac{1}{2}}{\frac{0.2}{2}×\frac{0.2}{2}}$=50>K,故反应向逆反应进行,则反应达到平衡前v(正)<v(逆),故D正确,
故选:D.
点评 本题考查化学平衡计算,C选项也可以利用平衡常数计算具体的值,注意等效思想应用,掌握平衡常数应用,难度中等.


 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案科目:高中化学 来源: 题型:解答题
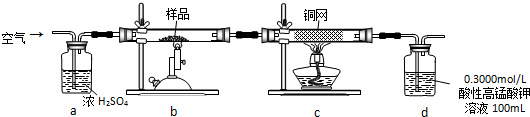
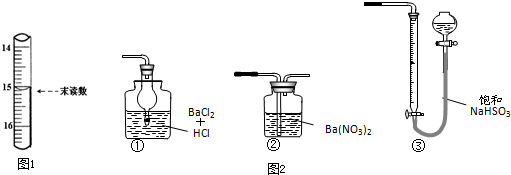
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
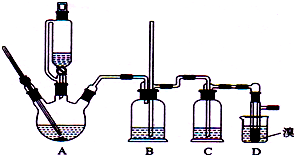 实验室制备1,2-二溴乙烷的反应原理如下:
实验室制备1,2-二溴乙烷的反应原理如下:| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | 一l30 | 9 | -1l6 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
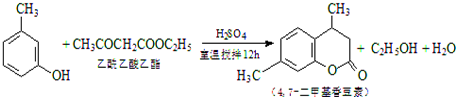
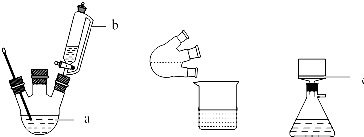
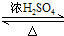 CH3COOCH2CH3+H2O,用饱和的碳酸钠溶液(填药品名称)收集粗产品,用分液(填操作名称)的方法把粗产品分离.
CH3COOCH2CH3+H2O,用饱和的碳酸钠溶液(填药品名称)收集粗产品,用分液(填操作名称)的方法把粗产品分离.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若甲乙两容器均为恒容容器,则x必等于2 | |
| B. | 若甲乙两容器均为恒压容器,则x必等于3 | |
| C. | 若甲为恒压容器,乙为恒容容器,且x不等于3,则n1必大于n2 | |
| D. | 若甲为恒容容器,乙为恒压容器,且x等于3,则n1必大于n2 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热 | |
| B. | 蒸馏时,温度计水银球靠近蒸馏烧瓶的底部 | |
| C. | 分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 | |
| D. | 检验溶液中是否含有NH4+:取少量试液于试管中,加入NaOH溶液并加热,用湿润的红色石蕊试纸检验产生的气体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com