
【题目】某有机物M的结构简式如下: ![]() 下列有关M的叙述中正确的是( )
下列有关M的叙述中正确的是( )
A.M的分子式为:C12H15O5N2
B.M可以发生水解反应、中和反应、加成反应、消去反应
C.M的水解产物中一定含有醇类
D.1 molM最多可以与1L4mol/L的NaOH溶液完全反应
 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案科目:高中化学 来源: 题型:
【题目】原子序数依次递增的甲、乙、丙、丁、戊是周期表中前30号元素,其中甲、乙、丙三元素的基态原子2p能级都有单电子,单电子个数分别是2、3、2;丁与戊原子序数相差18,戊元素是周期表中ds区的第一种元素。回答下列问题:
(1)甲能形成多种常见单质,在熔点很高的两种常见单质中,原子的杂化方式分别为______、__________。
(2)+1价气态基态阳离子再失去一个电子形成+2价气态基态阳离子所需要的能量称为第二电离能I2,依次还有I3、I4、I5…,推测丁元素的电离能突增应出现在第________电离能。
(3)戊的基态原子有________种形状不同的原子轨道;
(4)甲、乙分别都能与丙形成原子个数比为 1:3的微粒,则该两种微粒的空间构型分别为:_________________ ;__________________。
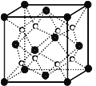
(5)丙和丁形成的一种离子化合物的晶胞结构如右图,该晶体中阳离子的配位数为_________ 。距一个阴离子周围最近的所有阳离子为顶点构成的几何体为_______________。已知该晶胞的密度为ρ g/cm3,阿伏加德罗常数为NA,该化合物的相对分子质量为 M,则该晶胞中黑球的半径r =_____cm。(用含ρ、NA的计算式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝、钠混合物投入足量的水中,充分反应后,得到澄清溶液,并收集到4.48L H2(标准状况),若钠的物质的量为0.1mol,则铝的物质的量为( )
A.0.1 mol
B.0.2 mol
C.0.05 mol
D.0.025 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向100mL未知浓度的AlCl3和MgCl2的混合溶液中逐滴加入0.1 molL﹣1的NaOH溶液,生成沉淀的质量随加入NaOH溶液体积的变化关系如图所示,则AlCl3的浓度为( ) 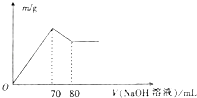
A.0.005 molL﹣1
B.0.01 molL﹣1
C.0.2 molL﹣1
D.0.1 molL﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成氨技术的创立开辟了人工固氮的重要途径,其研究自正确的理论指导,合成氨反应N2+3H2![]() 2NH3的平衡常数K值和温度的关系如下:
2NH3的平衡常数K值和温度的关系如下:
温度/℃ | 360 | 440 | 520 |
K值 | 0.036 | 0.010 | 0.0038 |
(1)①由表中数据可知该反应为______反应(填“放热”或“吸热”)
②理论上,为了增大平衡时H2的转化率,可采取的措施是______________(填字母序号)。
a.增大压强 b.使用合适的催化剂
c.升高温度 d.及时分离出产物中的NH3
(2)原料气H2可通过反应CH4(g)+H2O(g) ![]() CO(g)+3H2(g)获取,已知该反应中,当初始混合气中的
CO(g)+3H2(g)获取,已知该反应中,当初始混合气中的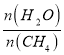 恒定时,温度、压强对平衡混合气中CH4含量的影响如图所示:
恒定时,温度、压强对平衡混合气中CH4含量的影响如图所示:
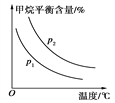
①图中,两条曲线表示压强的关系是p1________p2(填“>”、“=”或“<”)。
②该反应为________反应(填“吸热”或“放热”)。
(3)原料气H2还可通过反应CO(g)+H2O(g) ![]() CO2(g)+H2(g)获取。T ℃时,向容积固定为2 L的容器中充入1 mol水蒸气和1 mol CO,反应达平衡后,测得CO2的浓度为0.3 mol·L-1,则平衡时CO的转化率为________
CO2(g)+H2(g)获取。T ℃时,向容积固定为2 L的容器中充入1 mol水蒸气和1 mol CO,反应达平衡后,测得CO2的浓度为0.3 mol·L-1,则平衡时CO的转化率为________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】加热试管中的NH4HCO3,使放出的气体依次通过盛有足量过氧化钠的干燥管、足量浓硫酸的洗气瓶,最后得到的气体是
A. NH3 B. O2 C. H2O D. CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述错误的是
A. 通常情况下,甲烷跟强酸、强碱和强氧化剂都不反应
B. 甲烷化学性质稳定,不能被任何氧化剂氧化
C. 甲烷与Cl2反应无论生成CH3Cl、CH2Cl2、CHCl3还是CCl4,都属于取代反应
D. 甲烷的四种有机取代产物有一种气态,其余三种为液态且都不溶于水
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com