
| A. | 150mL 1mol/L的NaCl溶液 | B. | 75mL 1mol/L的FeCl3溶液 | ||
| C. | 150mL 0.5mol/L的MgCl2溶液 | D. | 75mL 2mol/L的NH4Cl溶液 |
分析 根据化学式可知1mol•L-1的AlCl3溶液中c(Cl-)为3mol/L,结合各选项中化学式判断溶液中c(Cl-),注意离子的浓度与溶液的体积无关,与物质的构成有关.
解答 解:50mL1mol/L的AlCl3溶液中的Cl-浓度为3mol/L.
A.150ml1mol/L的NaCl溶液中Cl-浓度为1mol/L,与50mL1mol/L的AlCl3溶液中的Cl-浓度不相等,故A错误;
B.75mL1mol/L氯化铁溶液中,Cl-浓度为1mol•L-1×3=3mol•L-1,与50mL1mol/L的AlCl3溶液中的Cl-浓度相等,故B正确;
C.150ml0.5mol/L的氯化镁溶液中Cl-浓度为1mol/L,与50mL1mol/L的AlCl3溶液中的Cl-浓度不相等,故C错误;
D.75ml2mol/L的氯化铵溶液中Cl-浓度为2mol/L,与50mL1mol/L的AlCl3溶液中的Cl-浓度不相等,故D错误.
故选B.
点评 本题考查物质的量浓度的计算与理解,题目难度不大,注意溶液中溶质离子的浓度与溶液体积无关,只取决于物质电离出的离子的数目多少与溶质的浓度.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4+、Ba2+、Cl-、NO3- | B. | Na+、K+、SO42-、NO3- | ||
| C. | Fe3+、Cu2+、SO42-、Cl- | D. | Cl-、K+、HCO3-、Al3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 该烃有三种同分异构体 | |
| B. | 所得产物中,气体的物质的量是液体的1.2倍 | |
| C. | 该烃必有一种同分异构体的核磁共振氢谱有两组峰 | |
| D. | 该烃与2,6二甲基-3,5-二乙基-4-异丙基-庚烷是同系物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 氮、磷、砷是同族元素,该族元素单质及其化合物在农药、化肥等方面有重要应用.请回答下列问题.
氮、磷、砷是同族元素,该族元素单质及其化合物在农药、化肥等方面有重要应用.请回答下列问题.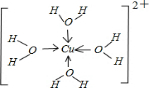 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 ⑧
⑧
| A. | ①②④⑤⑥⑧ | B. | ①②③④⑥⑧ | C. | ②③④⑤⑦⑧ | D. | ①②④⑥⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 品红溶液 | B. | 氨水 | ||
| C. | 酸性高锰酸钾溶液 | D. | 以上都能 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com