
分析 (1)常温下pH=12的氢氧化钠溶液中,氢氧根离子抑制了水的电离,溶液中的氢离子为水电离的,据此计算出水电离的氢离子浓度;
(2)①常温下pH=12的氢氧化钠溶液中,氢氧根离子浓度为:0.01mol/L,pH=11的溶液中氢氧根离子浓度为0.001mol/L,稀释过程中溶质的物质的量不变,据此列式计算出稀释后溶液体积,再计算出需要加入水的体积;
②pH=10的氢氧化钠溶液中氢氧根离子浓度为0.0001mol/L,设加入pH=10的氢氧化钠溶液体积为V,则:$\frac{(0.0001×V+0.01×0.1)mol}{VL+0.1L}$=0.001mol/L,据此计算出需要加入该氢氧化钠溶液体积.
解答 解:(1)常温下pH=12的氢氧化钠溶液中,氢氧根离子抑制了水的电离,溶液中的氢离子为水电离的,则水电离的氢离子浓度为:c(H+)=1.0×10-12mol•L-1,
故答案为:1.0×10-12mol•L-1;
(2)①常温下pH=12的氢氧化钠溶液中,氢氧根离子浓度为:0.01mol/L,pH=11的溶液中氢氧根离子浓度为0.001mol/L,稀释过程中溶质的物质的量不变,则稀释后溶液体积为:$\frac{0.01mol/L×0.1L}{0.001mol/L}$=11L=1000mL,需要加入的蒸馏水体积为:1000mL-100mL=900mL,
故答案为:900;
②pH=10的氢氧化钠溶液中氢氧根离子浓度为0.0001mol/L,设加入pH=10的氢氧化钠溶液体积为V,则:$\frac{(0.0001×V+0.01×0.1)mol}{VL+0.1L}$=0.001mol/L,解得:V=1L=1000mL,
故答案为:1000.
点评 本题考查了溶液pH的简单计算、水的电离及其影响,题目难度中等,注意明确酸碱溶液抑制了水的电离,熟练掌握溶液酸碱性与溶液pH的关系及计算方法.


科目:高中化学 来源: 题型:解答题

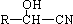 $\stackrel{H_{2}O/H+△}{→}$
$\stackrel{H_{2}O/H+△}{→}$ 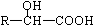
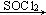
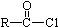 $\stackrel{R′OH}{→}$ RCOORˊ(R、Rˊ代表烃基)
$\stackrel{R′OH}{→}$ RCOORˊ(R、Rˊ代表烃基)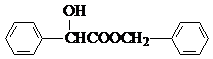 .
.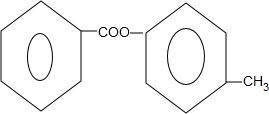 +2NaOH$\stackrel{△}{→}$
+2NaOH$\stackrel{△}{→}$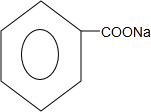 +
+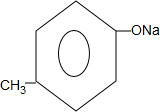 +H2O.
+H2O.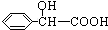 的同分异构体中:①能发生水解反应;②能发生银镜反应;③能与氯化铁溶液发生显色反应;④含氧官能团处在对位.满足上述条件的同分异构体共有3种(不考虑立体异构),写出核磁共振氢谱图中有五个吸收峰的同分异构体的结构简式
的同分异构体中:①能发生水解反应;②能发生银镜反应;③能与氯化铁溶液发生显色反应;④含氧官能团处在对位.满足上述条件的同分异构体共有3种(不考虑立体异构),写出核磁共振氢谱图中有五个吸收峰的同分异构体的结构简式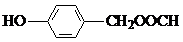 .
.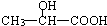 )的路线(其它试剂任选).
)的路线(其它试剂任选).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 431 kJ•mol-1 | B. | 946 kJ•mol-1 | C. | 649 kJ•mol-1 | D. | 896 kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 容器中SO2、O2和SO3共存 | |
| B. | SO2和SO3的物质的量浓度相等 | |
| C. | 容器中SO2、O2、SO3的物质的量之比为2:1:2 | |
| D. | 反应器内压强不再随时间发生变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{a}{V}$mol/L | B. | $\frac{b}{V}$ mol/L | ||
| C. | $\frac{a-2b}{V}$ mol/L | D. | $\frac{a-b}{V}$mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加热,将湿润的红色石蕊试纸放在管口 | |
| B. | 加氢氧化钠溶液,加热,将湿润的酚酞试纸放在管口 | |
| C. | 加氢氧化钠溶液,加热,将蘸有浓盐酸的玻璃棒放在试管口 | |
| D. | 加氢氧化钠溶液,加热,将湿润的红色石蕊试纸放在管口 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{m-n-2}{w•m}$ mol | B. | $\frac{w(m-n)}{m}$ mol | C. | w($\frac{m-n-2}{m}$) mol | D. | w($\frac{m-n+2}{m}$) mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有①③⑤ | B. | 只有①④⑤ | C. | 只有②③⑤ | D. | 全部 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com