
【题目】生物质资源是一种污染小的可再生能源。生物质的主要转化途径及主要产物如下图。

(1)下列有关说法正确的是_____________。
a.生物质能,本质上能量来源于太阳能
b.由纤维素水解获得的乙醇作燃料是利用了生物质能
c.生物质裂解获得的汽油、柴油等属于纯净物
d.由植物秸杆等厌氧发酵获得的沼气,主要成分是甲烷
(2)由生物质能获得的CO和H2,可以合成甲醇和二甲醚(CH3OCH3)及许多烃类物质。当两者1∶1催化反应,其原子利用率达100%,合成的物质可能是____________。
a.汽油 b.甲醇(CH3OH) c.甲醛(HCHO) d.乙酸(CH3COOH)
(3)甲醇是一种重要的化工原料,工业上合成甲醇的反应:CO(g)+2H2(g) ![]() CH3OH(g) △H=﹣90.8kJ·mol-1。若在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:
CH3OH(g) △H=﹣90.8kJ·mol-1。若在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:
容器 | 甲 | 乙 | 丙 |
反应物投入量 | 1molCO 、2molH2 | 1mol CH3OH | 2molCO、4molH2 |
CH3OH的浓度(mol/L) | c1 | c2 | c3 |
反应的能量变化 | 放出Q1 kJ | 吸收Q2 kJ | 放出Q3 kJ |
平衡常数 | K1 | K2 | K3 |
反应物转化率 | α 1 | α 2 | α 3 |

下列说法正确的是________________。
a.c1 = c2 b.2Q1 = Q3 c.K1 = K3 d.α2 + α3<100%
(4)某实验小组设计如图b所示的电池装置,正极的电极反应式为__________________。
【答案】 abd cd a c O2 + 2H2O + 4e- = 4OH-
【解析】(1)a.生物质本质上能来源于太阳能,故A正确; b.乙醇来源于纤维素,属于生物质能,故B正确;c.汽油、柴油等属于混合物,故C错误;d.沼气的主要成分是甲烷,故D正确;故选abd;
(2)“绿色化学”能实现零排放,即反应物中的原子利用率达到100%,也就是说反应类型一般是化合反应,且反应后产物中的各原子数目比不变,CO和H2在一定条件下按照不同的比例反应,可假定反应时的化学计量数之比为1:1,则只要各选项中的化学式能化为形式(CO)n(H2)n,都是正确的,汽油是混合物,甲醇(CH4O)可变为(CO)1(H2)2,甲醛(CH2O)可变为(CO)1(H2)1,乙酸(C2H4O2)可变为(CO)2(H2)2,故答案为cd;
(3)a.1molCO、2molH2与1molCH3OH的等效的,平衡时CH3OH的浓度c1=c2,故a正确;b.丙的反应物投入量是甲的二倍,容积相同,压强比甲大,平衡向右进行,放出的热量2Q1<Q3,故b错误;c.平衡常数只与温度有关,温度相同,平衡常数相同,故c正确;
d.无法求出转化率,故d错误,故答案为ac;
(4)电池的正极发生还原反应,氧气在正极发生还原反应,电解质溶液为KOH溶液,应写为O2+2H2O+4e-=4OH-。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】下列各数值表示有关元素的原子序数,其所表示的各原子组中能以离子键相互结合成稳定化合物的是( )
A.6与16B.11与17C.14与8D.10与19
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学反应其ΔH=122 kJ/mol,S=231 J/(mol·K),则此反应在下列哪种情况下可自发进行
A.在任何温度下都能自发进行
B.在任何温度下都不能自发进行
C.仅在高温下自发进行
D.仅在低温下自发进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室需要0.1mol/L NaOH溶液450mL和0.5mol/L硫酸溶液450mL.根据这两种溶液的配制情况回答下列问题:
(1)如图所示的仪器中配制溶液肯定不需要的是(填序号),仪器C的名称是 , 本实验所需玻璃仪器E规格和名称是 . 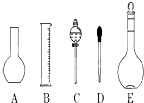
(2)下列操作中,容量瓶所不具备的功能有(填序号).
A.配制一定体积准确浓度的标准溶液
B.长期贮存溶液
C.用来加热溶解固体溶质
D.量取一定体积的液体
(3)在配制NaOH溶液实验中,其他操作均正确.若定容时仰视刻度线,则所配制溶液浓度0.1mol/L(填“大于”“等于”或“小于”,下同).若NaOH溶液未冷却即转移至容量瓶定容,则所配制溶液浓度0.1mol/L.
(4)根据计算得知,所需质量分数为98%、密度为1.84g/cm3的浓硫酸的体积为mL(计算结果保留一位小数).如果实验室有10mL、25mL、50mL量筒,应选用mL规格的量筒最好.
(5)如果定容时不小心超过刻度线,应如何操作 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图中X、Y、Z为单质,其他为化合物,它们之间存在如下转化关系(部分产物已略去)。其中,A俗称磁性氧化铁,E是不溶于水的酸性氧化物,能与氢氟酸反应。
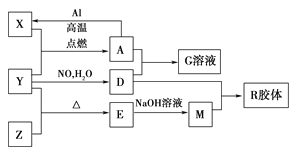
回答下列问题:
(1)组成单质Z的元素在周期表中的位置是________;M中存在的化学键类型为________;R的化学式是______________。
(2)一定条件下,Z与H2反应生成ZH4,ZH4的电子式为____________。
(3)已知A与1 mol Al反应转化为X时(所有物质均为固体),放出a kJ热量。写出该反应的热化学方程式:_____________________________________________________________。
(4)写出A和D的稀溶液反应生成G的离子方程式:__________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况下VL氨气溶解在1L水中(水的密度近似为lg/ml),所得溶液的密度为ρg/ml,质量分数为W,物质浓度为cmol/L,则下列关系中不正确的是
A. W= 17V/(17V+22400) B. W= 17c/(l000ρ)
C. ρ= (17V+ 22400)/(22.4 + 22.4V) D. c=1000Vρ/(17V+22400)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了除去粗盐中的Ca2+、Mg2+、SO ![]() 及泥沙,可将粗盐溶于水,然后进行下列5项操作:①过滤;②加过量NaOH溶液;③加适量盐酸;④加过量Na2CO3溶液;⑤加过量BaCl2溶液.正确的操作顺序可以是( )
及泥沙,可将粗盐溶于水,然后进行下列5项操作:①过滤;②加过量NaOH溶液;③加适量盐酸;④加过量Na2CO3溶液;⑤加过量BaCl2溶液.正确的操作顺序可以是( )
A.⑤②④③①
B.④①②⑤③
C.②⑤④①③
D.①④②⑤③
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com