
下列物质性质的变化规律,与化学键的强弱无关的是( )
A.F2、Cl2、Br2、I2的熔点、沸点逐渐升高
B.HF、HCl、HBr、HI的热稳定性依次减弱
C.金刚石的硬度、熔点、沸点都高于晶体硅
D.NaF、NaCl、NaBr、NaI的熔点依次降低
科目:高中化学 来源: 题型:
氯化铯晶胞(晶体重复的结构单位)如图甲所示,该晶体中Cs+与Cl-的个数比为1∶1,化学式为CsCl。若某晶体晶胞结构如图乙所示,其中含有A、B、C三种元素的粒子,则该晶体中A、B、C的粒子个数比为( )
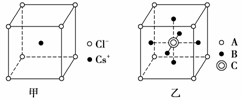
A.8∶6∶1 B.4∶3∶1
C.1∶6∶1 D.1∶3∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
BGO是我国研制的一种闪烁晶体材料,它是锗酸铋的简称。已知:①在BGO中,锗处于其最高价态;②在BGO中,铋的价态与铋跟氯形成某种共价氯化物时所呈的价态相同,在此氯化物中,铋具有最外层8电子稳定结构;③BGO可看作是由锗和铋两种元素的氧化物所形成的复杂氧化物,且在BGO晶体的化学式中,这两种氧化物所含氧的总质量相同。请填空。
(1)锗的铋的元素符号分别是________和________。
(2)BGO晶体的化学式是______________。
(3)BGO晶体中所含铋的氧化物的化学式是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
如图所示为氯化钠晶体的晶胞。请回答:
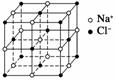
(1)Cl-的配位数为________;晶体中氯离子按______型方式进行紧密堆积,钠离子填在氯离子所构成的空隙中。
(2)一个氯化钠晶胞中实际包含________个氯离子,________个钠离子。
查看答案和解析>>
科目:高中化学 来源: 题型:
干冰和二氧化硅晶体同属ⅣA族元素的最高价氧化物,它们的熔、沸点差别很大的原因是( )
A.二氧化硅的相对分子质量大于二氧化碳的相对分子质量
B.C===O键键能比Si—O键键能小
C.干冰为分子晶体,二氧化硅为原子晶体
D.干冰易升华,二氧化硅不能
查看答案和解析>>
科目:高中化学 来源: 题型:
有A、B、C三种晶体,分别由H、C、Na、Cl 4种元素的一种或几种形成,对这3
种晶体进行实验,结果如下表。
| 熔点/℃ | 硬度 | 水溶性 | 导电性 | 水溶液与 Ag+反应 | |
| A | 811 | 较大 | 易溶 | 水溶液或熔融导电 | 白色沉淀 |
| B | 3 550 | 很大 | 不溶 | 不导电 | 不反应 |
| C | -114.2 | 很小 | 易溶 | 液态不导电 | 白色沉淀 |
(1)晶体的化学式分别为:
A____________;B____________;C____________。
(2)晶体的类型分别为:
A____________;B____________;C____________。
(3)晶体中粒子间的作用力分别为:
A____________;B____________;C____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
NH3分子空间构型是三角锥形,而CH4是正四面体形,这是因为( )
A.两种分子的中心原子杂化轨道类型不同,NH3为sp2杂化,而CH4是sp3杂化
B.NH3分子中N原子形成3个杂化轨道,CH4分子中C原子形成4个杂化轨道
C.NH3分子中有一对未成键的孤对电子,它对成键电子的排斥作用较强
D.NH3分子中有3个σ键,而CH4分子中有4个σ键
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于苯分子的结构与性质的描述错误的是( )
A.苯分子呈平面正六边形,六个碳碳键完全相同,键角皆为120°
B.苯分子中C原子采取sp2杂化,六个碳原子中未参与杂化的2p轨道以“肩并肩”的方式形成一个大π键
C.苯分子中的碳碳双键是介于单键和双键之间的一种特殊类型的键
D.苯能使溴水褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中不正确的是( )
A.在共价化合物中不可能含有离子键
B.非金属元素之间形成的化学键一定是共价键
C.含有共价键的化合物不一定是共价化合物
D.含有离子键的化合物一定是离子化合物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com