
下列说法错误的是( )
A.热化学方程式各物质前的化学计量数不表示分子个数,只代表物质的量
B.热化学方程式未注明温度和压强时,ΔH表示标准状况下的数据
C.同一化学反应,化学计量数不同,ΔH不同;化学计量数相同而状态不同,ΔH也不相同
D.化学反应过程所吸收或放出的热量与参加反应物质的物质的量成正比
科目:高中化学 来源:2015-2016学年陕西省高一下学期期中考试化学试卷(解析版) 题型:选择题
一定温度下,对反应2A(g)+B(s)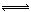 2C(g)能说明其达到平衡状态的是( )
2C(g)能说明其达到平衡状态的是( )
A.容积中A、B、C三者共存
B.单位时间内反应的A与生成的C的物质的量之比为1:1
C.c(A):c(B):c(C)=2:1:2
D.气体的总质量不再发生变化
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省济宁市任城区高二下学期期中考试化学试卷(解析版) 题型:选择题
以2-丁烯为原料,通过一步反应(所需其它试剂自选)无法完成的是
A.2-丁醇 B.2,3-二氯丁烷 C.2-溴丁烷 D.2,3-丁二醇
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林省高一下学期期中考试化学试卷(解析版) 题型:实验题
50ml0.50mol·L-1盐酸与50mL0.55mol·L-1NaOH溶液在如下图所示的装置中进行中和反应。通过测定反应过程中放出的热量可计算中和热。回答下列问题:
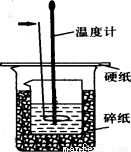
(1)箭头所指仪器的名称是 。作用是 。
(2)实验所用的NaOH溶液体积与盐酸相同,但浓度却比盐酸大的原因是 。
(3)用相同浓度和体积的醋酸代替HCl溶液进行上述实验,放出的热量会 。(填“偏大”“偏小”或“无影响”)。测得的△H会 (填“偏大”“偏小”或“无影响”)。
(4)上图所示实验装置存在着一处错误,这处错误是 。
(5)实验测得中和热△H = - 57.3 kJ·mol –1若忽略能量的损失,请你计算出实验前后温度的差值△t (保留一位小数,水的比热容c=4.18J/(g·℃)两种溶液的密度近似取1g/ml )
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林省高一下学期期中考试化学试卷(解析版) 题型:选择题
已知反应:① 2C(s)+O2(g)=2CO(g) ΔH=-221 kJ/mol
② 稀溶液中,H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ/mol
下列结论正确的是( )
A.碳的燃烧热为△H = -110.5 kJ/mol
B.1molC(s)所具有的能量一定高于1molCO(g)所具有的能量
C.稀硫酸与稀NaOH溶液反应的中和热为△H = -57.3 kJ/mol
D.稀醋酸与稀NaOH溶液反应生成1 mol水,也放出57.3 kJ 热量
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林省高一下学期期中考试化学试卷(解析版) 题型:选择题
同周期的X、Y、Z三种元素,它们最高价氧化物对应水化物分别是HXO4、H2YO4、H3ZO4 ,则下列判断正确的是( )
A.含氧酸的酸性H3ZO4>H2YO4>HXO4,
B.HXO4、H2YO4、H3ZO4一定都是强酸
C.元素的负化合价的绝对值按X、Y、Z减小
D.气态氢化物的稳定性按X、Y、Z的顺序减弱
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林省高二下学期期中考试化学试卷(解析版) 题型:填空题
黄铁矿被称“愚人金”,化学成分是FeS2,晶体属正方体晶系的硫化物矿物。室温为非活性物质。温度升高后变得活泼。在空气中氧化成三氧化二铁和二氧化硫,主要用于接触法制造硫酸:

回答下列问题:
(1)在FeS2中的S2-的核外电子排布式是________________________;
(2)常温下Fe3+比Fe2+要更加稳定的原因是__________________________________;
(3)将FeS2与稀盐酸反应得到H2S2,H2S2分子中,共价键的类型是___________________;FeS2氧化得到SO2,在SO2分子中的S原子的杂化轨道类型是______________________ ,写出两个与SO2互为等电子体的分子或离子_______________________。-
(4)H2SO4和H2SO3都是S的含氧酸,请用结构知识解释H2SO4比H2SO3酸性强的原因:
_____________________________________________________________________。
(5)FeS2的晶体中的Fe2+离子的排列方式如下图。
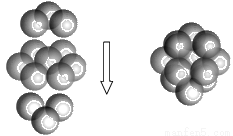
①每个Fe2+周围最近的等距离的S22-离子有____________个。
②已知FeS2的晶胞参数是a0=0.54nm,它的密度为_____________________g·cm-3(列式并计算,阿伏加德罗常数为6.02×1023)。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林省高二下学期期中考试化学试卷(解析版) 题型:选择题
已知次氯酸分子的结构式为H﹣O﹣Cl,下列有关说法正确的是( )
A.依据其结构判断该含氧酸为强酸
B.O原子与H、Cl都形成σ键
C.该分子为直线形非极性分子
D.该分子的电子式是H:O:Cl
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江苏省高一下学期期中考试化学试卷(解析版) 题型:选择题
下列反应过程中的能量变化情况符合右图的是

A.铝热反应
B.氧化钙和水反应
C.C+H2OCO+H2
D.一氧化碳气体的燃烧
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com