
已知2-丁烯有顺、反两种异构体,在某条件下两种气体处于平衡,下列说法正确的是:( )
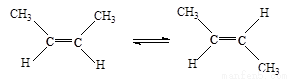 △H=-4.2 kJ/mol
△H=-4.2 kJ/mol
A.顺-2-丁烯比反-2-丁烯稳定
B.顺-2-丁烯的燃烧热比反-2-丁烯大
C.加压和降温有利于平衡向生成顺-2-丁烯反应方向移动
D.它们与氢气加成反应后的产物具有不同的沸点
科目:高中化学 来源:2015-2016学年江西省高一下学期期未化学试卷(解析版) 题型:选择题
下列有关资源的开发利用说法正确的是 ( )
A.从海带中提取碘单质的过程一定涉及氧化还原反应
B.从海水中可以得到NaCl,电解NaCl溶液可制备Na和Cl2
C.天然气、乙醇和水煤气分别属于化石能源、不可再生能源和二次能源
D.Cu、Al、Hg可以分别用热还原CuO、电解AlCl3和热分解HgO冶炼得到
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东省肇庆市高二下学期期末化学试卷(解析版) 题型:填空题
某芳香烃C7H8是一种重要的有机化工原料,研究部门以它为初始原料设计出如下
转化关系图(部分产物、合成路线、反应条件略去)。其中A是一氯代物,F是一种功能高分子,链节组成为(C7H5NO)。
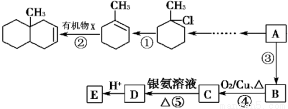

已知:(ⅰ) 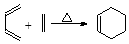
(ⅱ)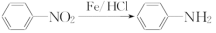 (苯胺,易被氧化)
(苯胺,易被氧化)
(1)反应①的反应类型是 ,反应⑥的反应类型是 。
(2)反应③的反应条件为 ;有机物X的结构简式为 。
(3)鉴别B和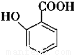 不可选用的试剂有 (填标号)。
不可选用的试剂有 (填标号)。
A.FeCl3溶液 b.浓溴水 C.Na d.NaHCO3溶液
(4)写出反应⑤的化学方程式: ;
若F为高分子化合物,则反应⑦的化学方程式为 。
(5)根据已有知识并结合相关信息,写出以芳香烃C7H8为原料制备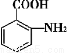 的合成路线流程图(无机试剂任用)。合成路线流程图示例如下(已知
的合成路线流程图(无机试剂任用)。合成路线流程图示例如下(已知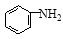 容易被氧化剂氧化):
容易被氧化剂氧化):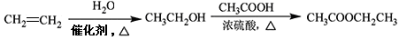
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东省肇庆市高二下学期期末化学试卷(解析版) 题型:选择题
下列叙述错误的是( )
A. 采用多次盐析和溶解,可以分离提纯蛋白质
B. 乙烯和苯都能使溴水褪色,褪色的原因相同
C. 淀粉、油脂、蛋白质都能水解,但水解产物不同
D. 煤油可由石油分馏获得,可用作燃料和保存少量金属钠
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东省高二下学期期末理科化学试卷(解析版) 题型:实验题
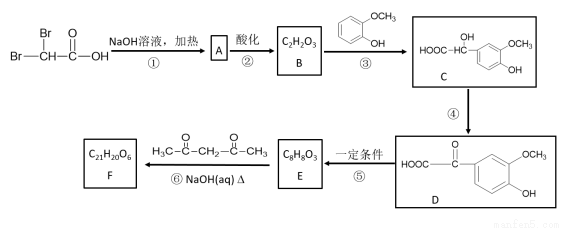
有机物F(C21H20O6)在临床医学上具有预防肿瘤的作用,其合成路线如下:其中反应③中反应物的原子利用率为100%。
已知:
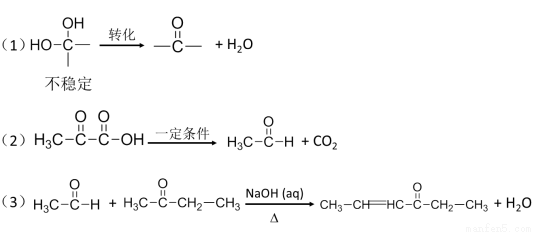
请回答下列问题:
(1)B中含有的官能团名称是___________。③的反应类型为__________。
(2)反应①的化学方程式是________________。反应④的化学方程式是___________。
(3)E的结构简式是______________。F的结构简式是__________________。
(4)E的同分异构体中,同时符合下列两个条件的共有种,其中核磁共振氢谱中有4组吸收峰的同分异构体的结构简式为______________。
①苯环上的一取代物只有2种;
②1 mol该物质与足量NaOH溶液反应时,反应消耗3 mol NaOH
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东省高二下学期期末理科化学试卷(解析版) 题型:选择题
下列关于一些有机物在合适条件下的化学反应说法正确的是( )
A. 能催化氧化生成醛
能催化氧化生成醛
B. 能在浓硫酸的作用下生成烯
能在浓硫酸的作用下生成烯
C.CH3Br 能在氢氧化钠的乙醇溶液的作用下生成醇
D. 既能与酸反应也能与碱反应生成盐
既能与酸反应也能与碱反应生成盐
查看答案和解析>>
科目:高中化学 来源:2015-2016学年甘肃省高一下学期期末化学试卷(解析版) 题型:填空题
已知A、B、C、D四种元素的原子序数为A<B<C<D,且都小于18。A、B位于同周期,A元素的原子最外层电子数是次外层电子数的2倍,B元素的原子最外层电子数是次外层电子数的3倍。C、D同周期, C元素的原子半径在同周期中最大,D元素的原子最外层电子数比次外层电子数少1个。试推断:
(1)请写出A、B、C、D四种元素的元素符号:A________,B________,C________,D_______。
(2)画出D元素的离子结构示意图_______________。
(3)AB2中存在的化学键是 (离子键、共价键), CD的电子式为 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年甘肃省高一下学期期末化学试卷(解析版) 题型:选择题
一定条件下反应N2(g)+3H2(g) 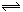 2NH3(g)在10 L的密闭容器中进行,测得2 min内,N2的物质的量由20mol减小到8mol,则2min内N2的反应速率为 ( )
2NH3(g)在10 L的密闭容器中进行,测得2 min内,N2的物质的量由20mol减小到8mol,则2min内N2的反应速率为 ( )
A.1.2 mol/(L·min)
B.6 mol/(L·min)
C.0.6 mol/(L·min)
D.0.4 mol/(L·min)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高二下学期第四次月考化学试卷(解析版) 题型:填空题
氯化铜、氯化亚铜是重要的化工原料,广泛地用作有机合成催化剂。
I.实验室中以粗铜(含杂质Fe)为原料制备铜的氯化物。现用左图所示的实验仪器及药品来制备纯净、干燥的氯气并与粗铜反应(铁架台、铁夹、酒精灯已省略)。按要求回答下列问题:

(1)按气流方向连接各仪器接口顺序是:a→ 、 → 、 → 、 → 。
(2)写出加热时硬质试管中主要发生反应的化学方程式 。
II.若将上述实验制得的固体产物按如上右图的流程操作,请回答下列问题:
(3)检验溶液2中是否含有杂质离子的试剂是 。
(4)溶液l可加试剂X用于调节pH以除去杂质,X可选用下列试剂中的(填序号) 。
a.NaOH b.NH3·H2O C.CuO d.CuSO4 e.Cu2(OH)2CO3
(5)反应②是向溶液2中通入一定量的SO2,加热一段时间后生成CuCl白色沉淀。写出制
备CuCl的离子方程式
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com