
| A、0.2 mol |
| B、0.5 mol |
| C、2 mol |
| D、5 mol |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:

| A、盐桥的作用是让电子通过,以构成闭合回路 |
| B、总反应为:2H++Zn═H2+Zn2+且△H<0 |
| C、随着反应进行,右烧杯中溶液pH变小 |
| D、随着反应进行,左烧杯溶液中的SO42-向右烧杯迁移 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氧化铝熔点很高,可制造用于熔融烧碱的坩埚 |
| B、炭具有还原性,一定条件下能将二氧化硅还原为硅 |
| C、常温下二氧化硅不与强酸反应,可用石英容器盛放氢氟酸 |
| D、SO2具有漂白性,可用作熏蒸粉丝使其增白 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、锌作负极 |
| B、铜片上有气泡产生 |
| C、将电能转化为化学能 |
| D、锌片的电极反应式为:Zn-2e-=Zn2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| c(H+) |
| c(OH-) |
| A、①④ | B、①③ | C、②③ | D、①④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、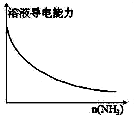 向一定量的CH3COOH溶液中通入NH3至过量 |
B、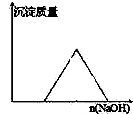 向等物质的量的HCl和AlCl3溶液中滴入NaOH溶液至过量 |
C、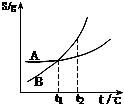 表示A、B两物质的溶解度随温度变化情况,将t1℃时A、B饱和溶液升温至t2℃时,溶质的质量分数B=A |
D、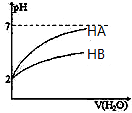 表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则同浓度的NaA溶液的pH大于NaB溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向硫酸亚铁溶液中通入H2S气体:Fe2++H2S→FeS↓+2H+ |
| B、碳酸钙溶于醋酸:CaCO3+2CH3COOH→Ca2++2CH3COO-+CO2↑+H2O |
| C、少量氢氧化钙溶液与碳酸氢钠溶液混合:OH-+HCO3-→H2O+CO32- |
| D、稀氯化铵溶液和澄清石灰水混合:NH4++OH-→NH3?H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com