
【题目】关于2molSO2的叙述中,正确的是( )
A.体积为44.8 LB.含有4mol氧原子
C.分子数为6.02×1023D.摩尔质量为128 g
 优生乐园系列答案
优生乐园系列答案 新编小学单元自测题系列答案
新编小学单元自测题系列答案科目:高中化学 来源: 题型:
【题目】将3.48gFe3O4完全溶解于100mL1mol/L硫酸中,然后加入K2Cr2O7溶液25mL,恰好使溶液中Fe2+全部转化为Fe3+ , Cr2O72﹣全部还原为Cr3+ , 则K2Cr2O7溶液的物质的量浓度为( )
A.0.05mol/L
B.0.1mol/L
C.0.2mol/L
D.0.3mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于制取蒸馏水的实验装置与操作的说法中,不正确的是( )
A.可用过滤的方法制取蒸馏水
B.冷凝器中的水流方向是从下口进入,上口排出
C.实验中需要在蒸馏烧瓶中加入几片碎瓷片,防止出现暴沸现象
D.给蒸馏烧瓶加热时必须垫石棉网
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业生产尿素的原理是以NH3和CO2为原料合成尿素[CO(NH2)2],反应的化学方程式为:2NH3 (g)+CO2 (gCO(NH2)2 (l)+H2O (l),该反应的平衡常数和温度关系如下:
T/℃ | 165 | 175 | 185 | 195 |
K | 111.9 | 74.1 | 50.6 | 34.8 |
①△H(填“>”、“<”或“=”)0.
②在一定温度和压强下,若原料气中的NH3和CO2的物质的量之比(氨碳比) ![]() ,如图是氨碳比(x)与CO2平衡转化率(α%)的关系.α随着x增大而增大的原因是 .
,如图是氨碳比(x)与CO2平衡转化率(α%)的关系.α随着x增大而增大的原因是 .
③图中的B点处,NH3的平衡转化率 为 . 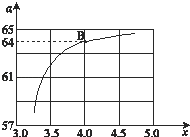
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能正确表示下列反应的离子方程式是( )
A. 将Cl2通入氯化亚铁溶液:Fe2++Cl2![]() Fe3++2Cl-
Fe3++2Cl-
B. 氯气通入水中:Cl2+H2O![]() 2H++Cl-+ClO-
2H++Cl-+ClO-
C. FeCl3溶液中通入过量的氨水: Fe3++3OH-![]() Fe(OH)3↓
Fe(OH)3↓
D. Cl2通入烧碱溶液中:Cl2+2OH-![]() Cl-+ClO-+H2O
Cl-+ClO-+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(14分)H2S和SO2会对环境和人体健康带来极大的危害,工业上采取多种方法减少这些有害气体的排放,回答下列方法中的问题.
Ⅰ.H2S的除去
方法1:生物脱H2S的原理为:
H2S+Fe2(SO4)3═S↓+2FeSO4+H2SO4
4FeSO4+O2+2H2SO4 ![]() 2Fe2(SO4)3+2H2O
2Fe2(SO4)3+2H2O
(1)硫杆菌存在时,FeSO4被氧化的速率是无菌时的5×105倍,该菌的作用是 .
(2)由图1和图2判断使用硫杆菌的最佳条件为 . 若反应温度过高,反应速率下降,其原因是 . 
(3)方法2:在一定条件下,用H2O2氧化H2S
随着参加反应的n(H2O2)/n(H2S)变化,氧化产物不同.当n(H2O2)/n(H2S)=4时,氧化产物的分子式为 .
(4)Ⅱ.SO2的除去
方法1(双碱法):用NaOH吸收SO2 , 并用CaO使NaOH再生
NaOH溶液 ![]() Na2SO3溶液
Na2SO3溶液
写出过程①的离子方程式:;CaO在水中存在如下转化:
CaO(s)+H2O (l)═Ca(OH)2(s)Ca2+(aq)+2OH﹣(aq)
从平衡移动的角度,简述过程②NaOH再生的原理 .
(5)方法2:用氨水除去SO2
已知25℃,NH3H2O的Kb=1.8×10﹣5 , H2SO3的Ka1=1.3×10﹣2 , Ka2=6.2×10﹣8 . 若氨水的浓度为2.0molL﹣1 , 溶液中的c(OH﹣)=molL﹣1 . 将SO2通入该氨水中,当c(OH﹣)降至1.0×10﹣7 molL﹣1时,溶液中的c(SO32﹣)/c(HSO3﹣)= .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图1为实验室制取氨气的实验装置。
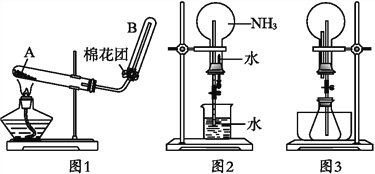
(1)写出A中所发生反应的化学方程式_______________________。要收集干燥的氨气,可以用____________________作干燥剂。
(2)在收集氨气时试管口棉花的作用是___________。
(3)一位学生用制得的氨气,按图2装置进行喷泉实验,烧瓶已充满干燥的氨气,引发喷泉实验的操作是___________。
(4)另一学生积极思考产生喷泉的其他方法,设计了图3装置。首先在锥形瓶中分别加入足量的下列物质,反应后能产生喷泉的是___________。
A.CaCO3粉末和浓盐酸 B.NH4HCO3溶液与稀NaOH溶液
C.HCl和AgNO3溶液 D.HCl和无色酚酞溶液
该同学又向锥形瓶中加入酒精,水槽中加入冷水后,再加入足量的下列物质,结果也产生了喷泉。水槽中加入的物质可以是___。
A.硝酸铵 B.食盐 C.浓硫酸 D.硫酸铜
(5)检验氨气已充满试管B的方法是______________.
(6)如制得标准状况下的氨气2.24L,则反应中至少需要熟石灰______g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com