
分析 (1)Zn与稀硫酸反应生成硫酸锌和氢气;
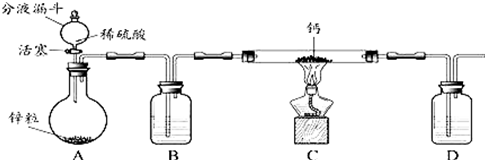
(2)由实验装置可知,因Ca与水反应,则B、D中均利用浓硫酸吸收水,在C中发生Ca与氢气的反应;
(3)氢气不纯,加热易发生爆炸;
(4)Ca与氢气发生反应生成氢化钙;
【实验反思】利用氢气的质量计算氢化钙的质量,从而判断是否纯净.
解答 解:(1)实验室用稀硫酸和锌粒反应制取氢气,化学方程式Zn+H2SO4=ZnSO4+H2↑,故答案为:Zn+H2SO4=ZnSO4+H2↑;
(2)用氢气与钙加热制得氢化钙,因钙遇水立即发生剧烈反应生成氢氧化钙和氢气,并放出大量的热,所以与钙反应的氢气必须是干燥的氢气,故制取的氢气需通过浓硫酸进行干燥,因生成的氢化钙遇水反应生成氢氧化钙和氢气,因此为防止防止空气中的水蒸汽进入C中,需在D中装有浓硫酸进行干燥,
故答案为:浓硫酸;干燥氢气;防止空气中的水蒸汽进入C中;
(3)点燃不纯的氢气可能会发生爆炸,因此氢气与钙加热反应前需将装置内的空气排出,故实验时先打开A中活塞,一段时间后,再点燃C中酒精灯,以排除装置内的空气,防止加热时产生爆炸,
故答案为:排除装置内的空气,防止加热时产生爆炸;
(4)钙和氢气反应在加热的条件下生成氢化钙,反应的方程式为H2+Ca$\frac{\underline{\;\;△\;\;}}{\;}$CaH2,故答案为:H2+Ca$\frac{\underline{\;\;△\;\;}}{\;}$CaH2;
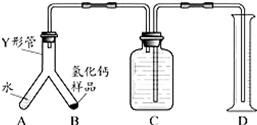
【实验反思】根据图示,要验证氢化钙是否纯净,可取一定量氢化钙样品与水完全反应,根据生成氢气的质量求出氢化钙的质量,然后与样品质量比较,
故答案为:根据实验得出的氢气的体积,可计算出氢气的质量,再根据氢化钙与水反应的化学方程式,计算出所需氢化钙的质量,并与氢化钙样品质量作对比.
点评 本题考查物质的制备实验方案,为高频考点,把握物质的性质、发生的反应、实验装置的作用及实验技能为解答的关键,侧重分析与实验能力的考查,综合性较强,题目难度不大.


 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案科目:高中化学 来源:2017届江苏省高三上第一次测试化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值。下列叙述正确的是
A.标准状况下,0.56 L丙烷中含有共价键的数目为0.2NA
B.常温常压下,6.4 g氧气和臭氧中含有的原子总数为0.4NA
C.5.6 g铁与一定量硝酸恰好反应,转移的电子数目一定为0.3NA
D.常温下,2 L 0.1 mol·L-1Na2CO3溶液中,含有的CO32-离子数为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
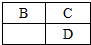 A、B、C、D、E均为短周期主族元素,B、C、D在周期表中的位置关系如图所示,A是短周期中原子半径最小的元素,A、B、C三种元素的原子序数之和等于D元素的原子序数,E是短周期中最活泼的金属元素.下列说法错误的是( )
A、B、C、D、E均为短周期主族元素,B、C、D在周期表中的位置关系如图所示,A是短周期中原子半径最小的元素,A、B、C三种元素的原子序数之和等于D元素的原子序数,E是短周期中最活泼的金属元素.下列说法错误的是( )| A. | 氢化物的稳定性:B>D | B. | 简单离子的半径大小:D>E>C | ||
| C. | 简单阴离子的还原性:C<D | D. | A、B、C可形成离子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 2 | C | O | F | |||||
| 3 | Na | Mg | P | S | Cl |
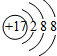 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol/L NaHCO3溶液与0.1mol/L NaOH溶液等体积混合,所得溶液中: c(Na+)>c(CO32-)>c(HCO3-)>c(OH-) | |
| B. | 20mL 0.1mol/L CH3COONa溶液与10mL 0.1mol/L HCl溶液混合后溶液呈酸性,所得溶液中:c(CH3COO-)>c(Cl-)>c(CH3COOH)>c(H+) | |
| C. | 室温下,pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中:c(Cl-)+c(H+)>c(NH4+)+c(OH-) | |
| D. | 已知某温度下,Ksp(AgCl)=1×10-10,Ksp(Ag2CrO4)=1×10-12.若将0.001mol•L-1AgNO3溶液滴入浓度均为0.001 mol•L-1的KCl和K2CrO4混合溶液中,则先产生Ag2CrO4沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Y的气态氢化物的沸点在同主族中最高,所以其气态氢化物最稳定 | |
| B. | Y、W形成的化合物与Y、Z形成的化合物中所含化学键相同 | |
| C. | 简单离子半径:Z>Y | |
| D. | 单质的氧化性:Y>W |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO3 | B. | HCl | C. | FeCl2 | D. | Na2O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 将少量碳酸钠溶液滴加到盐酸中 CO32-+2H +═H2O+CO2↑ | |
| B. | 向明矾中加入氢氧化钡使硫酸根完全沉淀 Ba2++SO42-═BaSO4↓ | |
| C. | 苯酚钠中通入少量CO2 C6H5O-+CO2+H2O→C6H5OH+HCO3- | |
| D. | 向石灰乳中通入过量的SO2 OH-+SO2═HSO3- |
查看答案和解析>>
科目:高中化学 来源:2017届江苏省如皋市高三上学期质量调研一化学试卷(解析版) 题型:选择题
2016年8月,联合国开发计划署在中国的首个“氢经济示范城市”在江苏如皋落户。用吸附了H2的碳纳米管等材料制作的二次电池的原理如图所示。下列说法正确的是
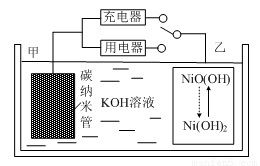
A.放电时,甲电极为正极,OH-移向乙电极
B.放电时,乙电极反应为:
NiO(OH)+H2O+e-=Ni(OH)2+OH-
C.充电时,电池的碳电极与直流电源的正极相连
D.电池总反应为H2+2NiOOH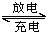 2Ni(OH)2
2Ni(OH)2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com