
某同学按图示装置进行实验:A极是铜锌合金,B极为纯铜,溶液为足量的硫酸铜溶液。通电一段时间后,若A极恰好全部溶解,此时B极质量增加5.76g,溶液质量增0.03g,则合金中Cu、Zn原子个数比为

A.4:1 B.3:1 C.2:1 D.任意比
C
【解析】
试题分析:阳极A极是铜锌合金,发生反应:Zn-2e-=Zn2+;Cu-2e-=Cu2+.阴极B极为纯铜,发生反应Cu2+ +2e-= Cu。n(Cu)= 5.76g÷64g/mol=0.09mol.由于Zn、Cu都是+2价的金属,所以阳极溶解的合金的物质的量也是0.09mol。1摩尔的Zn质量是65g,1摩尔的Cu质量是64g,相差1g. 现在溶液质量增0.03g,说明合金中含有Zn的物质的量为n(Zn)=0.03mol,n(Cu)=0.06mol.因此n(Cu): n(Zn)=0.06:0.03=2:1.即二者的个数比为2:1.选项为C。
考点:考查电解池、金属的精炼的知识


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
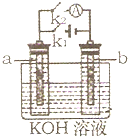 (2008?梅州一模)如图所示,a、b是多孔石墨电极,某同学按图示装置进行如下实验:断开K2,闭合K1一段时间,观察到两只玻璃管内都有气泡将电极包围,此时断开K1,闭合K2,观察到电流计A的指针有偏转.下列说法不正确的是( )
(2008?梅州一模)如图所示,a、b是多孔石墨电极,某同学按图示装置进行如下实验:断开K2,闭合K1一段时间,观察到两只玻璃管内都有气泡将电极包围,此时断开K1,闭合K2,观察到电流计A的指针有偏转.下列说法不正确的是( )查看答案和解析>>
科目:高中化学 来源: 题型:
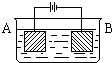 某同学按图示装置进行实验:A极是铜锌合金,B极为纯铜,溶液为足量的硫酸铜溶液.通电一段时间后,若A极恰好全部溶解,此时B极质量增加5.76g,溶液质量增0.03g,则合金中Cu、Zn原子个数比为( )
某同学按图示装置进行实验:A极是铜锌合金,B极为纯铜,溶液为足量的硫酸铜溶液.通电一段时间后,若A极恰好全部溶解,此时B极质量增加5.76g,溶液质量增0.03g,则合金中Cu、Zn原子个数比为( )查看答案和解析>>
科目:高中化学 来源: 题型:
如下图所示,a、b是多孔石墨电极,某同学按图示装置进行如下实验:t1时刻断开K2,闭合K1一段时间,观察到两只玻璃管内都有气泡将电极包围,t2时刻断开K1,闭合K2,观察到电流计A的指针有偏转。下列说法不正确的是
A、t1时刻开始断开K2,闭合K1一段时间,溶液的pH要变大
B、t2时刻断开K1,闭合K2时,b极上的电极反应式为:2H++2e—= H2↑
C、t1时刻断开K2,闭合K1时,a极上的电极反应式为:4OH—―4e—=O2↑ +2H2O
D、t2时刻断开K1,闭合K2时,OH-向b极移动
查看答案和解析>>
科目:高中化学 来源:2014届山东省威海市高二上学期期末考试化学试卷(解析版) 题型:选择题
某同学按图示装置进行实验:A极是铜锌合金,B极为纯铜,溶液为足量的硫酸铜溶液。通电一段时间后,若A极恰好全部溶解,此时B极质量增加5.76g,溶液质量增0.03g,则合金中Cu、Zn原子个数比为
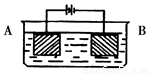
A.4:1 B.3:1 C.2:1 D.任意比
查看答案和解析>>
科目:高中化学 来源:2014届福建省高二第一次月考化学试卷(解析版) 题型:选择题
如图所示,a、b是多孔石墨电极,某同学按图示装置进行如下实验: 断开K2,闭合K1一段时间,观察到两支玻璃管内都有气泡将电极包围,此时断开K1,闭合K2,观察到电流计A的指针有偏转。下列说法不正确的是( )
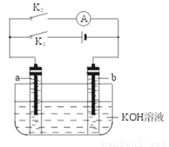
A.断开K2,闭合K1一段时间,溶液的pH变大
B.断开K1,闭合K2时,OH-向b极移动
C.断开K2,闭合K1时,a极上的电极反应式为:4OH--4e-====O2↑+2H2O
D.断开K1,闭合K2时,b极上的电极反应式为:2H+ + 2e-====H2↑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com