
| A. | Cl2与H2O反应:Cl2+H2O?2H++Clˉ+ClOˉ | |
| B. | 碳酸钡与稀硫酸反应:CO32-+2H+=CO2↑+H2O | |
| C. | CuSO4溶液与少量稀氨水反应:Cu2++2OH-=Cu(OH)2↓ | |
| D. | 铁和氯化铁溶液反应:2Fe3++Fe=3Fe2+ |
分析 A.次氯酸为弱酸,应保留化学式;
B.碳酸钡为沉淀,与硫酸反应生成硫酸钡、二氧化碳和水;
C.一水合氨为弱碱,应保留化学式;
D.二者反应生成氯化亚铁.
解答 解:A.Cl2与H2O反应,离子方程式:Cl2+H2O?H++Clˉ+HClO,故A错误;
B.碳酸钡与稀硫酸反应,离子方程式:BaCO3+SO42-+2H+=CO2↑+H2O+BaSO4,故B错误;
C.CuSO4溶液与少量稀氨水反应,离子方程式:Cu2++2NH3•H2O=Cu(OH)2↓+2NH4+,故C错误;
D.铁和氯化铁溶液反应,离子方程式:2Fe3++Fe=3Fe2+,故D正确;
故选:D.
点评 本题考查了离子方程式书写正误的判断,明确反应实质及离子方程式书写方法是解题关键,注意化学式拆分,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 1-丁醇和乙酸在浓硫酸作用下,通过酯化反应制得乙酸丁酯,反应温度为115~125℃,反应装置如图.下列对该实验的描述错误的是( )
1-丁醇和乙酸在浓硫酸作用下,通过酯化反应制得乙酸丁酯,反应温度为115~125℃,反应装置如图.下列对该实验的描述错误的是( )| A. | 不能用水浴加热 | |
| B. | 长玻璃管起冷凝回流作用 | |
| C. | 加入过量乙酸可以提高1-丁醇的转化率 | |
| D. | 提纯乙酸丁酯需要经过水、氢氧化钠溶液洗涤 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
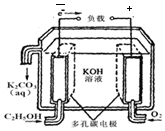
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲和丙可能都是IA族元素 | |
| B. | 若甲是非金属单质,则丙不可能是金属 | |
| C. | .乙和丁可能都为氧化物 | |
| D. | .乙和丁可能都为盐 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com