
����Ŀ��ú�������Ƶü״��������Ǻϳɾۺ���M��·��ͼ��
��֪����E��F���ܷ���������Ӧ���� ![]() +RX
+RX ![]()
![]() +HX���������գ�
+HX���������գ�
��1�����ڼ״�˵�����������ѡ����ţ���a���״��ɷ���ȡ������������ȥ�ȷ�Ӧ b���״����Բ���CH3OCH3�����ѣ�
c���״��ж��ԣ���ʹ��˫Ŀʧ�� d���״����Ҵ�����ͬϵ��
��2���״�ת��ΪE�Ļ�ѧ����ʽΪ ��
��3��C����D�ķ�Ӧ�������� д��G�Ľṹ��ʽ ��
��4��ȡ1.08gA���ʣ�ʽ��108��������������ˮ��ȫ��Ӧ������2.66g��ɫ������д��A�Ľṹ��ʽ ��
���𰸡�
��1��a
��2��2CH3OH+O2 ![]() 2HCHO+2H2O
2HCHO+2H2O
��3����ȥ��Ӧ��HCOOCH3
��4��
���������⣺һ�������£�������һ����̼��Ӧ���ɼ״����״���������EΪ��ȩ����ȩ������FΪ���ᣬ������״�����������GΪ����������״��������ᷢ��ȡ����Ӧ����һ����飬�ڴ��������£�һ�����ͺ�A��Ӧ����B��B��Ӧ����C��C��Ӧ����D������A�ķ���ʽ֪��A�к��д��ǻ����Ǽ�����ͷ��ǻ�������D�Ľṹ��ʽ֪��A�к��м��ͷ��ǻ����ӷ���ȡ����Ӧʱȡ��λ��Ϊ���ǻ����ڶ�λ������D֪��A�Ǽ�����ӣ�������Ӻ�һ����鷴Ӧ����B��2��5���������ӣ���2��5���������Ӻ����������ӳɷ�Ӧ���� ![]() ��
�� ![]() ������ȥ��Ӧ����
������ȥ��Ӧ���� ![]() ��
�� ![]() �ͱ�ϩ�����ӳɷ�Ӧ����M��M�Ľṹ��ʽΪ��
�ͱ�ϩ�����ӳɷ�Ӧ����M��M�Ľṹ��ʽΪ�� 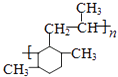 ����1��a���״��ɷ���ȡ����������Ӧ�����ܷ�����ȥ���ʴ��� b���״����Ӽ���ˮ����CH3OCH3 �� ����ȷ��c���״��ж��ԣ���ʹ��˫Ŀʧ��������ȷ��d���״����Ҵ�����һ���ǻ���������һ��CH2����������ͬϵ�����ȷ����ѡa����2���״�ת��Ϊ��ȩ�Ļ�ѧ����ʽΪ 2CH3OH+O2
����1��a���״��ɷ���ȡ����������Ӧ�����ܷ�����ȥ���ʴ��� b���״����Ӽ���ˮ����CH3OCH3 �� ����ȷ��c���״��ж��ԣ���ʹ��˫Ŀʧ��������ȷ��d���״����Ҵ�����һ���ǻ���������һ��CH2����������ͬϵ�����ȷ����ѡa����2���״�ת��Ϊ��ȩ�Ļ�ѧ����ʽΪ 2CH3OH+O2 ![]() 2HCHO+2H2O�����Դ��ǣ�2CH3OH+O2
2HCHO+2H2O�����Դ��ǣ�2CH3OH+O2 ![]() 2HCHO+2H2O����3����������ķ�����֪��C����D�ķ�Ӧ������ ��ȥ��Ӧ��GΪ���������G�Ľṹ��ʽ HCOOCH3 �� ���Դ��ǣ���ȥ��Ӧ��HCOOCH3����4��ȡ1.08g A���ʣ�ʽ��108�������ʵ���=
2HCHO+2H2O����3����������ķ�����֪��C����D�ķ�Ӧ������ ��ȥ��Ӧ��GΪ���������G�Ľṹ��ʽ HCOOCH3 �� ���Դ��ǣ���ȥ��Ӧ��HCOOCH3����4��ȡ1.08g A���ʣ�ʽ��108�������ʵ���= ![]() ��������������ˮ��ȫ��Ӧ������2.66g��ɫ����������̼ԭ���غ�֪����ɫ���������ʵ�����0.01mol�����ɫ������Ħ��������266g/mol��A��ʽ���Ͱ�ɫ������ʽ�����158������ԭ��ȡ�����ǻ����ڶ�λ������A�Ľṹ��ʽΪ��
��������������ˮ��ȫ��Ӧ������2.66g��ɫ����������̼ԭ���غ�֪����ɫ���������ʵ�����0.01mol�����ɫ������Ħ��������266g/mol��A��ʽ���Ͱ�ɫ������ʽ�����158������ԭ��ȡ�����ǻ����ڶ�λ������A�Ľṹ��ʽΪ�� 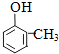 �����Դ��ǣ�
�����Դ��ǣ�  ��
��


 �γ̴����Ծ�����100��ϵ�д�
�γ̴����Ծ�����100��ϵ�д� �¾�����ĩ���100��ϵ�д�
�¾�����ĩ���100��ϵ�д� ȫ�ܴ���100��ϵ�д�
ȫ�ܴ���100��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������������ڵ���ʵ����� ��
A. ���� B. NaCl C. ���� D. SO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�������£�ʵ����������ͼ��ʾװ�ã�ͨ�����ѹ���� Ksp��AgCl��������һ��ʱ������缫��������������˵��������ǣ� �� 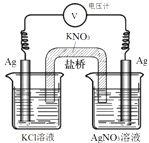
A.��װ�ù���ʱ��ѧ��ת��Ϊ����
B.����е����缫������
C.�ܷ�ӦΪAg+��aq��+Cl����aq��AgCl��s��
D.�����е�K+���ҳط����ƶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£�����˵����ȷ���ǣ� ��
A.�ֱ��к�pH��ͬ�ĵ����������ʹ�����Һ�����ĵ�����NaOH
B.pH=a��CH3COOH��Һ��ˮϡ��10n����pH=a+n
C.pH��ȵ�CH3COONa��NaOH��Һ�У�ˮ�ĵ���̶���ͬ
D.Na2CO3��Һ�У�c��OH����=c��H+��+c��HCO ![]() ��+2c��H2CO3��
��+2c��H2CO3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij���к�θ���ҩ����Ҫ�ɷֵĻ�ѧʽAl2Mg6(OH)16CO3��4H2O��1mol
Al2Mg6(OH)16CO3��4H2O�У���ԭ�ӵ����ʵ���Ϊ�� ��
A. 16mo1B. 19molC. 20molD. 23mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ʢ��KI��Һ���Թ��У�����������ˮ��ַ�Ӧ���ټ����Ȼ�̼�����ú�۲쵽��������(����)
A.�ϲ��Ϻ�ɫ���²�ӽ���ɫ
B.���ȡ������Ϻ�ɫ
C.���ȡ�������ɫ
D.�ϲ�ӽ���ɫ���²��Ϻ�ɫ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ʵ���У�������������ȷ���ǣ� ��
A. ��������ƿ��ʢԼ1/2���������ˮ�������뼸����ʯ
B. ���¶ȼ�ˮ�����������ˮ��
C. ��ˮ���������¿��룬�Ͽڳ�
D. �ռ�����ˮʱ��Ӧ��ȥ��ʼ����IJ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijѧϰС�鰴����ʵ������̽�������е⺬���IJⶨ�͵����ȡ��ʵ��һ���⺬���IJⶨ
ȡ0.0100mol/L��AgNO3����Һ�ζ�100.00mL������ȡԭҺ���õ��Ƶζ����ⶨ��ĺ�������õĵ綯�ƣ�E����ӳ��Һ��C��I���� �仯�������ִ��������Ƴ��ζ����������߱仯���£�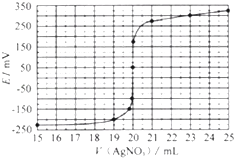
ʵ����������ȡ
��ȡ������ȡԭҺ���ס�������ʵ�鷽�����£�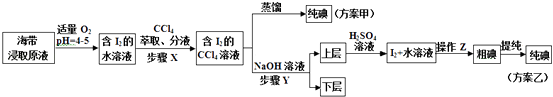
��֪��3I2+6NaOH��5NaI+NaIO3+3H2O
��ش�
��1��ʵ��һ�е��������ƣ�����A �� ����B��ʵ����в���Z������ ��
��2�����ݱ������߿�֪���˴εζ��յ�ʱ��ȥAgNO3��Һ�����Ϊml������ú����е�İٷֺ���Ϊ ��
��3������X�У���ȡ���Һ©���ڹ۲쵽�������� ��
��4�������йز���Y��˵������ȷ����A��Ӧ����NaOH��Һ��Ũ�Ⱥ���� B������ת�������ӽ���ˮ��
C����Ҫ�dz�ȥ������ȡԭҺ�е��л����� D��NaOH��Һ�������Ҵ�����
�������У��ϲ�Һ������ᷢ����Ӧ�����ӷ���ʽ�� ��
��5������������������������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����Ѿ��ﵽƽ��ķ�Ӧ��2SO2+O2 ![]() 2SO3��Сѹǿʱ�Է�Ӧ������Ӱ���� �� ��
2SO3��Сѹǿʱ�Է�Ӧ������Ӱ���� �� ��
A.�淴Ӧ������������Ӧ���ʼ�С��ƽ�����淴Ӧ�����ƶ�
B.�淴Ӧ���ʼ�С������Ӧ��������ƽ��������Ӧ�����ƶ�
C.���������ʶ���С��ƽ�����淴Ӧ�����ƶ�
D.���������ʶ�����ƽ��������Ӧ�����ƶ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com