
【题目】在一定温度下,10mL0.40mol/L H2O2发生催化分解。不同时刻测定生成O2的体积(已折算为标准状况)如下表。
t/min | 0 | 2 | 4 | 6 | 8 | 10 |
V(O2)/mL | 0.0 | 9.9 | 17.2 | 22.4 | 26.5 | 29.9 |
下列叙述不正确的是(溶液体积变化忽略不计)
A.0~6min的平均反应速率:v(H2O2)![]()
![]() mol/(L·min)
mol/(L·min)
B.6~10min的平均反应速率:v(H2O2)<![]() mol/(L·min)
mol/(L·min)
C.反应至6min时,c(H2O2)=0.3mol/L
D.反应至6min时,H2O2分解了50%
 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案科目:高中化学 来源: 题型:
【题目】有NO、CO2、N2O4三种气体,它们分别都含有0.5mol氧原子,则三种气体的物质的量之比为( )
A.1∶1∶2B.1∶1∶1C.4∶2∶1D.1∶2∶4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)如图装置(Ⅰ)为以NaOH溶液为电解质溶液的氢氧燃料电池。装置(Ⅰ)中a和b为气体进口,其中a口进入的是(填名称)____,写出电极②发生反应的电极反应式______。
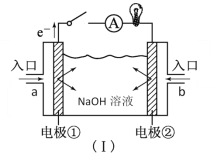
(2)将质量相等的铁片和铜片用导线相连浸入500mL硫酸铜溶液中构成如图的装置:(以下均假设反应过程中溶液体积不变)。
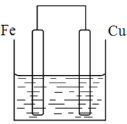
①铁片上的电极反应式为_____。
②溶液中的铜离子移向____(填铁电极或铜电极)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于决定物质体积的因素的说法中不正确的是( )
A.物质的体积取决于粒子数目、粒子大小和粒子间距
B.相同条件下,粒子数相同的任何气体都具有相同体积
C.同温同压下,1 mol任何物质所占的体积都相同
D.等质量的氢气,压强越小、温度越高,其体积越大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了检验淀粉水解的产物,设计如下实验方案:
![]()
请回答下列问题:
(1)试剂1为20%的H2SO4溶液,其作用是____________________________________。
(2)试剂2为______________,其作用是__________________,使检验水解产物的实验得以顺利进行。
(3)反应①的化学方程式为__________________________________________________。
(4)为检验淀粉液是否已完全水解,取少量水解液于试管中,加入碘水,则证明淀粉未完全水解的现象是__________。
(5)如果实验过程中没有加入试剂2而直接加入试剂3,能否实现实验目的________(填”能”或”否”),若不能,其原因是_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在体积固定的密闭容器中加入2mol A和1mol B,发生反应:2A(g)+B(g)![]() 3C(g)+D(g),达到平衡时C的浓度为a mol/L.若维持容器体积和温度不变,按下列四种配比作为起始物质,达到平衡后,C的浓度仍为a mol/L的是
3C(g)+D(g),达到平衡时C的浓度为a mol/L.若维持容器体积和温度不变,按下列四种配比作为起始物质,达到平衡后,C的浓度仍为a mol/L的是
A. 4 mol A+2 mol B B. 2 mol A+1 mol B+1 mol He
C. 3 mol C+2 mol D D. 2 mol A+1 mol D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,将气体X和气体Y各0.16mol充入10L恒容密闭容器中,发生反应:X(g)+Y(g) ![]() 2Z(g)△H<0,一段时间后达到平衡,反应过程中测定的数据如下表:下列说法不正确的是
2Z(g)△H<0,一段时间后达到平衡,反应过程中测定的数据如下表:下列说法不正确的是
t/min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
A. 反应前2min的平均速率v(Z)=2.0×10-3 mol·L-1·min-1
B. 其他条件不变,降低温度,反应达到新平衡前:v(逆)<v(正)
C. 该温度下此反应的平衡常数:K=1.44
D. 保持其他条件不变,起始时向容器充入0.32 mol气体X和0.32 mol气体Y,到达平衡时,c(Z)=0.024 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某有机物X的结构简式为 ,下列有关叙述不正确的是 ( )
,下列有关叙述不正确的是 ( )
A. 1 mol X分别与足量的Na、NaOH溶液、NaHCO3溶液反应,消耗这三种物质的物质的量分别为3 mol、4 mol、1 mol
B. X在一定条件下能与FeCl3溶液发生显色反应
C. X在一定条件下能发生消去反应和酯化反应
D. X的化学式为C10H10O6
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com