
分析 (1)金属氧化物和酸反应生成盐和水;
(2)氯化铁和NaOH发生复分解反应生成红褐色沉淀氢氧化铁;
(3)氢氧化铁胶体呈红褐色;氢氧化铁胶体具有聚沉性质,遇到电解质溶液发生聚沉,氢氧化铁沉淀溶于稀硫酸.
解答 解:(1)氧化铁属于碱性氧化物,和酸反应生成铁盐和水,反应方程式为Fe2O3+6HCl=2FeCl3+3H2O,
故答案为:Fe2O3+6HCl=2FeCl3+3H2O;
(2)氯化铁和NaOH发生复分解反应生成红褐色沉淀氢氧化铁,同时生成NaCl,离子方程式为Fe3++3OH-=Fe(OH)3↓,
故答案为:Fe3++3OH-=Fe(OH)3↓;
(3)将蒸馏水加热至沸腾后,向烧杯中加入几滴FeCl3溶液,继续煮沸至出现红褐色,得到氢氧化铁胶体,在向所得Fe(OH)3胶体中逐滴加入稀硫酸的现象是先产生红褐色沉淀,后又溶解为黄色溶液,
故答案为:红褐;先产生红褐色沉淀,后又溶解为黄色溶液.
点评 本题以铁元素为载体考查化学方程式和离子方程式的书写、胶体的制取和性质等知识点,侧重考查基本理论,知道胶体性质的特殊性,难点是离子方程式的书写,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题

| 实验编号 | T(℃) | n(CO)/n(H2) | p(MPa) |
| 1 | 150 | $\frac{1}{3}$ | 0.1 |
| 2 | a | $\frac{1}{3}$ | 5 |
| 3 | 350 | b | 5 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
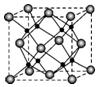 M、R、X、Y为原子序数依次增大的短周期主族元素,Z是一种过渡元素.M基态原子L层中p轨道电子数是s电子的2倍,R是同周期元素中最活泼的金属元素,X和M形成的一种化合物是引起酸雨的主要大气污染物,Z的基态原子4s和3d轨道半充满.请回答下列问题:
M、R、X、Y为原子序数依次增大的短周期主族元素,Z是一种过渡元素.M基态原子L层中p轨道电子数是s电子的2倍,R是同周期元素中最活泼的金属元素,X和M形成的一种化合物是引起酸雨的主要大气污染物,Z的基态原子4s和3d轨道半充满.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅥⅠA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ | ⑪ | ⑫ |
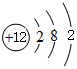 ,⑤
,⑤ .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分液时,分液漏斗的上层液体应由上口到出 | |
| B. | 向某溶液中加入稀盐酸,产生的气体通入澄清石灰水,石灰水变浑浊,该溶液一定是碳酸盐溶液 | |
| C. | 配置0.1000mol•L-1氢氧化钠溶液时,将液体转移到容量瓶中需用玻璃棒引流 | |
| D. | 锥形瓶用作反应容器时可以加热 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
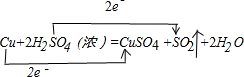 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com