
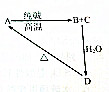
 几种含硅物质的相互转化关系如图所示,其中物质A是一种高熔点化合物,不溶于稀硫酸、硝酸,却溶于氢氟酸;C是一种气体;D是白色胶状沉淀.
几种含硅物质的相互转化关系如图所示,其中物质A是一种高熔点化合物,不溶于稀硫酸、硝酸,却溶于氢氟酸;C是一种气体;D是白色胶状沉淀.
| ||
| ||
| ||
| ||


科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A | B | C | D |  | |
| 甲 | AlCl3 | NaOH | NaAlO2 | AlCl3 | |
| 乙 | NaOH | AlCl3 | HCl | NH3?H2O |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
 (1)如图是某溶液稀释过程中,溶液的物质的量浓度随溶液体积的变化曲线图,根据图中数据分析得出a 值等于
(1)如图是某溶液稀释过程中,溶液的物质的量浓度随溶液体积的变化曲线图,根据图中数据分析得出a 值等于查看答案和解析>>
科目:高中化学 来源: 题型:

| A、DE段方程式为NH4++OH-=NH3?H2O |
| B、原硝酸溶液中含硝酸的物质的量为0.47 mol |
| C、C点对应的溶液体积为40 mL |
| D、混合物中铝粉与铁粉的物质的量之比为5:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A | B | C | D |
| ①能使溴的四氯化碳溶液褪色 ②比例模型为 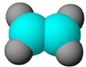 ③组成该有机物的两元素质量比为6:1 | ①由C、H两种元素组成 ②球棍模型为  | ①由C、H、O三种元素组成 ②能与Na反应,但不能与NaOH溶液反应 ③能与D反应生成相对分子质量为130的酯F | ①由C、H、O三种元素组成 ②球棍模型为 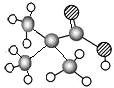 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 某学习小组用如图装置测定铝美合金中铝的质量分数和铝的相对原子质量.
某学习小组用如图装置测定铝美合金中铝的质量分数和铝的相对原子质量.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、吸滤完毕或中途需停止吸滤时,应先关闭水龙头,然后拆下连接抽气泵和吸滤瓶的橡皮管 |
| B、在层析实验操作中,应沿试管壁小心地将展开剂慢慢倒入试管底部 |
| C、要从硝酸钾和食盐(少量)的混合物中,分离出较纯净的硝酸钾,应把它们制成热饱和溶液,降温后再过滤 |
| D、由于碘在酒精中的溶解度大,故可用酒精把碘水中的碘萃取出来 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com