
【题目】惕格酸(C5H8O2,分子中有两个甲基)可用于制备香精,由烃A生成惕格酸的反应如下:
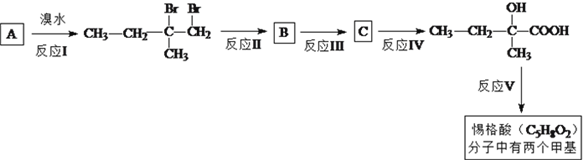
完成下列填空:
(1)写出反应类型。反应I:_____________反应、反应V:_______________反应。
(2)写出反应II试剂和反应条件:________________________________________。
(3)写出反应III的化学反应方程式:___________________________________________。
(4)如何检验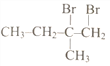 中的溴元素?____________________________________。
中的溴元素?____________________________________。
(5)写出符合下列条件的惕格酸的同分异构体的结构简式:_________________________。条件:与惕格酸含相同官能团,且也有两个甲基。 溴代甲基环己烷(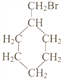 也可表示为
也可表示为![]() )可通过反应合成1-甲基环己烯(
)可通过反应合成1-甲基环己烯(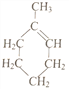 也可表示为
也可表示为![]() )
)
(6)设计一条以溴代甲基环己烷为原料合成1-甲基环己烯的合成路线。(合成路线常用的表示方式为: ![]() )________________
)________________
【答案】 加成 消除 NaOH水溶液,加热 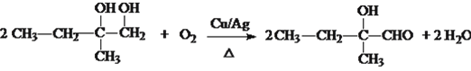 取样,向其中加入NaOH溶液,加热;再加稀硝酸至溶液显酸性,加AgNO3溶液产生淡黄色沉淀,则该有机物中含溴元素,反之则无
取样,向其中加入NaOH溶液,加热;再加稀硝酸至溶液显酸性,加AgNO3溶液产生淡黄色沉淀,则该有机物中含溴元素,反之则无 ![]()

【解析】(1)由下一种物质可推出反应I为加成反应,反应V为消除反应。
(2)反应II为卤代烃的水解反应所以条件为NaOH水溶液,加热
(3)反应III为醇的催化氧化,方程式为: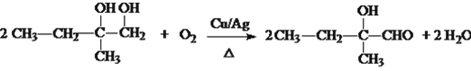
(4)因为卤代烃中的卤原子电离不出来,要想检验必须先让其水解,生成卤化氢再检验。方法为:取样,向其中加入NaOH溶液,加热;再加稀硝酸至溶液显酸性,加AgNO3溶液产生淡黄色沉淀,则该有机物中含溴元素,反之则无。
(5)惕格酸中含碳碳双键和羧基且有两个甲基,符合条件的同分异构体为:![]()
(6)有卤代烃到烯烃可以经过消去-加成-消去的方式得到,过程为:



 全能测控期末小状元系列答案
全能测控期末小状元系列答案科目:高中化学 来源: 题型:
【题目】某溶液中含有X-、Y2-、Z2-三种常见的无机离子。如下图所示,发生了一系列化学反应。第④步反应生成的白色沉淀中含Y2-.

(1)判断X-、Y2-、Z2-分别为________、________、________(写离子符号)。
(2)写出④、⑤步反应的离子方程式。
④______________________________________________________;
⑤______________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)下列物质中①NaCl晶体 ②液态S03 ③醋酸 ④汞 ⑤BaS04固体 ⑥酒精 ⑦熔化的KN03 属于电解质的是(填序号)_________________________
(2)质量为3.9 g的Na2X中含有Na+的物质的量为0.1mol,则Na2X的摩尔质量为______,
(3)某气体对氧气的相对密度为2,则此气体的相对分子质量为______
(4)3.01×1022个S2-的物质的量为________,质量为________,含有质子的物质的量为______,含有电子的物质的量为________。
(5)某地酸雨经检验,除含氢离子外,还有如下离子:c(Na+)=1.4×10-3 mol·L-1 ,c(Cl-) =3.5×10-3 mol·L-1 ,c(NH) =2.3×10-3 mol·L-1 , c(SO![]() ) =1.5×10-3 mol·L-1。则该溶液中氢离子的浓度为_____________ mol·L-1。
) =1.5×10-3 mol·L-1。则该溶液中氢离子的浓度为_____________ mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于铜锌原电池(稀硫酸作电解质溶液)的叙述错误的是( )
A.电子由正极通过导线流向负极
B.负极反应式为:Zn﹣2e﹣=Zn2+
C.正极产生1molH2电池转移2mol电子
D.可以用碳棒代替铜片作为正极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SO2的催化氧化: ![]() ,是工业制取硫酸的关键步骤之一。在容积都为2L的
,是工业制取硫酸的关键步骤之一。在容积都为2L的![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 五个密闭容器中,投入相同的催化剂,并均充入1mol O2和2mol SO2,控制不同的反应温度进行反应,反应进行到5min时,测得相关数据如下表:
五个密闭容器中,投入相同的催化剂,并均充入1mol O2和2mol SO2,控制不同的反应温度进行反应,反应进行到5min时,测得相关数据如下表:
容器温度 物质的量(mol) |
400℃ |
425℃ |
450℃ |
475℃ |
500℃ |
O2 | 0.8 | 0.6 | 0.3 | 0.5 | 0.7 |
SO3 | 0.4 | 0.8 | 1.4 | 1.0 | 0.6 |
(1)计算5min内![]() 容器中SO2的平均反应速率___________________________。
容器中SO2的平均反应速率___________________________。
(2)反应进行到5min时, ![]() 容器中的反应是否达到平衡状态?_______(填“已达”、“未达”)理由是:_________________________________________________
容器中的反应是否达到平衡状态?_______(填“已达”、“未达”)理由是:_________________________________________________
(3)在右图中画出![]() 容器中SO3物质的量随时间的变化曲线。____________
容器中SO3物质的量随时间的变化曲线。____________
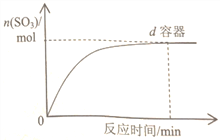
(4)工业上常用Na2SO3溶液来吸收SO2,该反应的离子方程式是:______________________。
(5)Na2SO3和NaHSO3混合溶液的pH随Na2SO3和NaHSO3比例的不同而不同,数据如下:
序号 | ① | ② | ③ |
| 91:9 | 1:1 | 1:91 |
pH | 8.2 | 7.2 | 6.2 |
表中第________组(填写序号)数据,可判断NaHSO3溶液显_______性(填“酸”或“碱”)。
(6)NaHSO3既能和强酸反应也能和强碱溶液反应。用平衡移动原理说明NaHSO3能和强碱溶液反应的原因:_________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中科大陈乾旺教授等人发明![]() 合成金刚石的新方法,化学原理为:①
合成金刚石的新方法,化学原理为:①![]() (未配平)该方法比1955年人工首次制得金刚石的旧方法容易得多。②
(未配平)该方法比1955年人工首次制得金刚石的旧方法容易得多。②![]() 。以下表述正确的是( )
。以下表述正确的是( )
A. 反应①中既有旧化学键的断裂又有新化学键的形成
B. 新方法利用的是物理变化,旧方法利用的是化学变化
C. 在反应①中每生成![]() 金刚石需要消耗
金刚石需要消耗![]() 金属钠
金属钠
D. 反应①和反应②中所得的金刚石都是还原产物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】借助下表提供的信息,实验室制备乙酸丁酯所采取的措施正确的是
物质 | 乙酸 | 1-丁醇 | 乙酸丁酯 |
沸点 | 117.9℃ | 117.2℃ | 126.3℃ |
A. 采用水浴加热 B. 使用浓硫酸做催化剂
C. 用NaOH(aq)洗涤产物后分液 D. 边制备边蒸出乙酸丁酯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苄丙酮香豆素(H)常用于防治血觑栓栓塞性疾病。其合成路线如图所示(部分反应条件略去。)
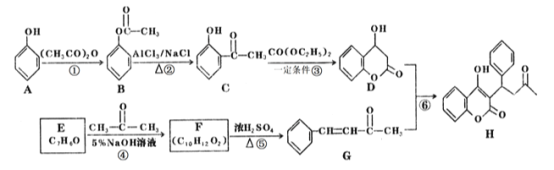
(1)E的名称是_________,D中含氧官能团的名称是_________。
(2)反应①的反应类型是__________,反应⑤的反应类型是_________。
(3)1mol H与H2加成,最多可消耗_____mol H2。
(4)反应③的化学方程式为____________________________________。
(5)C的同分异构体中满足下列条件的有______种,其中核磁共振氢谱有4组峰且峰面积之比为1:2:2:3的结构简式为__________(写一种即可)。
①不能和FeCl3溶液发生显色反应 ②1mol该有机物能与2molNaOH恰好完全反应
(6)参照苄丙酮香豆素的合成路线,设计一种以E和乙醛为原料制备![]() 的合成路线________。
的合成路线________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com