
【题目】在密闭容器中充入4mol SO2和3mol O2 一定条件下建立平衡2SO2(g)+O2(g)═2SO3(g)△H=﹣Q KJ/mol,测得SO2的转化率为90%,则在此条件下,反应放出的热量为( )
A.1.8Q KJ
B.2Q KJ
C.Q KJ
D.0.9Q KJ
 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案科目:高中化学 来源: 题型:
【题目】硫酸是一种重要的化工产品,硫酸的消耗量常被视为一个国家工业发展水平的一种标志.目前的重要生产方法是“接触法”,有关接触氧化反应2SO2+O2 ![]() 2SO3 , 的说法不正确的是( )
2SO3 , 的说法不正确的是( )
A.该反应为可逆反应,故在一定条件下二氧化硫和氧气不可能全部转化为三氧化硫
B.达到平衡后,反应就停止了,故此时正、逆反应速率相等且均为零
C.一定条件下,向某密闭容器中加入2molSO2和1molO2 , 则从反应开始到达到平衡的过程中,正反应速率不断减小,逆反应速率不断增大,某一时刻,正、逆反应速率相等
D.在利用上述反应生产三氧化硫时,要同时考虑反应所能达到的限度和化学反应速率两方面的问题
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙硼烷(B2H6)碱性燃料电池是一种新型电池,具有能量转化效率高、无污染等优点,其结构示意图如图所示.下列说法中不正确的是( ) 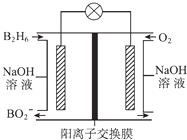
A.正极的电极反应式为O2+4e﹣+2H2O═4OH﹣
B.电池工作时,Na+通过阳离子交换膜向右移动
C.转移6mol电子理论上消耗乙硼烷的质量为14g
D.消耗1mol B2H6时负极参与反应的n(OH﹣)为12mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】C、H、N三种化学元素的质量分数共占人体化学成分的73%左右,而这三种元素在组成岩石圈的化学成分中,质量分数不到1%,这个事实说明
A. 生物界和非生物界具有统一性
B. 生物界与非生物界本质是不同的
C. 生物界没有一种元素是生物所特有的,生物和非生物从本质上看是相同的
D. 生物界和非生物界存在着本质的区别,两者还具有差异性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,反应X(g)+3Y(g)2Z(g)△H=﹣92.4 kJ/mol,X的平衡转化率(α)与体系总压强(P)的关系如图所示.下列说法正确的是( ) 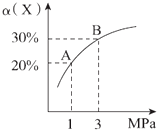
A.图中A,B两点,达到相同的平衡体系
B.上述反应在达到平衡后,增大压强,H2的转化率提高
C.升高温度,平衡向逆反应方向移动,说明逆反应速率增大,正反应速率减小
D.将1.0 mol X、3.0 mol Y,置于1 L密闭容器中发生反应,放出的热量为92.4 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述或操作中正确的是( )
A.稀释浓硫酸时,将浓硫酸沿着量筒壁慢慢的注入盛有水的量筒中,并不断搅拌
B.浓硫酸具有氧化性,稀硫酸无氧化性
C.浓硫酸不慎沾到皮肤上,应立即用布拭去,再用大量的水冲洗
D.浓硫酸与铜反应中,被氧化和被还原的物质的物质的量之比为1:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁和铁合金是生活中常用的材料,下列说法正确的是( )
A.不锈钢是铁合金,只含金属元素
B.一定条件下,铁粉可与水蒸气反应
C.铁与盐酸反应,铁合金不与盐酸反应
D.在空气中,铁板比镀锌铁板更耐腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SO2被称为“空中死神”,其对环境的危害常表现为_______________。为了减少危害,人们进行了许多有益的探索和研究,并且在实际应用上取得了一定的成果。
(1)工业上常用生石灰来处理煤炭中的SO2,这是利用了SO2属于_______氧化物的性质。
(2)近年来,有人提出了一种利用电解饱和氯化钠溶液,循环治理含二氧化硫的废气并回收二氧化硫的方法。该方法的流程如下:

①此种方法中,可以循环利用的物质是_____________________________。
②写出反应Ⅰ的离子方程式:_____________________________________。
(3)SO2通过下列工艺流程可制备化工原料H2SO4和清洁能源H2

下列说法中正确的是____________ 。
A. 设备A中的溴水褪色,体现了SO2的漂白性
B. 该生产工艺的优点:Br2可以循环利用,并获得清洁能源H2
C. 该工艺流程的总反应方程式为:SO2+2H2O=H2SO4+H2
D. 设备B中物质分离操作为过滤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com