
(12分)I.硝酸铜在1000℃时分【解析】
Cu(NO3)2=Cu+2NO2↑+O2,用试管收集一试管气体并倒立于盛水的水槽中,观察到的现象是 ,若溶质不扩散,试管内溶液中溶质的物质的量浓度是 (假设在标准状况下)。
II.工业上生产硝酸铜晶体的流程图如下:
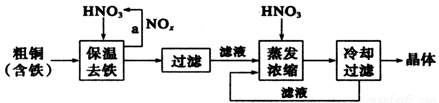
①若保温去铁反应生成气体是NO时,则离子方程式是 。
②蒸发浓缩时,要用硝酸调节溶液的pH=1,其目的是 (结合离子方程式说明)。
③如图所示为硝酸铜晶体[Cu(NO3)2·nH2O]的溶解度曲线(温度在30℃前后对应不同的晶体),从图中获取如下信息,不正确的有 (填字母)。

a.C点溶液为Cu(NO3)2的不饱和溶液
b.30℃时结晶可析出两种晶体
c.按上述流程最终得到的晶体是Cu(NO3)2·3H2O
d.将A点溶液升温至30℃时,可以析出Cu(NO3)2·3H2O晶体
④某些共价化合物(如H2O、NH3、N2O4等)在液态时发生了微弱的电离,如:2H2O OH—+H3O+, 则液态NH3电离的方程式是 ,液态N2O4电离得到电子数相差18的阴阳离子,因此可用Cu与液态N2O4反应制备无水硝酸铜,其反应的化学方程式是 。
OH—+H3O+, 则液态NH3电离的方程式是 ,液态N2O4电离得到电子数相差18的阴阳离子,因此可用Cu与液态N2O4反应制备无水硝酸铜,其反应的化学方程式是 。
Ⅰ.红棕色气体溶解成无色溶液,试管中的气柱为无色(2分)
0.036 mol·L-1或1/28 mol·L-1
Ⅱ.①3Fe + 8H+ + 2NO3- = 3Fe2++ 2NO↑ + 4H2O(2分)
②由于Cu2+发生水解:Cu2++2H2O Cu(OH)2+2H+,加入硝酸可以抑制硝酸铜的水解
Cu(OH)2+2H+,加入硝酸可以抑制硝酸铜的水解
③c、d(2分) ④ 2NH3 NH4++NH2- (1分) Cu+2N2O4=Cu(NO3)2+2NO↑(2分)
NH4++NH2- (1分) Cu+2N2O4=Cu(NO3)2+2NO↑(2分)
【解析】
试题分析:I.二氧化氮、氧气和水反应生成硝酸,化学方程式为4NO2+O2+2H2O=4HNO3,用试管收集一试管气体并倒立于盛水的水槽中,观察到的现象是红棕色气体溶解成无色溶液,试管中的气柱为无色,剩余气体为氧气;设二氧化氮为2mol,氧气为1mol,根据反应方程式知生成的硝酸为2mol,剩余气体0.5mol,进入试管内液体的体积为2.5mol×22.4L/mol=56L,即为稀硝酸的体积,试管内溶液中溶质的物质的量浓度c=n/V=2mol/56L=0.036 mol·L-1或1/28 mol·L-1;II.①保温去铁是铁与硝酸反应生成硝酸亚铁、一氧化氮和水,离子方程式是3Fe + 8H+ + 2NO3- = 3Fe2++ 2NO↑ + 4H2O;②蒸发浓缩时,要用硝酸调节溶液的pH=1,其目的是由于Cu2+发生水【解析】
Cu2++2H2O Cu(OH)2+2H+,加入硝酸可以抑制硝酸铜的水解;③ a.根据题给图像知,溶解度曲线上的点对应的溶液为饱和溶液,C点在曲线的下方,溶液为Cu(NO3)2的不饱和溶液,正确;b.根据题给图像知,30℃时结晶可析出两种晶体,正确;c.上述流程在低温下进行,最终得到的晶体是Cu(NO3)2·6H2O,错误;d.将A点溶液升温至30℃时,溶液为不饱和溶液,无晶体析出;④迁移题给水的电离方程式:2H2O
Cu(OH)2+2H+,加入硝酸可以抑制硝酸铜的水解;③ a.根据题给图像知,溶解度曲线上的点对应的溶液为饱和溶液,C点在曲线的下方,溶液为Cu(NO3)2的不饱和溶液,正确;b.根据题给图像知,30℃时结晶可析出两种晶体,正确;c.上述流程在低温下进行,最终得到的晶体是Cu(NO3)2·6H2O,错误;d.将A点溶液升温至30℃时,溶液为不饱和溶液,无晶体析出;④迁移题给水的电离方程式:2H2O OH—+H3O+,则液态NH3电离的方程式是2NH3
OH—+H3O+,则液态NH3电离的方程式是2NH3 NH4++NH2-,液态N2O4电离得到电子数相差18的阴阳离子,则液态四氧化二氮的电离方程式为2N2O4
NH4++NH2-,液态N2O4电离得到电子数相差18的阴阳离子,则液态四氧化二氮的电离方程式为2N2O4 NO++NO3-,根据原子守恒和电子守恒得用Cu与液态N2O4反应制备无水硝酸铜的化学方程式是Cu+2N2O4=Cu(NO3)2+2NO↑。
NO++NO3-,根据原子守恒和电子守恒得用Cu与液态N2O4反应制备无水硝酸铜的化学方程式是Cu+2N2O4=Cu(NO3)2+2NO↑。
考点:考查氮的氧化物的性质,溶解度曲线,盐类水解,化学工艺流程分析。


科目:高中化学 来源:2015届江苏省高三上学期期中考试化学试卷(解析版) 题型:选择题
火法炼铜首先要焙烧黄铜矿,主要涉及以下反应:①2CuFeS2+O2= Cu2S+2FeS+SO2②Cu2S+O2=2Cu+SO2,下列说法正确的是
A.在反应①中:SO2既是氧化产物又是还原产物
B.在反应②中:Cu2S仅作还原剂,硫元素被氧化
C.在反应①中:每转移1.2 mol电子,有0.2 mol硫被氧化
D.在反应②中:每消耗1.0 molCu2S,有4.0 mol电子转移
查看答案和解析>>
科目:高中化学 来源:2015届江苏省中学高三上学期第一次月考化学试卷(解析版) 题型:填空题
(12分)为探索工业废料的再利用,某化学兴趣小组设计了如下实验流程,用含有铝、铁和铜的合金废料制取氯化铝、绿矾晶体(FeSO4·7H2O)和胆矾晶体。
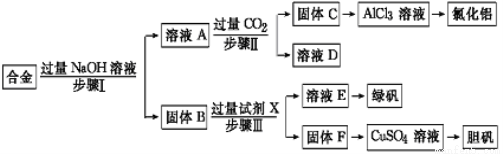
请回答:
(1)写出步骤Ⅰ反应的离子方程式: 。
(2)试剂X是 。步骤Ⅰ、Ⅱ、Ⅲ中均需进行的实验操作是 。
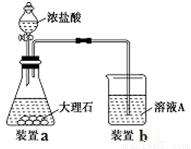
(3)进行步骤Ⅱ时,该小组用如下图所示装置及试剂制取CO2并将制得的气体通入溶液A中。一段时间后,观察到烧杯中产生的白色沉淀会逐渐减少。为了避免固体C减少,可采取的改进措施是 。
(4)用固体F制备CuSO4溶液,可设计以下三种途径:

写出途径①中反应的离子方程式 ,请选出你认为的最佳途径并说明选择的理由 。
查看答案和解析>>
科目:高中化学 来源:2015届广东省高三9月月考化学试卷(解析版) 题型:推断题
以甲苯为主要原料合成麻黄素的合成路线如下
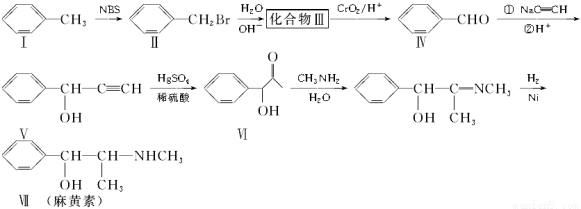
(1)化合物Ⅵ的分子式为________。
(2)化合物Ⅰ、Ⅱ、Ⅳ、Ⅴ能使Br2的CCl4溶液褪色是_______________________。
(3)化合物Ⅲ的结构简式为________,生成化合物Ⅶ的反应类型为________。
(4)在浓硫酸和加热条件下,麻黄素可以发生消去反应,该反应方程式为________________。
(5)任意写出满足下列条件的化合物Ⅵ的二种同分异构体______________________。
①含一个苯环 ②无酸性,酸性条件下水解生成两种有机物 ③能发生银镜反应
(6)如何通过实验证明化合物Ⅱ分子中含有溴元素,简述实验操作:______________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源:2015届广东省高三9月月考化学试卷(解析版) 题型:选择题
下列离子在溶液中能大量共存的一组是( )
A.Fe2+、H+、ClO-、SO32- B.K+、Al3+、Cl-、CO32-
C.Na+、Ca2+、HCO3-、OH- D.Fe2+、NH4+、NO3-、SO42-
查看答案和解析>>
科目:高中化学 来源:2015届江西南昌三中高三11月份月考化学试卷(解析版) 题型:选择题
向甲、乙两恒温恒容的密闭容器中,分别充入一定量的A和B,发生反应:A(g)+B(g) xC(g),△H<0。测得两容器中c(A)随时间t的变化如图所示:
xC(g),△H<0。测得两容器中c(A)随时间t的变化如图所示:


下列说法正确的是
A.x=1
B.Q1=2Q2
C.根据题中信息无法计算a值
D.保持其他条件不变,起始时向乙容器充入0.2 mol A、0.2 mol B、0.2 mol C,则此时v(正)> v(逆)
查看答案和解析>>
科目:高中化学 来源:2015届江西南昌三中高三11月份月考化学试卷(解析版) 题型:选择题
将某些化学知识用图像表示,可以收到直观、简明的效果。下列图象所表示的化学知识中,不正确的是

查看答案和解析>>
科目:高中化学 来源:2015届江苏连云港市高三上第一次月考化学试卷(解析版) 题型:选择题
下列变化中,需要加入氧化剂的是( )
A.SO2→SO3 B.HCl→H2 C.FeCl2→FeCl3 D.Fe2O3→Fe
查看答案和解析>>
科目:高中化学 来源:2015届江苏省盐城市、建湖二中高二上期中化学试卷(必修)(解析版) 题型:选择题
下列溶液中的Cl?浓度与50mL1 mol·L-1MgCl2溶液中的Cl?浓度相等的是
A.100 mL 1 mol·L-1 NaCl溶液
B.150 mL 2 mol·L-1 KCl溶液
C.25 mL 2 mol·L-1 CaCl2溶液
D.75 mL 1 mol ·L-1 AlCl3溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com