
【题目】工业废水中含有的Cr2O72-和CrO42-会对水体产生很大的危害,因此这种工业废水必须净化处理。一种处理含铬废水的工艺流程如下:
![]()
①中反应为2 CrO42-(黄色)+2H+![]() Cr2O72-(橙色)+H2O。
Cr2O72-(橙色)+H2O。
下列说法正确的是
A. ①中,酸化后废水黄色加深
B. ②中,反应的氧化剂与还原剂的物质的量之比为3︰1
C. ③中,所得沉淀Cr(OH)3中含有Fe(OH)3
D. ①中,所加酸可以是盐酸
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】在质量为G克的坩埚中,加入BaCl2.nH2O晶体后称得质量为W1克。加热使结晶水全部失去,冷却后称得坩埚和固体的质量为W2克。则n值为( )
A.![]() B.
B.![]()
C.![]() D.
D.![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)下列三组物质中,均有一种物质的类别与其他三种不同。
①MgO、Na2O、CO2、CuO②HCl、H2O、H2SO4、HNO3③NaOH、Na2CO3、KOH、Ba(OH)2
三种物质依次是(填化学式)_________、_______、________。
(2)某气体由双原子分子构成,它的摩尔质量为 Mg/mol。现有该气体 mg,按要求填空(设NA代表阿伏加德罗常数的数值,列表达式)
①该气体的物质的量为______mol;
②该气体在标准状况下的体积为______L;
③该气体在标准状况下的密度为______ g/L;
④该气体所含原子总数为______;
⑤该气体一个分子的质量为______g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学平衡原理在工农业生产中发挥着重要的指导作用。
(1)反应C(s)+CO2(g) ![]() 2CO(g)平衡常数K的表达式为________________;
2CO(g)平衡常数K的表达式为________________;
已知C(s) + H2O(g)![]() CO(g)+H2(g)的平衡常数为K1;H2(g)+CO2(g)
CO(g)+H2(g)的平衡常数为K1;H2(g)+CO2(g) ![]() CO(g)+H2O(g)的平衡常数为K2 ,则K与K1、K2二者的关系为________________________。
CO(g)+H2O(g)的平衡常数为K2 ,则K与K1、K2二者的关系为________________________。
(2)已知某温度下,反应2SO2+O22SO3,的平衡常数K=19
在该温度下的体积固定的密闭容器中,c0(SO2)=1mol·L-1,c0(O2)=1 mol·L-1,当反应在该温度下SO2转化率为80%时,该反应__________(填“是”或“否”)达到化学平衡状态,若未达到,向_________(填“正反应”或“逆反应”) 方向进行。
(3)对于可逆反应:aA(g) +bB(g) ![]() cC(g)+dD(g) △H = a kJ·mol-1;若a+b>c+d,减小压强平衡向_______(填“正反应”或“逆反应”)方向移动;若升高温度,平衡向逆反应方向移动,则a_______0(填“>”或“<”)
cC(g)+dD(g) △H = a kJ·mol-1;若a+b>c+d,减小压强平衡向_______(填“正反应”或“逆反应”)方向移动;若升高温度,平衡向逆反应方向移动,则a_______0(填“>”或“<”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,将1mol的CO和1mol水蒸气通入容器中发生下述反应:
CO+H2O![]() CO2+H2,达到平衡后,测得CO2为0.6mol,再通入0.4mol水蒸气,又达到平衡后,CO2的物质的量为
CO2+H2,达到平衡后,测得CO2为0.6mol,再通入0.4mol水蒸气,又达到平衡后,CO2的物质的量为
A. 等于0.6mol B. 等于1mol
C. 大于0.6mol且小于1mol D. 大于1mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温时,用0.100mol· L -1AgNO3溶液滴定50.0mL0.0500mol· L -1NaCl溶液的滴定曲如右图所示[pCl=-lg(Cl-)]。下列有关描述错误的是

A. 室温时Ksp(AgCl)的数量级为10-10
B. 室温时,各点Ksp(AgCl)的关系:a=b=c
C. 相同实验条件下,若改用0.0400mol· L-1 NaCl溶液,反应终点b移动到d
D. 相同实验条件下,若改用0.0500ml· L-1 NaBr溶液,反应终点b向e方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】空气污染物NO通常用含Ce4+的溶液吸收,生成HNO2、NO3-,再利用电解法将上述吸收液中的HNO2转化为无毒物质,同时生成Ce4+,其原理如图所示。下列说法正确的是
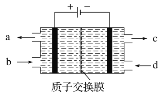
A. H+由右室进入左室
B. Ce4+从电解槽的c口流出,且可循环使用
C. 阴极的电极反应式:2HNO2+6H++6e-===N2↑+4H2O
D. 若用甲烷燃料电池作为电源,当消耗标准状况下33.6 L甲烷时,理论上可转化2mol HNO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)不能用手直接拿取金属钠,其理由是:___________________;
(2)资料显示,钠着火时不能CO2灭火,为寻找原因进行如下探究实验:A、将燃烧匙中的钠引燃后迅速伸入盛有CO2的集气瓶中。可以看到,火焰黄色,产生大量白烟;火焰熄灭后,集气瓶底部有黑色固体,瓶壁上附着白色固体;B、集气瓶中加入适量蒸馏水,振荡、过滤,滤纸上留下黑色固体,滤液为无色;C、取适量滤液置于两支试管中,向第一支试管中滴加一滴酚酞溶液,溶液变红,向第二支试管中滴加澄清石灰水,溶液变浑浊。写出实验C中澄清石灰水变浑浊的化学方程式:____________,根据以上实验事实判断实验B中的无色滤液显________(填“酸性”、“碱性”或者“中性”),根据以上实验事实写出:钠在点燃条件下与CO2反应化学方程式:_______________;
(3)用胶头滴管将新制的饱和氯水慢慢滴入含有酚酞的氢氧化钠稀溶液中,当滴到一定量时,红色突然褪去。试回答下列问题,产生上述现象的原因,①可能是氯水呈酸性,与氢氧化钠溶液中和使溶液褪色;②也可能是_________;设计出一个方案证明红色褪去的原因是①或②_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种以软锰矿(主要成分为MnO2、SiO2、Al2O3)和黄铁矿(FeS2、SiO2)为原料冶炼金属锰的工艺流程如图所示:
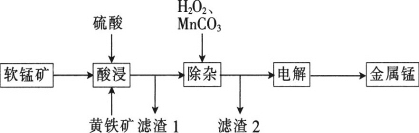
已知相关金属离子[c(Mn+)=0.1mol·L-1]形成氢氧化物沉淀的pH如下:
金属离子 | Fe3+ | Mn2+ | Al3+ |
开始沉淀的pH | 2.7 | 8.3 | 3.2 |
沉淀完全的pH | 3.7 | 9.8 | 5.0 |
回答下列问题:
(1)MnO2本身不能溶于硫酸,但是在Fe2+的作用下却能溶解,写出该反应的离子方程式:____________________________。
(2)滤渣1的成分除了SiO2外,还有一种淡黄色的物质是_______________(填化学式)。
(3)除杂步骤中加入的MnCO3的作用是____________________________,该过程需调节溶液pH的范围是___________________________,若把pH调得过高,其后果是_________________________。
(4)用惰性电极进行电解,电解刚开始时阴极的电极反应式为____________________,电解后阳极的电解质溶液可返回_______________________(填“酸浸”“除杂”或“电解”)工序继续使用。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com