
| A�� | ÿ����1molCH4���������·�ṩ4mole- | |
| B�� | ��طŵ����ҺPH�������� | |
| C�� | ������O2�õ����ӣ��缫��ӦʽΪ��O2+2H2O+4e-�T4OH- | |
| D�� | ������CH4ʧȥ���ӣ��缫��Ӧʽ��CH4+10OH--8e-�TCO32-+7H2O |
���� ���Լ���ȼ�ϵ�أ����л�ԭ�Եļ���Ϊԭ��صĸ���������������Ӧ���缫��ӦʽΪCH4+10OH--8e-=CO32-+7H2O��ͨ��������һ��Ϊԭ��ص�������������ԭ��Ӧ���缫��ӦʽΪO2+2H2O+4e-=4OH-��ԭ��ع���ʱ�����ӴӸ��������·�����������������Һ�У��������������ƶ������������ƣ�
��� �⣺A��ͨ��CH4�ĵ缫Ϊ�������缫��ӦΪ��CH4+10OH--8e-=CO32-+7H2O��ÿ����1molCH4���������·�ṩ8mole-����A����
B����ط�ӦʽΪ��CH4+2OH-+2O2=CO32-+3H2O�����ŷ�Ӧ�Ľ��У���Һ�����������Ӳ��ϼ��٣���ҺpH���ϼ�С�����Ըõ��ʹ��һ��ʱ���Ӧ����KOH����B����
C��ͨ��������һ��Ϊԭ��ص��������õ����ӷ�����ԭ��Ӧ��O2+2H2O+4e-=4OH-����C����
D��ͨ��CH4�ĵ缫Ϊ����ʧ���ӷ�Ӧ������Ӧ���缫��ӦΪ��CH4+10OH--8e-=CO32-+7H2O����D��ȷ��
��ѡD��
���� ���⿼����Լ����صĹ���ԭ������Ŀ�ѶȲ�������ע����յ缫��Ӧʽ����д����ȷ�ж������Ļ�ѧ��Ӧ����ѧϰ��ע����۵��ӡ����������ӵ�����


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ڷ�ӦCaH2+2H2O�TCa��OH��2+2H2���У�ˮ�������� | |
| B�� | ���ݷ�ӦCu+H2SO4$\frac{\underline{\;���\;}}{\;}$CuSO4+H2�����Ƴ�Cu�Ļ�ԭ�Ա�H2��ǿ | |
| C�� | ��Ӧ3NO2+H2O�T2HNO3+NO���������ͻ�ԭ�������ʵ���֮����3��1 | |
| D�� | ��Cl2��������ǿ��I2�������ԣ������û���ӦI2+2NaClO3�T2NaIO3+Cl2���ܷ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
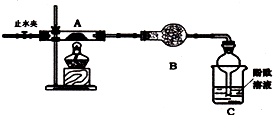

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
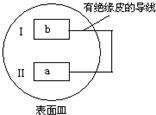 �ѻ��ý���Ƭa��b����ʢ��ϡʳ��ˮ�ͷ�̪���Һ�ı������У�������ͼ��ʾԭ��أ�һ��ʱ���۲쵽����I���ɫ��������������ȷ���ǣ�������
�ѻ��ý���Ƭa��b����ʢ��ϡʳ��ˮ�ͷ�̪���Һ�ı������У�������ͼ��ʾԭ��أ�һ��ʱ���۲쵽����I���ɫ��������������ȷ���ǣ�������| A�� | a��ԭ��صĸ��� | B�� | b�Ļ����Դ���a | ||
| C�� | �������� | D�� | b �缫�������ݲ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
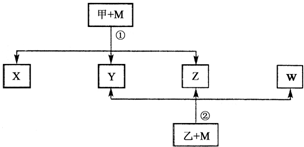
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ʵ��ʱ��������У�Ӧ������ˮ��ϴ��������գ�ۣ��������ִ����۾� | |
| B�� | ���������������Һ��Fe2+�ķ����ǣ��ȵμ����ư�ˮ��μ�KSCN��Һ | |
| C�� | ֤��������������ʴ�ķ����ǣ��ڶ�п��Ƥ�ϵ�1��3�κ���̪�ı���ʳ��ˮ������1��2min���۲����� | |
| D�� | ��Ϊ��������һ�ּ�����������Գ�������ɫ�����Ϳ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
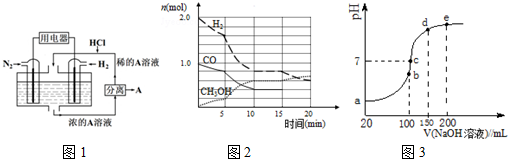
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 3.36L | B�� | 1.12L | C�� | 2.24L | D�� | 4.48L |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com