
 £ØR”¢R”䔢R”å“ś±ķōĒ»ł£©
£ØR”¢R”䔢R”å“ś±ķōĒ»ł£© £®
£® £®
£® £®
£®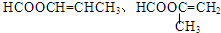 £®
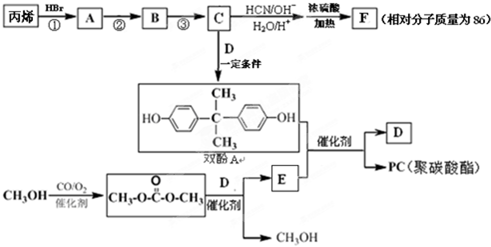
£®·ÖĪö ±ūĻ©¾¹żĻµĮŠ·“Ó¦µĆµ½C£¬CÓėD·“Ó¦µĆµ½Ė«·ÓA£¬CÄÜŗĶĒāĒčĖį·¢ÉśŠÅĻ¢ÖŠµÄ¼Ó³É·“Ó¦£¬øł¾ŻĢāøųŠÅĻ¢¼°Ė«·ÓAµÄ½į¹¹æÉÖŖ£¬CŹĒ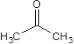 £¬ŌņBŹĒ
£¬ŌņBŹĒ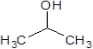 £¬DŹĒ
£¬DŹĒ £¬AŹĒ
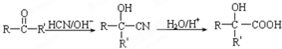
£¬AŹĒ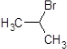 £¬±ūĶŖÓėHCN·“Ó¦”¢Ėį»ÆµĆµ½£ØCH3£©2C£ØOH£©COOH£¬MµÄĻą¶Ō·Ö×ÓÖŹĮæŹĒ86£¬±Č£ØCH3£©2C£ØOH£©COOHŠ”18£¬Ó¦ŹĒ£ØCH3£©2C£ØOH£©COOHŌŚÅØĮņĖį”¢¼ÓČČĢõ¼žĻĀ·¢Éś·Ö×ÓÄŚĶŃČ„1·Ö×ÓĖ®Éś³ÉF£¬ŌņFæÉÄÜĪŖCH2=C£ØCH3£©COOH»ņ
£¬±ūĶŖÓėHCN·“Ó¦”¢Ėį»ÆµĆµ½£ØCH3£©2C£ØOH£©COOH£¬MµÄĻą¶Ō·Ö×ÓÖŹĮæŹĒ86£¬±Č£ØCH3£©2C£ØOH£©COOHŠ”18£¬Ó¦ŹĒ£ØCH3£©2C£ØOH£©COOHŌŚÅØĮņĖį”¢¼ÓČČĢõ¼žĻĀ·¢Éś·Ö×ÓÄŚĶŃČ„1·Ö×ÓĖ®Éś³ÉF£¬ŌņFæÉÄÜĪŖCH2=C£ØCH3£©COOH»ņ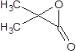 £¬Ģ¼Ėį¶ž¼×õ„ÓėD£Ø
£¬Ģ¼Ėį¶ž¼×õ„ÓėD£Ø £©·“Ó¦µĆµ½EÓė¼×“¼£¬ŌņEĪŖ
£©·“Ó¦µĆµ½EÓė¼×“¼£¬ŌņEĪŖ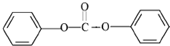 £¬Ė«·ÓAÓėE·“Ó¦µĆµ½±½·ÓÓėPC£¬ŌņPCĪŖ
£¬Ė«·ÓAÓėE·“Ó¦µĆµ½±½·ÓÓėPC£¬ŌņPCĪŖ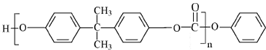 »ņ
»ņ £¬¾Ż“Ė½ā“š£®
£¬¾Ż“Ė½ā“š£®
½ā“š ½ā£ŗ±ūĻ©¾¹żĻµĮŠ·“Ó¦µĆµ½C£¬CÓėD·“Ó¦µĆµ½Ė«·ÓA£¬CÄÜŗĶĒāĒčĖį·¢ÉśŠÅĻ¢ÖŠµÄ¼Ó³É·“Ó¦£¬øł¾ŻĢāøųŠÅĻ¢¼°Ė«·ÓAµÄ½į¹¹æÉÖŖ£¬CŹĒ £¬ŌņBŹĒ
£¬ŌņBŹĒ £¬DŹĒ
£¬DŹĒ £¬AŹĒ
£¬AŹĒ £¬±ūĶŖÓėHCN·“Ó¦”¢Ėį»ÆµĆµ½£ØCH3£©2C£ØOH£©COOH£¬MµÄĻą¶Ō·Ö×ÓÖŹĮæŹĒ86£¬±Č£ØCH3£©2C£ØOH£©COOHŠ”18£¬Ó¦ŹĒ£ØCH3£©2C£ØOH£©COOHŌŚÅØĮņĖį”¢¼ÓČČĢõ¼žĻĀ·¢Éś·Ö×ÓÄŚĶŃČ„1·Ö×ÓĖ®Éś³ÉF£¬ŌņFæÉÄÜĪŖCH2=C£ØCH3£©COOH»ņ
£¬±ūĶŖÓėHCN·“Ó¦”¢Ėį»ÆµĆµ½£ØCH3£©2C£ØOH£©COOH£¬MµÄĻą¶Ō·Ö×ÓÖŹĮæŹĒ86£¬±Č£ØCH3£©2C£ØOH£©COOHŠ”18£¬Ó¦ŹĒ£ØCH3£©2C£ØOH£©COOHŌŚÅØĮņĖį”¢¼ÓČČĢõ¼žĻĀ·¢Éś·Ö×ÓÄŚĶŃČ„1·Ö×ÓĖ®Éś³ÉF£¬ŌņFæÉÄÜĪŖCH2=C£ØCH3£©COOH»ņ £¬Ģ¼Ėį¶ž¼×õ„ÓėD£Ø
£¬Ģ¼Ėį¶ž¼×õ„ÓėD£Ø £©·“Ó¦µĆµ½EÓė¼×“¼£¬ŌņEĪŖ
£©·“Ó¦µĆµ½EÓė¼×“¼£¬ŌņEĪŖ £¬Ė«·ÓAÓėE·“Ó¦µĆµ½±½·ÓÓėPC£¬ŌņPCĪŖ
£¬Ė«·ÓAÓėE·“Ó¦µĆµ½±½·ÓÓėPC£¬ŌņPCĪŖ »ņ
»ņ £¬
£¬
£Ø1£©CŹĒ±ūĶŖ£¬±ūĻ©ŗĶäå»ÆĒā·¢Éś¼Ó³É·“Ӧɜ³É2-äå±ūĶ飬2-äå±ūĶéŗĶĒāŃõ»ÆÄʵÄĖ®ČÜŅŗ·¢ÉśČ”“ś·“Ӧɜ³É2-±ū“¼£¬2-±ū“¼±»Ńõ»ÆÉś³É±ūĶŖ£¬
ĖłŅŌa£®¢ŁµÄ·“Ó¦ĄąŠĶŹĒ¼Ó³É·“Ó¦£¬
b£®¢ŚµÄ·“Ó¦ŹŌ¼ĮŗĶĢõ¼žŹĒĒāŃõ»ÆÄĘĖ®ČÜŅŗŗĶ¼ÓČČ£¬
c£®¢ŪµÄ»Æѧ·½³ĢŹ½ŹĒ £¬
£¬
¹Ź“š°øĪŖ£ŗ¼Ó³É·“Ó¦£»ĒāŃõ»ÆÄĘĖ®ČÜŅŗ”¢¼ÓČČ£» £»
£»
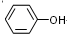
£Ø2£©ĶعżŅŌÉĻ·ÖĪöÖŖ£¬DŹĒ±½·Ó£¬ŌņDµÄ½į¹¹¼ņŹ½ŹĒ  £¬¹Ź“š°øĪŖ£ŗ
£¬¹Ź“š°øĪŖ£ŗ £»
£»
£Ø3£©CÓėD·“Ӧɜ³ÉĖ«·ÓAµÄ»Æѧ·½³ĢŹ½ŹĒ £¬
£¬
¹Ź“š°øĪŖ£ŗ £»
£»
£Ø4£©FŹĒ2-¼×»ł±ūĻ©Ėį£¬FÓŠ¶ąÖÖĶ¬·ÖŅģ¹¹Ģ壬FµÄĶ¬·ÖŅģ¹¹Ģå·ūŗĻĻĀĮŠĢõ¼ž¢Łŗ¬ÓŠ¼×»ł”¢¢Śŗ¬ÓŠĢ¼Ģ¼Ė«¼ü”¢¢ŪÄÜ·¢ÉśŅų¾µ·“Ó¦ĖµĆ÷ŗ¬ÓŠČ©»ł”¢¢ÜŹōÓŚõ„ĖµĆ÷ŗ¬ÓŠõ„»ł£¬Ōņ·ūŗĻĢõ¼žµÄFµÄĶ¬·ÖŅģ¹¹Ģå½į¹¹¼ņŹ½ĪŖ£ŗ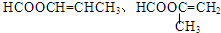 £¬¹Ź“š°øĪŖ£ŗ
£¬¹Ź“š°øĪŖ£ŗ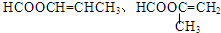 £»
£»
µćĘĄ ±¾Ģāæ¼²éĮĖÓŠ»śĪļµÄŗĻ³É£¬Ć÷Č·ÓŠ»śĪļµÄ¹ŁÄÜĶż°ĘäŠŌÖŹŹĒ½ā±¾Ģā¹Ų¼ü£¬ŅŌCĪŖĶ»ĘĘæŚ²ÉÓĆÕżÄęĻą½įŗĻµÄ·½·Ø½ųŠŠ·ÖĪö½ā“š£¬Ć÷Č·ÓŠ»ś·“Ó¦ÖŠ»Æѧ¼üµÄ±ä»Æ£¬ÄѶČÖŠµČ£®


 ×ŪŗĻ×Ō²āĻµĮŠ“š°ø
×ŪŗĻ×Ō²āĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | K+”¢Ba2+”¢OH-”¢SO42- | B£® | Ag+”¢NO3-”¢Cl-”¢K+ | ||
| C£® | H3O+”¢NO3-”¢Fe2+”¢Na+ | D£® | Cu2+”¢NH4+”¢Br-”¢OH- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŅŃÖŖC£ØŹÆÄ«£¬s£©=C£Ø½šøÕŹÆ£¬s£©”÷H£¾0£¬Ōņ½šøÕŹÆ±ČŹÆÄ«ĪČ¶Ø | |
| B£® | C£Øs£©+$\frac{1}{2}$O2£Øg£©=CO£Øg£©”÷H=-101.5 kJ•mol-1£¬øĆ·½³ĢŹ½µÄ”÷HæɱķŹ¾Ģ¼µÄČ¼ÉÕČČ | |
| C£® | ŅŃÖŖ£ŗC£Øs£©+O2£Øg£©=CO2£Øg£©”÷H1C£Øs£©+$\frac{1}{2}$O2£Øg£©=CO £Øg£©”÷H2£¬Ōņ”÷H1£¼”÷H2 | |
| D£® | Ba£ØOH£©2£Øaq£©+H2SO4£Øaq£©£©=BaSO4£Øs£©+2H2O£Øl£©”÷H=-2a kJ•mol-1£¬ŌņČĪŗĪĒæĖįŗĶĒæ¼ī·¢ÉśÖŠŗĶ·“Ӧɜ³É1 mol H2O£Øl£©µÄ·“Ó¦ČČ¾łĪŖ-a kJ•mol-1 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

 £®
£® £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
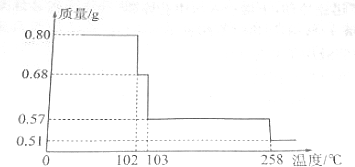
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | H2O£Øg£©=H2£Øg£©+$\frac{1}{2}$O2£Øg£©”÷H=242 kJ?mol-1 | B£® | 2H2£Øg£©+O2£Øg£©=2H2O£Øg£©”÷H=-484 kJ?mol-1 | ||
| C£® | H2£Øg£©+$\frac{1}{2}$O2£Øg£©=H2O£Ø1£©”÷H=-242 kJ?mol-1 | D£® | 2H2£Øg£©+O2£Øg£©=2H2O£Øg£©”÷H=+484 kJ?mol-1 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | AsH3£¾NH3£¾PH3 | B£® | PH3£¾AsH3£¾NH3 | C£® | NH3£¾PH3£¾AsH3 | D£® | NH3£¾AsH3£¾PH3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
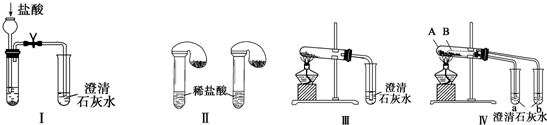
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com