
����Ŀ����һ���������İ���������������Ƶ��ܱ����������![]() ��������������䣬��������������Բ���
��������������䣬��������������Բ���![]() ��ʹ��ﵽ�ֽ�ƽ�⣺
��ʹ��ﵽ�ֽ�ƽ�⣺![]() ��ʵ���ò�ͬ�¶��µ�ƽ�����������±���
��ʵ���ò�ͬ�¶��µ�ƽ�����������±���
�¶� |
|
|
|
|
|
ƽ��������Ũ�� |
|
|
|
|
|
�����й�������ȷ����
A.�ÿ��淴Ӧ�ﵽƽ��ı�־֮һ�ǻ������ƽ����Է�����������
B.��÷�Ӧ![]() ��
��![]() �������ڵ������Է�����
�������ڵ������Է�����
C.�ﵽƽ������ں�����ѹ�������������ϵ�������Ũ������
D.���ݱ������ݣ�����![]() ʱ�ķֽ�ƽ�ⳣ��ԼΪ
ʱ�ķֽ�ƽ�ⳣ��ԼΪ![]()
���𰸡�D
��������
A���ӷ�Ӧ��ʼ��������ƽ����Է�������ʼ�ղ��䣬���Բ�����Ϊƽ��״̬�ı�־����A����
B�����ݱ��������ж������¶����ߣ�ƽ���ƶ��ķ��Ӷ��жϳ�����Ӧ�����ȣ������ʱ䣨��H������0��������̬���ʵ��ش���Һ̬���ʵ����жϳ���Ӧ�ر䣨��S������0�������ڸ������Է����У���B����
C����ƽ������ں�����ѹ�����������ƽ�������ƶ������¶Ȳ��䣬ƽ�ⳣ�����䣬�����ϵ�������Ũ�Ȳ��䣬��C����
D�����ݱ������ݣ�ƽ���������Ũ��Ϊ4.8��10-3mol/L�������������Ũ��֮��Ϊ2��1����NH3��CO2��Ũ�ȷֱ�Ϊ3.2��10-3mol/L��1.6��10-3mol/L������ƽ�ⳣ������ʽ��K=��3.2��10-3��2��1.6��10-3=![]() ����D��ȷ��
����D��ȷ��
��ѡD��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ƺ��¹���������Ļ��Һ����Ϊ̼�ظֵĻ�ʴ���������£�̼�ظ������ֲ�ͬ�����еĸ�ʴ����ʵ������ͼ��ʾ������˵������ȷ���ǣ� ��

A.�����Ũ��Խ��ʴ����Խ��
B.̼�ظֵĸ�ʴ���ʲ��������Ũ�����������˵����Ӧ���ʲ���c��H+��������
C.�����ƺ��¹����������Ũ�����ʱ����ʴ������С
D.�Ա�����������������ߣ���֪Cl-Ҳ���ܻ�Ӱ��̼�ظֵĸ�ʴ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(1)�״�![]() ����Ҫ���ܼ������ȼ�ϣ���ҵ����CO��H2��һ���������Ʊ�
����Ҫ���ܼ������ȼ�ϣ���ҵ����CO��H2��һ���������Ʊ�![]() �ķ�Ӧ��
�ķ�Ӧ��![]() �������Ϊ1L�ĺ����ܱ������У���2molCO��
�������Ϊ1L�ĺ����ܱ������У���2molCO��![]() ��һ�������·���������Ӧ�����
��һ�������·���������Ӧ�����![]() ��
��![]() ��Ũ����ʱ��仯��ͼ��ʾ��
��Ũ����ʱ��仯��ͼ��ʾ��
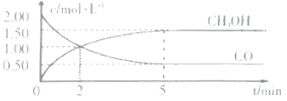
�ٴӷ�Ӧ��ʼ��5min����һ����̼��ʾ��ƽ����Ӧ��������CO��=______��
������˵����ȷ����______��
A.�ﵽƽ��ʱ��![]() ��ת����Ϊ
��ת����Ϊ![]()
B.5min�������л�������ƽ����Է����������ٸı�
C.�ﵽƽ����ٳ��백������Ӧ���ʼ�С
D.2minǰ��������>�����棩��2min����������<�����棩
(2)һ���¶��£���![]() ��
��![]() �������1��2�����ܱ������з�����Ӧ��
�������1��2�����ܱ������з�����Ӧ��
![]() ���ﵽƽ��ʱ
���ﵽƽ��ʱ![]() ���������Ϊ
���������Ϊ![]() ���÷�Ӧ��ƽ�ⳣ��
���÷�Ӧ��ƽ�ⳣ��![]() ______��
______��
(3)̼��ˮ������Ӧ��ȡ![]() ����ط�Ӧ���£�
����ط�Ӧ���£�
��![]()
��![]()
��![]()
�ټ��㷴Ӧ![]() ��
��![]() ______
______![]()
�ڶ��ڿ��淴Ӧ![]() ����ȡ���´�ʩ�������
����ȡ���´�ʩ�������![]() ���ʵ���______��
���ʵ���______��
A.������ϵ���¶�
B.ѹ�����������
C.����CaO����
D.ѡ���ʵ��Ĵ���
(4)�Լ״�Ϊȼ�ϣ�![]() Ϊ��������KOH��ҺΪ�������Һ�����Ƴ�ȼ�ϵ��
Ϊ��������KOH��ҺΪ�������Һ�����Ƴ�ȼ�ϵ��![]() �缫����Ϊ���Ե缫
�缫����Ϊ���Ե缫![]() ����KOH��Һ������д����ȼ�ϵ�ظ����ĵ缫��Ӧʽ��______��
����KOH��Һ������д����ȼ�ϵ�ظ����ĵ缫��Ӧʽ��______��
(5)����20mL![]() ������
������![]() ��Һ����μ���һ��Ũ�ȵ��ռ���Һ����û����Һ���¶ȱ仯��ͼ��ʾ�������й�˵����ȷ����______
��Һ����μ���һ��Ũ�ȵ��ռ���Һ����û����Һ���¶ȱ仯��ͼ��ʾ�������й�˵����ȷ����______
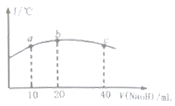
�ٸ��ռ���Һ��Ũ��Ϊ![]()
�ڸ��ռ���Һ��Ũ��Ϊ![]()
��![]() �ĵ���ƽ�ⳣ����b��
�ĵ���ƽ�ⳣ����b��![]() ��
��
�ܴ�b�㵽c�㣬�����Һ��һֱ���ڣ�c(Na+)>c(NO2-)>c(OH-)>c(H+)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����10L�ܱ������У�A��B��C������̬���ʹ����˿��淴Ӧ����ϵ��һ�������£�A��B��C�����������ʵ���![]() ��ʱ��
��ʱ��![]() �Ĺ�ϵ��ͼһ��ʾ��C�İٷֺ���
�Ĺ�ϵ��ͼһ��ʾ��C�İٷֺ���![]() ���¶�
���¶�![]() �Ĺ�ϵ��ͼ����ʾ�����з����������
�Ĺ�ϵ��ͼ����ʾ�����з����������
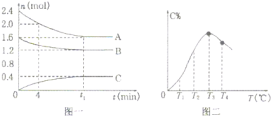
A.![]() ʱ��A��ƽ����Ӧ����Ϊ
ʱ��A��ƽ����Ӧ����Ϊ![]()
B.ͼ����![]() ��
��![]() ��Ӧ�����ϵĵ㶼���ڻ�ѧƽ��״̬
��Ӧ�����ϵĵ㶼���ڻ�ѧƽ��״̬
C.��![]() ��
��![]() �仯ʱ��
�仯ʱ��![]()
D.�÷�Ӧ������ӦΪ���ȷ�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£���һ�ݻ�������ܱ������з����Ŀ��淴Ӧ2X��g��![]() Y��g��+Z��s��������ѡ�����Ϊ��Ӧ�ﵽƽ���־����
Y��g��+Z��s��������ѡ�����Ϊ��Ӧ�ﵽƽ���־����
A. ��Ӧ������ѹǿ���ٱ仯 B. ���������ܶȲ��ٱ仯
C. ��������ƽ����Է����������ٱ仯 D. Z��Ũ�Ȳ��ٸı�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ�鷽�������ﵽ��ӦĿ�ĵ���
A | B | C | D | |
Ŀ�� | �Ƚ�̼�����̼�����ˮ��̶� | �о�Ũ�ȶԻ�ѧƽ���Ӱ�� | �Ƚϲ�ͬ�����Ի�ѧ��Ӧ���ʵ�Ӱ�� | �Ƚ�̼�ᡢ��������������ǿ�� |
ʵ�鷽�� |
|
|
|
|
A. AB. BC. CD. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���¶��£���ij�ܱ�������ijһ��Ӧ��M��N�����ʵ����淴Ӧʱ��仯��������ͼ��ʾ�����������У���ȷ����
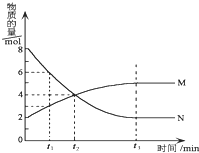
A.�÷�Ӧ�Ļ�ѧ����ʽΪ![]()
B.��![]() ����Ӧ��ʼ��
����Ӧ��ʼ��![]() ʱ���M �ķ�Ӧ����Ϊ
ʱ���M �ķ�Ӧ����Ϊ![]()
C.![]() ʱ���淴Ӧ������ȣ���Ӧ�ﵽƽ��״̬
ʱ���淴Ӧ������ȣ���Ӧ�ﵽƽ��״̬
D.![]() ʱ����Ӧ���ʵ����淴Ӧ����
ʱ����Ӧ���ʵ����淴Ӧ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ҹ�������ǿ��������CO2���⻯�ϳɼ״������Ĺ�ҵ�������о���ʵ�ֿɳ�����չ��
(1)��֪��CO2(g)+H2(g) H2O(g) +CO(g) ��H1 = + 41.1 kJmol-1
CO(g)+2H2(g) CH3OH(g) ��H2=��90.0 kJmol-1
д��CO2���⻯�ϳɼ״����Ȼ�ѧ����ʽ��___________________________________________��
(2)Ϊ���CH3OH���ʣ�������Ӧ���õ�������_______������ĸ����
a�����¸�ѹ b�����µ�ѹ c�����µ�ѹ d�����¸�ѹ
(3)250�桢�ں����ܱ���������CO2(g)���⻯�ϳ�CH3OH(g)����ͼΪ��ͬͶ�ϱ�[n(H2)/n(CO2)]ʱij��Ӧ��Xƽ��ת���ʱ仯���ߡ�
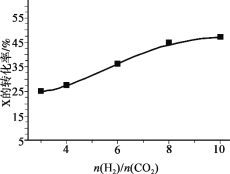
��Ӧ��X��_______������CO2������H2������
(4)250�桢�����Ϊ2.0L�ĺ����ܱ������м���6mol H2��2mol CO2�ʹ�����10minʱ��Ӧ�ﵽƽ�⣬���c(CH3OH) = 0.75 mol�� L��1��
�ٻ�ѧƽ�ⳣ��K = _______��
�ڴ����ͷ�Ӧ�����뷴Ӧ��ת���ʺͲ����ѡ�����и߶���ء�������ͬͶ�ϱȺ���ͬ��Ӧʱ�䣬����ʵ���������£�
ʵ���� | �¶ȣ�K�� | ���� | CO2ת���ʣ�%�� | �״�ѡ���ԣ�%�� |
A | 543 | Cu/ZnO���װ� | 12.3 | 42.3 |
B | 543 | Cu/ZnO����Ƭ | 11.9 | 72.7 |
C | 553 | Cu/ZnO���װ� | 15.3 | 39.1 |
D | 553 | Cu/ZnO����Ƭ | 12.0 | 70.6 |
�����ϱ��������ݣ���CO2�����״�������ѡ��Ϊ_______������ĸ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijѧ����0.1500mol/LNaOH��Һ�ⶨijδ֪Ũ�ȵ����ᣬ������ɷֽ�Ϊ���¼�����
A.������ˮϴ���ζ���
B.�ô��ⶨ����Һ��ϴ��ʽ�ζ���
C.����ʽ�ζ���ȡϡ����25.00mL��ע����ƿ�У������̪
D.��ȡ��ƿ�����ظ�����2-3��
E.���ζ����Ƿ�©ˮ
F.ȡ�¼�ʽ�ζ����ñ�NaOH��Һ��ϴ����Һע���ʽ�ζ�����0���̶�����2-3cm�����ٰѼ�ʽ�ζ��̶ܹ��ã�����Һ������0���̶Ȼ���0���̶�����
G.����ƿ���ڵζ������棬ƿ�µ�һ�Ű�ֽ���ߵα�ҡ����ƿֱ���ζ��յ㣬���µζ���Һ�����ڿ̶�
���������գ�
��1���ζ�ʱ��ȷ������˳����(�������ĸ��д)�� �� ��F�� �� �� ��D��___
��2������F��Ӧ��ѡ��ͼ�еζ���___(����)��
![]()
��3���ζ��յ��������___��
��4���ζ���������ʾ��
�ζ����� | ����Һ���/mL | ����Һ�����/mL | |
�ζ�ǰ�̶� | �ζ���̶� | ||
1 | 25.00 | 1.02 | 21.03 |
2 | 25.00 | 0.60 | 20.60 |
3 | 25.00 | 0.20 | 20.19 |
�������������ʵ���Ũ��Ϊ___(����4λ��Ч����)��
��5�����в����ᵼ�²ⶨ���ƫ�ߵ���___��
A.����ʽ�ζ�������ƿ�з�����ʱ�������Ӻ�ƽ�Ӷ���
B.��ƿ��������ϴ
C.��ʽ�ζ��ܼ��첿���ڵζ�ǰû�����ݣ��ζ��յ�ʱ��������
D.�ﵽ�ζ��յ�ʱ�����Ӷ���
��6����֪��c(NH4Cl)��0.1mol��L��1����pH��5.1������������0.1mol��L��1����ζ�10mL0.05mol��L��1��ˮ��������ָʾ�����ﵽ�յ�ʱ�����������Ӧ��___5mL��������������<������=������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com