

| A、步骤④的操作是过滤 |
| B、可用淀粉溶液检验步骤②的反应是否进行完全 |
| C、步骤①、③的操作分别是过滤、萃取 |
| D、步骤③中加入的有机溶剂可能是酒精或CCl4 |


科目:高中化学 来源: 题型:
| A、Zn2++2OH-═Zn(OH)2↓ ZnCO3+2NaOH═Zn(OH)2↓+Na2CO3 |
| B、Ag++Cl-═AgCl↓ AgNO3+NaCl═AgCl↓+NaNO3 |
| C、Ba2++SO42-═BaSO4↓ Ba(OH)2+CuSO4═BaSO4↓+Cu(OH)2↓ |
| D、Cu+2Ag+═Cu2++2Ag↓ Cu+2AgCl═2Ag+CuCl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| 物质组成 | 甲 | 乙 | 丙 | 丁 |
| 化合物中各元素 原子个数比 | A和C 1:1 | B和A 1:4 | D和E 1:3 | B和E 1:4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、产物B的状态一定为气态 |
| B、平衡时,单位时间内消耗n(A)与消耗n(C)相等 |
| C、保持体积不变,向平衡体系中加入B平衡向逆反应方向移动 |
| D、若开始时向容器中加入1molB和1molC,达到平衡时放出热量QkJ |
查看答案和解析>>
科目:高中化学 来源: 题型:
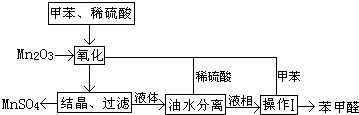
| 反应时间/h | 1 | 2 | 3 | 4 | 5 |
| 苯甲醛产率/% | 76.0 | 87.5 | 83.6 | 72.5 | 64.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:
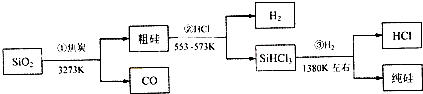
| A、①②③均属于氧化还原反应 |
| B、H2和HCl均可循环利用 |
| C、SiO2是一种坚硬难熔的固体 |
| D、光纤的主要成分是高纯度的单质硅 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com