
·ÖĪö £Ø1£©ŅĄ¾ŻÅäÖĘŅ»¶ØĪļÖŹµÄĮæÅضČČÜŅŗµÄŅ»°ć²½ÖčÅÅŠņ£»
£Ø2£©ŅĄ¾ŻÅäÖĘŅ»¶ØĪļÖŹµÄĮæÅضČČÜŅŗµÄŅ»°ć²½ÖčŃ”ŌńŠčŅŖŅĒĘ÷£»
£Ø3£©·ÖĪö²Ł×÷¶ŌČÜÖŹµÄĪļÖŹµÄĮæŗĶČÜŅŗĢå»żµÄÓ°Ļģ£¬ŅĄ¾ŻC=$\frac{n}{V}$½ųŠŠĪó²ī·ÖĪö£»
½ā“š ½ā£ŗ£Ø1£©ÅäÖĘ²½ÖčÓŠ¼ĘĖć”¢³ĘĮ攢Čܽā”¢ŅĘŅŗ”¢Ļ“µÓ”¢¶ØČŻ”¢Ņ”ŌČµČ²Ł×÷£¬
¹Ź“š°øĪŖ£ŗČܽā£»ŅĘŅŗ£»Ļ“µÓ£»
£Ø2£©ÅäÖĘ²½ÖčÓŠ¼ĘĖć”¢³ĘĮ攢Čܽā”¢ĄäČ“”¢ŅĘŅŗ”¢Ļ“µÓ”¢¶ØČŻ”¢Ņ”ŌČµČ²Ł×÷£¬Ņ»°ćÓĆĶŠÅĢĢģĘ½³ĘĮ棬ÓĆŅ©³×Č”ÓĆŅ©Ę·£¬ŌŚÉÕ±ÖŠČܽā£¬ĄäČ“ŗó×ŖŅʵ½500mLČŻĮæĘæÖŠ£¬²¢ÓĆ²£Į§°ōŅżĮ÷£¬µ±¼ÓĖ®ÖĮŅŗĆę¾ąĄėæĢ¶ČĻß1”«2cmŹ±£¬øÄÓĆ½ŗĶ·µĪ¹ÜµĪ¼Ó£¬ĖłŅŌŠčŅŖµÄŅĒĘ÷ĪŖ£ŗĶŠÅĢĢģĘ½”¢Ņ©³×”¢ÉÕ±”¢²£Į§°ō”¢500mLČŻĮæĘ攢½ŗĶ·µĪ¹Ü£¬ĖłŅŌ»¹ŠčŅŖµÄŅĒĘ÷£ŗ500mLČŻĮæĘ攢½ŗĶ·µĪ¹Ü£»
¹Ź“š°øĪŖ£ŗ500mLČŻĮæĘ攢½ŗĶ·µĪ¹Ü£»
£Ø3£©¶ØČŻŗ󣬼ÓøĒµ¹×ŖŅ”ŌČŗ󣬷¢ĻÖŅŗĆęµĶÓŚæĢ¶ČĻߣ¬ÓÖµĪ¼ÓÕōĮóĖ®ÖĮæĢ¶ČĻߣ¬µ¼ÖĀČÜŅŗĢå»żĘ«“ó£¬ČÜŅŗÅضČĘ«µĶ£»
¹Ź“š°øĪŖ£ŗĘ«µĶ£»Ņ”ŌČŗóŌŁ¼ÓÕōĮóĖ®µ¼ÖĀČÜŅŗĢå»żĘ«“ó£®
µćĘĄ ±¾Ģāæ¼²éĮĖŅ»¶ØĪļÖŹµÄĮæÅضČČÜŅŗµÄÅäÖĘŅŌ¼°Īó²ī·ÖĪö£¬Ć÷Č·ŹµŃéµÄ»ł±¾²Ł×÷·½·ØŗĶ×¢ŅāŹĀĻīŹĒ½āĢā¹Ų¼ü£¬ĢāÄæÄŃ¶Č²»“ó£®


 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¼ĘĖćĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | v£ØNH3£©=0.2mol£ØL•s£© | B£® | v£ØO2£©=1.4mol£ØL•min£© | C£® | v£ØH2O£©=0.2mol£ØL•s£© | D£® | v£ØNO£©=9mol£ØL•min£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

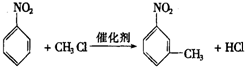 £®
£®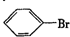 £®
£®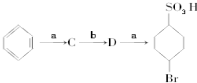 ”±ÖŠµÄ·“Ó¦ÖŠŹōÓŚČ”“ś·“Ó¦µÄŹĒab£¬ŹōÓŚ¼Ó³É·“Ó¦µÄŹĒc£ØĢī×ÖÄø£©£®
”±ÖŠµÄ·“Ó¦ÖŠŹōÓŚČ”“ś·“Ó¦µÄŹĒab£¬ŹōÓŚ¼Ó³É·“Ó¦µÄŹĒc£ØĢī×ÖÄø£©£®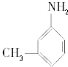 µÄĖłÓŠŌ×Ó²»ŹĒ£ØĢī”°ŹĒ”±»ņ”°²»ŹĒ”±£©ŌŚĶ¬Ņ»Ę½ĆęÉĻ£®
µÄĖłÓŠŌ×Ó²»ŹĒ£ØĢī”°ŹĒ”±»ņ”°²»ŹĒ”±£©ŌŚĶ¬Ņ»Ę½ĆęÉĻ£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | H2SO4 Na2CO3 NaCl CuO | |
| B£® | H2O Ca£ØOH£©2 HCl Na2SO4 | |
| C£® | H2SO4 NaOH Na2CO3 Fe2O3 | |
| D£® | NaOH H2CO3 NaCl CO2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĒāĘųŗĶĀČĘų·“Ӧɜ³ÉĀČ»ÆĒāĘųĢåµÄČČ»Æѧ·½³ĢŹ½ĪŖ£ŗH2£Øg£©+Cl2£Øg£©=2HCl£Øg£©”÷H=-183kJ | |
| B£® | ĒāĘųÓėĀČĘų·“Ӧɜ³É4.48LĀČ»ÆĒāĘųĢ壬·“Ó¦µÄ”÷H=-183kJ/mol | |
| C£® | ĒāĘųÓėĀČĘų·“Ӧɜ³É2molĀČ»ÆĒāĘųĢ壬·“Ó¦µÄ”÷H=+183kJ/mol | |
| D£® | ĒāĘųÓėĀČĘų·“Ӧɜ³ÉĀČ»ÆĒāĘųĢå·Å³ö183KJµÄČČĮæŹ±£¬×ŖŅʵē×ÓĪļÖŹµÄĮæĪŖ2 mol |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ±ź×¼×“æöĻĀ56 g ĢśŌ×Ó | B£® | ±ź×¼×“æöĻĀ1mol C2H5OH | ||
| C£® | ±ź×¼×“æöĻĀ6.02”Į1023 øöNH3 | D£® | Ķس£×“æöĻĀ1molHCl |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com