
【题目】元素周期表中铋元素的数据如图,下列说法正确的是( ) 
A.Bi元素的质量数是209
B.Bi元素的相对原子质量是209.0
C.Bi原子6p亚层有一个未成对电子
D.Bi原子最外层有5个能量相同的电子
【答案】B
【解析】解:A、元素是互为同位素原子的总称,不谈质量数,故A错误;
B、元素周期表中外围电子排布下方的数值为元素的相对原子质量,由图可知,Bi元素的相对原子质量是209.0,故B正确;
C、Bi原子的外围电子排布为6s26p3,p能级有3个轨道,p能级的3个电子优先各占据1个轨道,Bi原子6p亚层都是单电子,故C错误;
D、6p能级的能量高于6s能级能量,二者不是简并轨道,Bi原子最外层5个电子的能量不完全相同,6p能级的3个电子能力相同,6s能级的2个电子能量相同,故D错误;
故选B.
A、元素是互为同位素原子的总称,不谈质量数;
B、元素周期表中外围电子排布下方的数值为元素的相对原子质量;
C、Bi原子的外围电子排布为6s26p3,p能级有3个轨道,p能级的3个电子优先各占据1个轨道;
D、6p能级的能量高于6s能级能量.


科目:高中化学 来源: 题型:
【题目】化学能与热能、电能等可以相互转化,下列说法正确的是
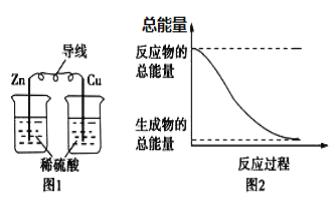
A. 图1所示的装置能将化学能转变为电能
B. 图2所示的反应为吸热反应
C. 化学反应中能量变化的主要原因是化学键的断裂与生成
D. 中和反应中,反应物的总能量比生成物的总能量低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁是一种在生产和生活中应用广泛的金属元素。己知:
反应Ⅰ:Fe2O3(s)+ 3H2(g)=2Fe(s)+3H2O(g) ΔH1= +89 .6kJ /mol
反应Ⅱ:4Fe2O3(s)+Fe(s)=3Fe3O4(s) ΔH2=+2833.4kJ/mol
反应Ⅲ:Fe(s)+2HCl(g)![]() FeCl2(l)+H2(g) ΔH3
FeCl2(l)+H2(g) ΔH3
(1)反应Ⅰ的平衡常数表达式K=______________,该反应在高温下进行,最易生成的副产物是________________ (填化学式)。
(2)温度为T1时,恒容密闭容器中发生反应Ⅲ,反应时间与体系压强关系如图a所示,体系温度与HCl转化率关系如图b所示。
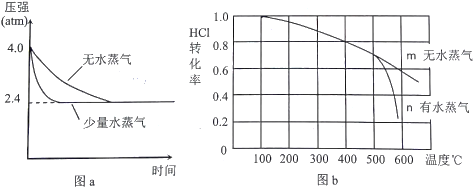
①分析图a,容器内通入少量水蒸气的作用是___________________。
②分析图b,ΔH3________0(填“>”、“<”或“=”),结合图a分析,T1=___________℃。
③分析图b,高于500℃后,曲线n发生的副反应热化学方程式为________________________________, 曲线n中HCl转化率明显降低的原因是____________________________________。
(3)①CaFeO4可制作半导体材料,向1L的高铁酸钠(Na2FeO4)溶液中加入0.0056g生石灰开始生成CaFeO4沉淀,原高铁酸钠溶液的物质的量浓度为________mol/L。已知Ksp(CaFeO4)=4.54×10-9,溶液体积变化忽略不计。
②用K2FeO4代替MnO2制备的碱性干电池(KOH做电解液)具有能量密度大、寿命长、无污染等优点,正极反应生成Fe2O3,写出正极的电极反应式______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】控制适合的条件,将反应Fe3++AgFe2++Ag+设计成如右图所示的原电池,(盐桥装有琼脂﹣硝酸钾溶液;灵敏电流计的0刻度居中,左右均有刻度)已知,接通后,观察到电流计指针向右偏转.下列判断正确的是( ) 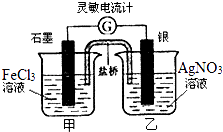
A.在外电路中,电子从石墨电极流向银电极
B.盐桥中的K+移向乙烧杯
C.一段时间后,电流计指针反向偏转,越过0刻度,向左边偏转
D.电流计指针居中后,往甲烧杯中加入一定量的铁粉,电流计指针将向左偏转
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面所写的有机反应方程式及其类型都正确的是
A.  取代反应
取代反应
B. 2CH3CHO+ O2 → 2CH3COOH 氧化反应
C. CH2=CH2 + Br2 → CH3CHBr2 加成反应
D. HCOOH + CH3CH2OH ![]() HCOOCH3CH2+ H2O 取代反应
HCOOCH3CH2+ H2O 取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钙能调节人体各系统生理功能,利用如图装置测定碳酸钙型补钙剂中钙的含量。已知氨基磺酸(H2NSO3H)俗称固体硫酸,在水溶液中为一元酸,广泛应用于锅炉水垢的清洗。
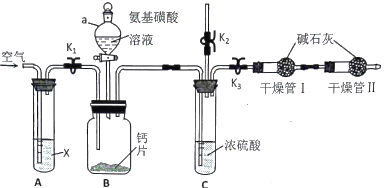
(1)A装置的作用为___________________,仪器a的名称为____________________。
(2)B 装置内发生反应的化学方程式为___________________________________,实验中不用盐酸与钙片反应的原因是_______________________________________。
(3)组装好仪器后,检查装置的气密性,接下来进行的操作是:打开K1、K2,关闭K3,通空气一段时间, ________________(填操作),打开仪器a活塞,滴入氨基磺酸溶液,待B装置中无气泡产生,关闭仪器a活塞。再次打开K1通空气一段时间,第二次通入空气目的是_______________________。如果不使用干燥管Ⅱ,测定结果____________(填“偏高”“偏低”“不变”)。
(4)取某补钙剂样品m克进行测定,测得干燥管Ⅰ在实验前后重量分别为m1克和m2克,则样品中钙的质量分数为__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,有关说法正确的是( )

A. e的氢化物比d的氢化物稳定
B. a、b、e三种元素的原子半径:e>b>a
C. 六种元素中,c元素单质的化学性质最活泼
D. c、e、f的最高价氧化物对应的水化物的酸性依次增强
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com