
【题目】现有4种物质:碳酸氢钠、硫酸钡、烧碱、苯。(以下必须填写化学式)
(1)属于碱的是________________;
(2)属于硫酸盐的是________________;
(3)属于酸式盐的是________________;
(4)属于有机物的是________________。
【答案】NaOH BaSO4 NaHCO3 C6H6
【解析】
(1)碱是电离产生的阴离子全部为氢氧根离子的化合物,烧碱化学式为NaOH,电离产生的阴离子全部为氢氧根离子,因此烧碱属于碱;;
(2)硫酸盐是由硫酸根离子(![]() )与其他金属离子(或铵根)组成的化合物,硫酸钡化学式为BaSO4,是由
)与其他金属离子(或铵根)组成的化合物,硫酸钡化学式为BaSO4,是由![]() 和Ba2+组成的化合物,则属于硫酸盐的是硫酸钡;
和Ba2+组成的化合物,则属于硫酸盐的是硫酸钡;
(3)酸式盐定义为:电离时生成的阳离子除金属离子(或铵根)外还有氢离子,阴离子为酸根离子的盐,碳酸氢钠化学式为NaHCO3,在溶液中电离时可生成钠离子和碳酸氢根离子,碳酸氢根离子又可以电离产生氢离子和碳酸根离子,属于酸式盐的是碳酸氢钠;
(4)有机物是含碳化合物(碳氧化物、碳硫化物、碳酸、碳酸盐、碳酸氢盐、金属碳化物、氰化物、硫氰化物、碳硼烷、烷基金属、羰基金属、金属的有机配体配合物等除外)或碳氢化合物及其常见衍生物的总称,苯化学式为C6H6,是由碳元素和氢元素构成的有机化合物,则属于有机物的是苯。


科目:高中化学 来源: 题型:
【题目】有关晶体的结构如图所示,下列说法中不正确的是( )
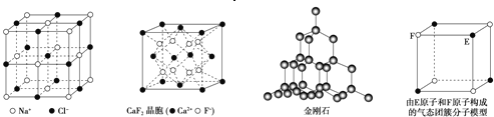
A.在NaCl 晶体中,距Na 最近的Cl 形成正八面体
B.在![]() 晶体中,每个晶胞平均占有4 个Ca2+
晶体中,每个晶胞平均占有4 个Ca2+
C.在金刚石晶体中,碳原子与碳碳键个数的比为1:2
D.该气态团簇分子的分子式为EF或FE
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醛是现在老百姓最关心的一个热点问题,甲醛已经被世界卫生组织认定为一类致癌物。我国科学家研制出一种催化剂,能在室温下高效催化空气中甲醛的氧化,其反应如下:HCHO+O2![]() CO2+H2O。下列有关说法正确的是( )
CO2+H2O。下列有关说法正确的是( )
A.反应物和生成物都含有π键
B.0.5molHCHO含有1molσ键
C.HCHO、CO2中心原子杂化类型相同
D.HCHO能溶解在H2O中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】莫沙朵林是一种镇痛药,它的合成路线如下:
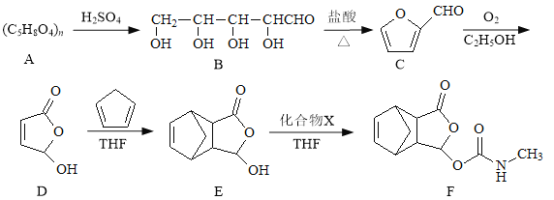
(1)B中手性碳原子数为_________________;化合物C中无氧官能团的名称为_________________。
(2)下列说法正确的是_________________。
A.B与葡萄糖是同系物关系
B.A→B是水解反应
C.E可以发生消去反应,F可与HC1反应
(3)C与银氨溶液反应的化学方程式为_________________。
(4)写出同时满足下列条件的E的同分异构体任意一种结构简式:_________________。
I.核磁共振氢谱有4个峰;
Ⅱ.能发生银镜反应和水解反应;
Ⅲ.能与FeCl3溶液发生显色反应。
(5)已知E+X→F为加成反应,化合物X的结构简式为_________________。
(6)已知: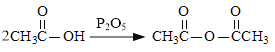 。化合物
。化合物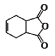 是合成抗病毒药阿昔洛韦的中间体,若以
是合成抗病毒药阿昔洛韦的中间体,若以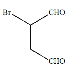 和
和![]() 为原料合成该化合物。请按要求完成下列转化过程:
为原料合成该化合物。请按要求完成下列转化过程: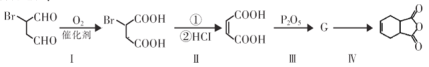
①第I步的反应类型_________________。
②上述步骤Ⅱ中①的反应条件_________________。
③第Ⅲ步中G的结构简式_________________。
④第Ⅳ步的化学方程式_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,表中所列的字母分别代表一种元素。
A | R | |||||||||||||||||
B | C | D | E | F | T | |||||||||||||
G | H | I | J | K | L | |||||||||||||
M | N | O | ||||||||||||||||
试回答下列问题(注意:每问中的字母代号为上表中的字母代号,并非为元素符号)
(1)N的单质和水蒸气反应能生成固体X,则I的单质与X高温下反应的化学方程式______。
(2)D的简单气态氢化物的VSEPR模型的名称为______。
(3)由A、C、D形成的ACD分子中,σ键和π键个数=______。
(4)元素M的化合物(ME2L2)在有机合成中可作氧化剂或氯化剂,能与许多有机物反应。回答问题:
①ME2L2常温下为深红色液体,能与CCl4、CS2等互溶,据此可判断ME2L2是______(填“极性”或“非极性”)分子。
②将N和O的单质用导线连接后插入D的最高价氧化物对应的水化物浓溶液中,可制成原电池,则组成负极材料的元素的外围电子轨道表示式为______。
(5)如图四条折线分别表示ⅣA族、Ⅴ/span>A族、ⅥA族、ⅦA族元素气态氢化物沸点变化,则E的氢化物所在的折线是______(填m、n、x或y)。
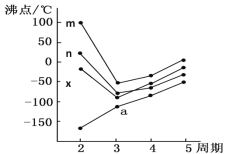
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分别调节0.01mol·L-1HCOOH溶液、0.01mol·L-1氨水的pH,系统中微粒浓度的负对数值(-lgc)与pH的关系分别如下图所
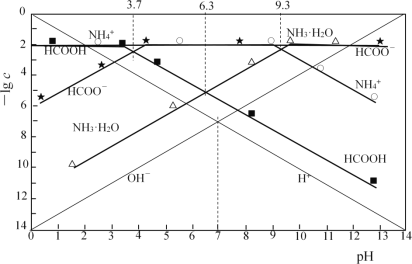
下列说法错误的是
A. 25℃时,NH3·H2O![]() NH4++OH-的lgK=-4.7
NH4++OH-的lgK=-4.7
B. 25℃时,0.01mol·L-1HCOOH溶液的pH为3.7
C. HCOONa溶液中加入NH4Cl至溶液呈中性:c(Cl-)>c(Na+)>c(HCOO-)
D. HCOONa溶液中加入KHSO3至溶液呈中性:c(HCOOH) +c(H2SO3) = c(SO32-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水中含有80多种元素,是重要的物质资源宝库,同时海水具有强大的自然调节能力,为解决环境污染问题提供了广阔的空间。
(1)①已知不同pH条件下,水溶液中碳元素的存在形态如下图所示。下列说法不正确的是______________(填字母序号)。

a.pH=8时,溶液中含碳元素的微粒主要是HCO3-
b.A点,溶液中H2CO3和HCO3-浓度相同
c.当c(HCO3-)=c(CO32-)时,c(H+)>c(OH -)
②向上述pH=8.4的水溶液中加入NaOH溶液时发生反应的离子方程式是______________。
(2)海水pH稳定在7.9—8.4之间,可用于烟道气中CO2和SO2的吸收剂。
①海水中含有的OH -可以吸收烟道气中的CO2同时为海水脱钙,生产CaCO3。写出此反应的离子方程式:__________。
②已知:25℃时,H2CO3电离平衡常数K1=4.3×10-7 K2=5.6×10 -11
H2SO3电离平衡常数K1=1.5×10-2 K2 =6.0×10-8
海水中含有的HCO3-可用于吸收SO2,该过程的离子方程式是_______________。
(3)洗涤烟气后的海水呈酸性,需处理后再行排放。与新鲜海水混合同时鼓入大量空气排出部分CO2,是一种处理的有效方式。
①通入O2可将酸性海水中的硫(IV)氧化,该反应的离子方程式是_______________。
②上述方式使处理后海水pH升高的原因是_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于反应2SO2(g)+O2(g)2SO3(g)的描述正确的是( )
A.使用催化剂,SO2的平衡转化率增大
B.增大O2浓度,平衡常数K增大
C.当2![]() 正(SO2)=
正(SO2)=![]() 逆(O2)时,反应达到平衡状态
逆(O2)时,反应达到平衡状态
D.升高温度,反应物中活化分子百分数提高,反应速率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为探究外界条件对反应:mA(g) +nB(g)![]() cZ(g) △H的影响,以A和B物质的量之比为 m:n开始反应,通过实验得到不同条件下达到平衡时Z的物质的量分数,实验结果如图所示。下列判断正确的是( )
cZ(g) △H的影响,以A和B物质的量之比为 m:n开始反应,通过实验得到不同条件下达到平衡时Z的物质的量分数,实验结果如图所示。下列判断正确的是( )
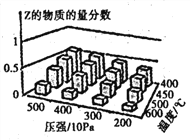
A.在恒温恒容条件下,向已达到平衡的体系中加入少量Z,平衡正向移动,Z的含量增大
B.升高温度,正、逆反应速率都增大,平衡常数增大
C.△H<0 m + n >c
D.△H>0 m +n<c
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com