
(选做题12分)
以富含硫酸亚铁的工业废液为原料生产氧化铁的工艺如下(部分操作和条件略):
Ⅰ.从废液中提纯并结晶出FeSO4·7H2O。
Ⅱ.将FeSO4·7H2O配制成溶液。
Ⅲ.FeSO4溶液与稍过量的NH4HCO3溶液混合,得到含FeC03的浊液。
Ⅳ.将浊液过滤,用90℃热水洗涤沉淀,干燥后得到FeC03固体。
ⅴ.煅烧FeCO3,得到Fe2O3固体。
已知:NH4HCO3在热水中分解。
(1)Ⅰ中,加足量的铁屑除去废液中的Fe3+,该反应的离子方程式是 。
(2)Ⅱ中,需加一定量硫酸。运用化学平衡原理简述硫酸的作用 。
(3)Ⅲ中,生成FeCO3的离子方程式是 。若FeCO3浊液长时间暴露在空气中,会有部分固体表面变为红褐色,该变化的化学方程式 。
(4)IV中,通过检验SO42-来判断沉淀是否洗涤干净。检验SO42的操作是 。
(5)已知煅烧FeC03的化学方程式是4FeCO3+O2  2Fe2O3+4CO2。现煅烧464.0 kg的FeCO3,得到316.8 kg产品。若产品中杂质只有FeO,则该产品中Fe2O3的质量是 Kg。(摩尔质量/g·mol-1:FeCO3 116 Fe2O3 160 FeO 72)
2Fe2O3+4CO2。现煅烧464.0 kg的FeCO3,得到316.8 kg产品。若产品中杂质只有FeO,则该产品中Fe2O3的质量是 Kg。(摩尔质量/g·mol-1:FeCO3 116 Fe2O3 160 FeO 72)
(1)Fe+2Fe3+=3Fe2+(2)加入硫酸,H+浓度增大,使Fe2++2H2O Fe(OH)2+2H+ 平衡向逆反应方向移动,从而抑制FeSO4的水解
Fe(OH)2+2H+ 平衡向逆反应方向移动,从而抑制FeSO4的水解
(3)Fe2++2HCO3-=FeCO3↓+CO2↑+H2O 4FeCO3+6H2O+O2=4Fe(OH)3↓+4CO2↑
(4)取少量洗涤后的滤液放入试管中,滴加酸化的BaCl2溶液,若无白色沉淀产生,则沉淀洗涤干净
(5)288.0
【解析】
试题分析:(1)Fe3+和Fe反应生成Fe2+,该反应的离子方程式是Fe+2Fe3+=3Fe2+;(2)Fe2+水解,Fe2++2H2O Fe(OH)2+2H+,加入硫酸,H+浓度增大,抑制FeSO4的水解;(3)Fe2++2HCO3-=FeCO3↓+CO2↑+H2O;亚铁盐易被氧气氧化,反应方程式为4FeCO3+6H2O+O2=4Fe(OH)3↓+4CO2↑;(4)若洗涤干净,则洗涤后的滤液中不含SO42—,所以取少量洗涤后的滤液放入试管中,滴加酸化的BaCl2溶液,若无白色沉淀产生,则沉淀洗涤干净;(5)设产品中含Fe2O3 Xmol、FeO Ymol;
Fe(OH)2+2H+,加入硫酸,H+浓度增大,抑制FeSO4的水解;(3)Fe2++2HCO3-=FeCO3↓+CO2↑+H2O;亚铁盐易被氧气氧化,反应方程式为4FeCO3+6H2O+O2=4Fe(OH)3↓+4CO2↑;(4)若洗涤干净,则洗涤后的滤液中不含SO42—,所以取少量洗涤后的滤液放入试管中,滴加酸化的BaCl2溶液,若无白色沉淀产生,则沉淀洗涤干净;(5)设产品中含Fe2O3 Xmol、FeO Ymol;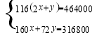 ,x=1800 mol;氧化铁的质量为288.0 Kg。
,x=1800 mol;氧化铁的质量为288.0 Kg。
考点:本题考查物质制备。


 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案科目:高中化学 来源:2014-2015学年甘肃省天水市高三上学期第四次检测化学试卷(解析版) 题型:填空题
(10分)蛇纹石可用于生产氢氧化镁,简要工程如下:
Ⅰ.制取粗硫酸镁:用酸液浸泡蛇纹石矿粉,过滤,并在常温常压下结晶,制得粗硫酸镁(其中常含有少量Fe3+、Al3+、Fe2+等杂质离子)
Ⅱ.提纯粗硫酸镁,将粗硫酸镁在酸性条件下溶解,加入适量的0.1mol/LH2O2溶液,再调节溶液pH至7~8,并分离提纯。
Ⅲ.制取氢氧化镁,向步骤II所得溶液中加入过量氨水。
已知:金属离子氢氧化物沉淀所需pH
Fe3+ | Al3+ | Fe2+ | Mg2+ | |
开始沉淀时 | 1.5 | 3.3 | 6.5 | 9.4 |
沉淀完全时 | 3.7 | 5.2 | 9.7 | 12.4 |
请回答:
(1)步骤II中加入适量的0.1mol/LH2O2溶液的目的是 ;可用于调节溶液pH至7~8的最佳试剂是 (填字母序号)
A.MgO B.Na2CO3 C.蒸馏水 D.NaOH .
(2)工业上常以Mg2+的转化率为考查指标,确定步骤III制备氢氧化镁工艺过程的适宜条件。
其中,反应温度与Mg2+转化率的关系如图所示。
①步骤III中制备氢氧化镁反应的离子方程式为 。根据图中所示50℃前温度与Mg2+转化率之间的关系,可判断此反应是 (填“吸热”或“放热”反应)

②图中,温度升高至50℃以上Mg2+转化率下降的可能原因是 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省莆田市高三上学期第二次月考化学试卷(解析版) 题型:选择题
金属钛对体液无毒且有惰性,能与肌肉和骨骼生长在一起,有“生物金属”之称。下列有关 和
和 的说法中正确的是
的说法中正确的是
A. 和
和 原子中均含有22个中子
原子中均含有22个中子
B.分别由 和
和 组成的金属钛单质互称为同分异构体
组成的金属钛单质互称为同分异构体
C. 与
与 为同一核素
为同一核素
D. 与
与 互称同位素,在周期表中位置相同,都在第4 纵行
互称同位素,在周期表中位置相同,都在第4 纵行
查看答案和解析>>
科目:高中化学 来源:2014-2015河南省英文学校高一上学期12月月考化学试卷(解析版) 题型:选择题
把铁片分别放入下列溶液中,铁片溶解,而溶液质量增加,但无气体产生,此溶液是
A.稀硫酸 B.AgNO3溶液
C.Fe2(SO4)3溶液 D.CuSO4溶液
查看答案和解析>>
科目:高中化学 来源:2014-2015河南省英文学校高一上学期12月月考化学试卷(解析版) 题型:选择题
下列关于Na和Na+的叙述中,错误的是
A.它们相差一个电子层 B.它们的化学性质相似
C.钠原子,钠离子均为同一元素 D.灼烧时,它们的焰色反应都呈黄色
查看答案和解析>>
科目:高中化学 来源:2014-2015河南省高二上学期第三次月考化学试卷(解析版) 题型:填空题
(9分)下表是不同温度下水的离子积数据:
温度/℃ | 25 | t1 | t2 |
Kw/ mol2·L-2 | 1×10-14 | a | 1×10-12 |
试回答以下几个问题:
(1)若25< t1< t2,则a 1×10-14(填“<”、“>”或“=”),由此判断的理由是:
。
(2)在t1℃下,pH=10的NaOH溶液中,水电离产生的[OH-]为: 。
(3)在t2℃下,将pH=11的苛性钠溶液V1 L与pH=1的硫酸溶液V2 L混合(设混合后溶液体积为原两溶液体积之和)所得溶液的pH=2,则V1︰V2 = ,此溶液中各种离子的浓度由大到小的顺序是 。
查看答案和解析>>
科目:高中化学 来源:2014-2015河南省高二上学期第三次月考化学试卷(解析版) 题型:选择题
已知温度T℃时水的离子积常数为Kw,该温度下,将浓度为a mol?L?1的一元酸HA与b mol?L?1的一元碱BOH等体积混合,可判定该溶液呈中性的依据是
A.a = b C.混合溶液中,c(H+)=  mol?L?1
mol?L?1
B.混合溶液的pH=7 D.混合溶液中,c(H+)+ c(B+) = c(OH-)+ c(A-)
查看答案和解析>>
科目:高中化学 来源:2014-2015河南省高一上学期第三次考试化学试卷(解析版) 题型:选择题
有一粉末,它是由铁的氧化物物中的一种或两种组成,取3.04 g粉末加热,同时通入足量的CO使之完全反应,再用澄清石灰水把产生的气体充分吸收,产生沉淀5g,则该粉末的组成可能是
A.只有Fe2O3 B.只有FeO
C.等物质的量的FeO和Fe3O4 D.等物质的量的Fe2O3和Fe3O4
查看答案和解析>>
科目:高中化学 来源:2014-2015河南省高二上学期第三次考试化学试卷(解析版) 题型:选择题
下列说法正确的是
A.强电解质溶液的导电能力一定比弱电解质溶液的导电能力强
B.物质的量浓度相同的磷酸钠(Na3PO4)溶液和磷酸(H3PO4)溶液中PO43-的物质的量浓度相同
C.足量Zn分别和等体积、等物质的量浓度的盐酸和醋酸反应时,产生H2的量相同,放出H2的速率不等。
D.因为CH3COOH是弱电解质,HCl是强电解质,所以中和等体积等物质的量浓度的醋酸和盐酸时,中和醋酸消耗的NaOH比盐酸消耗的NaOH用量少
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com