

| A��ʳ�� | B���Ȼ��� | C��̼���� | D��̼������ |
 MgCO3��+H2O+CO2���� MgCO3+H2O
MgCO3��+H2O+CO2���� MgCO3+H2O Mg(OH)2+CO2��
Mg(OH)2+CO2�� ��
��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| ������ | PbSO4 | PbCO3 | PbS |
| �ܽ��/g | 1.03��10��4 | 1.81��10��7 | 1.84��10��14 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��ϡ��ǰ����Һ pH���٣��� = �� |
| B��ϡ��ǰ����Һ�����ʵ����ʵ���Ũ�ȣ��ۣ��� =�� |
| C��ϡ�ͺ���Һ pH���٣��� = �� |
| D��ϡ�ͺ���Һ�����ʵ����ʵ���Ũ�ȣ��ۣ��� =�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�ʵ����
| ʵ�鲽�� | ��3��4 mL 1 mol/L��CaCl2��Һ�е���1mol/L��Na2SO4��Һ����Ӧ��ȫ�� |
| ʵ������ | ������ɫ���� |
| ���ӷ���ʽ | ��1�� |
| С�����۽��� | ��������Ӧ�����Һ�е�������1mol/L��Na2CO3��Һ�����ʲô���� |
| ������ֵ�ʵ������˵������ | ����� ������ ���ɣ���Ӧû���ȣ�Ca2+������ȫ �����2�� �����ɣ���3�� ���� |
| ֤����ļ��� | �����������İ�ɫ���� |
| ���ӷ���ʽ | ��4�� |
| ʵ����� | ��5�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| �������� | Fe(OH)3 | Mg(OH)2 | Al(OH)3 | |
| ��ʼ������pH | 2.3 | 10.8 | 3.7 | ��ʼ�ܽ��pH:7.8 |
| ��ȫ������pH | 4.3 | 12.4 | 5.2 | ��ȫ�ܽ��pH:10.0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 ������˵����ȷ���ǣ� ��
������˵����ȷ���ǣ� ��| A����Һ���¶����ߣ�BaSO4���ܶȻ��������� |
| B����Na2SO4��Һ�У�BaSO4���ܽ�Ȳ��� |
| C����BaCl2��Һ�У�BaSO4���ܶȻ�������С |
| D������NaClʱ������Һ�м����Թ�����BaCl2��Һ��Ϊ�˸��õس�ȥSO42-������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��40 mL 1 mol/L��BaCl2��Һ |
| B��30 mL 2 mol/L��Ba(OH)2��Һ |
| C��10 mL��ˮ |
| D��50 mL 0.1 mol/L��H2SO4��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
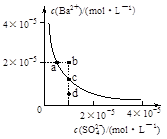
| A������Na2SO4����ʹ��Һ��a��䵽b�� |
| B��ͨ����������ʹ��Һ��d��䵽c�� |
| C��d����BaSO4�������� |
| D��a���Ӧ��BaSO4��Ksp����c���Ӧ��Ksp |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com