

分析 (1)SO2多余的尾气一般通过NaOH溶液来吸收反应生成亚硫酸钠和水;二氧化硫易溶于水需要防倒吸吸收;
(2)验证上述反应所产生的各种产物,应避免二氧化硫对二氧化碳检验产生的干扰,装置D是碳和浓硫酸的发生反应,生成的气体利用A检验生成的水蒸气,利用装置E检验二氧化硫的存在,通过装置C除去二氧化硫,再通过装置E检验二氧化硫是否除净,通过装置B中澄清石灰水检验二氧化碳的存在;
(3)酸雨腐蚀钢铁是铁和稀硫酸反应生成硫酸亚铁和氢气;
(4)SO2是还原剂,在反应中硫元素化合价+4价升高,标注反应中硫元素化合价变化分析判断选项.
解答 解:(1)实验室制备SO2多余的尾气一般通过NaOH溶液来吸收,此反应的化学方程式为:SO2+2NaOH=Na2SO3+H2O,二氧化硫易溶于水,可用于SO2吸收的装置需要防止倒吸,装置AC和直接通入水中相同,容易引起倒吸,装置B中倒扣在水面的漏斗可以防止倒吸,装置D中的干燥管上方面积较大,可以防止倒吸,故选BD,
故答案为:SO2+2NaOH=Na2SO3+H2O;BD;
(2)验证上述反应所产生的各种产物,应避免二氧化硫对二氧化碳检验产生的干扰,装置D是碳和浓硫酸的发生反应,生成的气体利用A检验生成的水蒸气,利用装置E检验二氧化硫的存在,通过装置C除去二氧化硫,再通过装置E检验二氧化硫是否除净,通过装置B中澄清石灰水检验二氧化碳的存在
①实验中装置A中无水硫酸铜可以观察到的现象是白色变为蓝色,装置D中①仪器的名称是分液漏斗,故答案为:变蓝; 分液漏斗;
②增加一个E装置,验证SO2是否除净,避免对CO2检验时的干扰,所以方案Ⅱ更合理,
故答案为:Ⅱ;增加一个E装置,验证SO2是否除净,避免对CO2检验时的干扰;
(3)酸雨是由SO2经过一系列转化最终生成硫酸,酸雨会严重腐蚀钢铁,酸雨腐蚀钢铁的过程中发生的化学反应方程式为:Fe+H2SO4=FeSO4+H2↑,
故答案为:Fe+H2SO4=FeSO4+H2↑;
(4)A.SO2+Cl2+2H2O=2HCl+H2SO4 反应中硫元素化合价升高做还原剂,故A正确;
B.SO2+2H2S=3S↓+2H2O,反应中二氧化硫中元素化合价+4价变化为0价,化合价降低做氧化剂,故B错误;
C.SO2+H2O=H2SO3 反应中硫元素化合价不变,不是氧化还原反应,故C错误;
D.5SO2+2KMnO4+2H2O=K2SO4+2MnSO4+2H2SO4,反应中硫元素化合价+4价变化为+6价,二氧化硫做还原剂,故D正确;
故答案为:AD.
点评 本题考查了物质性质的分析应用,主要是硫及其化合物性质、气体实验验证的方法和反应现象反判断,掌握基础是解题关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 容器内气体密度不再发生变化 | |
| B. | 容器内各物质的浓度不再发生变化 | |
| C. | v正(H2)=v逆(NH3) | |
| D. | 单位时间消耗0.1mol N2的同时生成0.2mol NH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
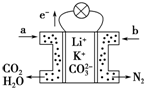 某种熔融碳酸盐燃料电池以Li2CO3、K2CO3为电解质,以C4H10为燃料时,该电池工作原理如图.下列说法正确的是( )
某种熔融碳酸盐燃料电池以Li2CO3、K2CO3为电解质,以C4H10为燃料时,该电池工作原理如图.下列说法正确的是( )| A. | a为C4H10,b为CO2 | |
| B. | 在熔融电解质中,CO32-向正极移动 | |
| C. | 此电池在常温时也能工作 | |
| D. | 通入丁烷的一极是负极,电极反应为:C4H10-26e-+13CO32-=17CO2↑+5H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 猜想1 | 猜想2 | 猜想3 |
| 只有CO | 只有 | 含有CO和CO2 |

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 项 目 | 每100克(g) | 营养素参考值% |
| 能 量 | 1500kJ | 18% |
| 蛋 白 质 | 0g | 0% |
| 脂 肪 | 2.0g | 3% |
| 碳水化合物 | 72g | 24% |
| 钠 | 30mg | 2% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ③④⑤ | C. | ⑤⑥⑦ | D. | ②③⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | AgI比AgCl稳定 | B. | 碘氧化性比氯弱 | ||
| C. | I-的还原性比Cl-强 | D. | 溶解度AgI<AgCl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯和聚乙烯均能使溴水褪色 | |
| B. | 甲烷、苯和油脂均不能使酸性KMnO4溶液褪色 | |
| C. | 乙酸和乙酸乙酯均能发生取代反应 | |
| D. | 蔗糖和麦芽糖是同分异构体,均可以水解且产物相同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com