
| A.原子半径:A>B>D>C | B.原子序数:d>c>b>a |
| C.离子半径:C>D>B>A | D.单质的还原性:A>B>D>C |
 轻松暑假总复习系列答案
轻松暑假总复习系列答案科目:高中化学 来源:不详 题型:实验题
 转化关系:
转化关系: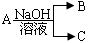 ,(若产物中有水生成则省略未表示出来)。
,(若产物中有水生成则省略未表示出来)。 ,且其在电子工业中有着重要的用途,则工业制取A化学方程式为 ;
,且其在电子工业中有着重要的用途,则工业制取A化学方程式为 ;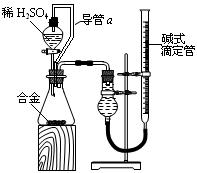
 ;
;查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A. 35Cl2与37Cl2互为同分异构体 |
| B.35Cl与37Cl的原子结构示意图不同 |
| C.通过化学变化可以实现35Cl与37Cl间的相互转化 |
| D.常温常压下,1.12LH35Cl与1.12LH37Cl所含原子总数相等 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.它位于周期表第四周期第VIA族 |
| B.最高价氧化物为SeO2,为酸性氧化物 |
| C.原子半径比钙小 |
| D.气态氢化物化学式为H2Se |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| | d | |
| a | b | c |
| A. a、b、c的最高价氧化物对应水化化物的酸性 强弱关系是c>b>a | B. d的氢化物没有b的氢化物稳定 | C.原子半径的大小关系c>b>a |
| D.单质的氧化性关系: a >b |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com