
分析 氧化铜可与盐酸反应,反应后的溶液加入过量氢氧化钠生成氢氧化铜沉淀,加热沉淀分解又可生成氧化铜.
解答 解:铜与盐酸不反应,为不活泼金属,可加入盐酸,氧化铜可与盐酸反应,发生CuO+2HCl═CuCl2+H2O,反应后的溶液加入过量氢氧化钠生成氢氧化铜沉淀,发生CuCl2+2NaOH═Cu(OH)2↓+2NaCl,过滤,将滤渣加热沉淀分解又可生成氧化铜,发生Cu(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CuO+H2O,
答:将混合物滴入盐酸后过滤(CuO+2HCl═CuCl2+H2O);将滤液加入NaOH溶液生成沉淀滤出〔CuCl2+2NaOH═Cu(OH)2↓+2NaCl〕将滤渣加热即得到CuO〔Cu(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CuO+H2O〕.
点评 本题考查混合物的分离,为高频考点,侧重于学生的分析、实验能力的考查,注意把握物质的性质的异同,为解答该题的关键,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | H2的燃烧热(△H)是285.8kJ•mol-1 | |
| B. | 反应2H2O(g)=2H2(g)+O2(g)H2的焓变(△H)是571.6kJ•mol-1 | |
| C. | 反应2H2O(l)=2H2(g)+O2(g)只能在电解条件下进行 | |
| D. | 反应2H2O(l)=2H2(g)+O2(g)在一定条件下可以自发进行 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

| 物质 | KMnO4 | K2CO3 | KHCO3 | K2SO4 | CH3COOK |
| 20℃溶解度 | 6.4 | 111 | 33.7 | 11.1 | 217 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH=2的HA溶液与pH=12的MOH溶液等体积混合后pH<7,则HA为弱酸 | |
| B. | pH相等的CH3COONa、NaOH和Na2CO3三种溶液:c(NaOH)<c(Na2CO3)<c(CH3COONa) | |
| C. | 物质的量浓度均为0.2mol•L-1CH3COOH和CH3COONa溶液等体积混合:2c(Na+)=c(CH3COO-)+c(CH3COOH)=0.2mol•L-1 | |
| D. | 0.1mol•L-1的NaHA溶液,其pH=4:c(HA-)>c(H+)>c(H2A)>c(A2-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
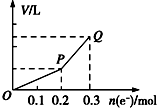 用惰性电极电解硫酸铜溶液,整个过程转移电子的物质的量与产生气体总体积的关系如图所示(气体体积均在相同状况下测定).欲使溶液恢复到起始状态,可向溶液中加入( )
用惰性电极电解硫酸铜溶液,整个过程转移电子的物质的量与产生气体总体积的关系如图所示(气体体积均在相同状况下测定).欲使溶液恢复到起始状态,可向溶液中加入( )| A. | 0.15 mol CuO | B. | 0.1 mol CuCO3 | ||
| C. | 0.075mol Cu(OH)2 | D. | 0.05 mol Cu2(OH)2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:2 | B. | 2:3 | C. | 3:2 | D. | 1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁丝在氧气中燃烧:火星四射,生成红色固体 | |
| B. | 硫粉在空气中燃烧:产生淡蓝色火焰,生成一种刺激性气味的气体 | |
| C. | 镁条在空气中燃烧:发出耀眼的白光,只生成一种黑色固体 | |
| D. | 红磷在空气中燃烧:发出白光,生成大量的白色烟雾 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com