
【题目】乙酸苯甲酯( ![]() )广泛存在于可可、咖啡、草莓等物质中,可用作食物和日化用品的香精. 已知:X的产量可以用来衡量一个国家的石油化工发展水平,工业上可用X和甲苯人工合成乙酸苯甲酯.其合成路线如下:
)广泛存在于可可、咖啡、草莓等物质中,可用作食物和日化用品的香精. 已知:X的产量可以用来衡量一个国家的石油化工发展水平,工业上可用X和甲苯人工合成乙酸苯甲酯.其合成路线如下: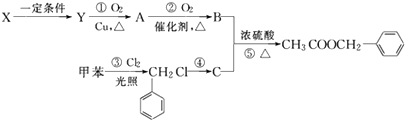
据此回答下列问题:
(1)X生成Y的化学方程式为 , 生成物Y中含有官能团的名称为 .
(2)![]() 发生反应④所需的条件是 , 该反应的反应类型为 .
发生反应④所需的条件是 , 该反应的反应类型为 .
(3)实验室为鉴别A和B两者的水溶液,可以选用的化学试剂是 . A.纯碱溶液 B.NaOH溶液 C.金属钠 D.银氨溶液
(4)上述反应①~⑤中原子的理论利用率为100%、符合绿色化学要求的反应是(填序号).
(5)请写出反应⑤的化学方程式 .
(6)写出符合下列条件的乙酸苯甲酯的一种同分异构体:①含苯环结构;②具有酯的结构. .
【答案】
(1)CH2=CH2+H2O ![]() CH3CH2OH;羟基
CH3CH2OH;羟基
(2)氢氧化钠水溶液、加热;水解反应
(3)A、D
(4)②
(5)CH3COOH+ ![]()
![]()
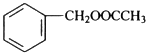 +H2O
+H2O
(6)![]()
【解析】解:X的产量可以用来衡量一个国家的石油化工发展水平,则X为CH2=CH2 , X转化得到Y,Y连续氧化得到B,而B与C反应得到乙酸苯甲酯,故B为CH3COOH,C为苯甲醇,结构简式为 ![]() ,则Y为CH3CH2OH,A为CH3CHO,(1)X生成Y是乙烯与水发生加成反应生成乙醇,反应化学方程式为:CH2=CH2+H2O
,则Y为CH3CH2OH,A为CH3CHO,(1)X生成Y是乙烯与水发生加成反应生成乙醇,反应化学方程式为:CH2=CH2+H2O ![]() CH3CH2OH,乙醇中含有的官能团为羟基,所以答案是:CH2=CH2+H2O
CH3CH2OH,乙醇中含有的官能团为羟基,所以答案是:CH2=CH2+H2O ![]() CH3CH2OH;羟基;(2)
CH3CH2OH;羟基;(2) ![]() 发生反应④是卤代烃的水解反应,所需的条件是:氢氧化钠水溶液、加热,所以答案是:氢氧化钠水溶液、加热;水解反应;(3)A.乙酸与碳酸钠反应生成二氧化碳,而乙醛与碳酸钠不反应,且互溶,能用纯碱溶液鉴别乙酸与乙醛,故A正确;B.乙酸与氢氧化钠反应,物明显现象,乙醛与NaOH溶液互溶,无法区别,故B错误; C.金属钠与乙酸反应生成氢气,虽然乙醛不与Na反应,但溶液中的水与钠反应生成氢气,无法区别,故C错误;D.乙醛与银氨溶液有银镜现象产生,而乙酸不与银氨溶液反应,可以区别,故D正确,故选:AD;(4)上述反应①~⑤中,乙醛催化氧化生成乙酸,符合原子的理论利用率为100%、符合绿色化学要求的反应是,所以答案是:②; (5)出反应⑤的化学方程式为:CH3COOH+
发生反应④是卤代烃的水解反应,所需的条件是:氢氧化钠水溶液、加热,所以答案是:氢氧化钠水溶液、加热;水解反应;(3)A.乙酸与碳酸钠反应生成二氧化碳,而乙醛与碳酸钠不反应,且互溶,能用纯碱溶液鉴别乙酸与乙醛,故A正确;B.乙酸与氢氧化钠反应,物明显现象,乙醛与NaOH溶液互溶,无法区别,故B错误; C.金属钠与乙酸反应生成氢气,虽然乙醛不与Na反应,但溶液中的水与钠反应生成氢气,无法区别,故C错误;D.乙醛与银氨溶液有银镜现象产生,而乙酸不与银氨溶液反应,可以区别,故D正确,故选:AD;(4)上述反应①~⑤中,乙醛催化氧化生成乙酸,符合原子的理论利用率为100%、符合绿色化学要求的反应是,所以答案是:②; (5)出反应⑤的化学方程式为:CH3COOH+ ![]()
![]()
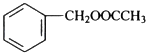 +H2O,所以答案是:CH3COOH+
+H2O,所以答案是:CH3COOH+ ![]()
![]()
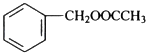 +H2O;(6)符合下列条件的乙酸苯甲酯的一种同分异构体:①含苯环结构;②具有酯的结构,符合条件的一种同分异构体为
+H2O;(6)符合下列条件的乙酸苯甲酯的一种同分异构体:①含苯环结构;②具有酯的结构,符合条件的一种同分异构体为 ![]() 等,所以答案是:
等,所以答案是: ![]() 等.
等.


科目:高中化学 来源: 题型:
【题目】分析实验中出现下列现象对所配溶液的浓度有何影响:
(1)①浓硫酸溶解后未冷却至室温即转移至容量瓶中进行定容,(填“偏高”、“偏低”或“无影响”);
②定容时仰视刻度线,;填“偏高”、“偏低”或“无影响”);
③量取好浓硫酸倒入烧杯溶解后,用水洗涤量筒2~3次,将洗涤液倒入烧杯中, . (填“偏高”、“偏低”或“无影响”);
(2)7.8g镁铝合金与足量的稀盐酸反应,生成氢气的体积为8.96L(标准状况),则此反应中转移电子的数目为 , 镁和铝分别产生氢气的体积之比为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是( )
A.油脂在人体内通过酶的参与可水解为高级脂肪酸和甘油
B.油脂主要在小肠中消化吸收
C.磷脂对人体吸收维生素A E是有利的
D.同质量的脂肪在体内氧化时放出的能量比糖类和蛋白质高得多,故脂肪是人体提供能量的主要物质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年来发现用铈(Ce)的氧化物可高效制取H2 , 制备原理如图所示,已知0<δ<2,下列说法不正确的是( ) 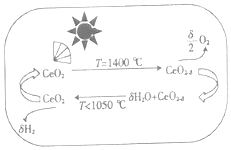
A.太阳能最终转变为化学能
B.CeO2是水分解的催化剂
C.T<1050℃时,CeO2﹣δ比CeO2稳定
D.两步反应均属于氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用图所示装置来制取乙酸乙酯,回答下列问题: 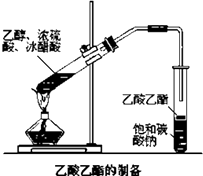
(1)请写出本实验中发生的主要反应方程式 .
(2)配置混合溶液时,加入试剂的正确顺序是(填“A”或“B”).
A.先加乙醇,再慢慢注入浓硫酸和乙酸
B.先加浓硫酸,再慢慢注入乙醇和乙酸
(3)浓硫酸的作用是 .
(4)饱和Na2CO3溶液的作用是 .
(5)实验完成后,右边试管液面上有透明的不溶于水的油状液体生成.若要分离10mL该液体混合物需要用到的主要玻璃仪器是 , 这种分离方法叫做 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素W,X,Y,Z的原子序数依次增加.m、n、p是由这些元素组成的二元化合物,W2、X2、Z2分别是元素W,X,Z的单质.已知:
I.一定条件下某密闭容器中可发生反应:aX2+bW2cm,反应过程中物质的浓度变化如下:
X2 | W2 | m | |
起始浓度/molL﹣1 | 0.4 | 0.4 | 0 |
平衡浓度/molL﹣1 | 0.3 | 0.1 | 0.2 |
II.它们可发生如下反应:2m(g)+3Z(g)=6n(g)+X2(g);4n(g)+Y2(g) ![]() 2p(l)+2Z2(g).下列说法正确的是( )
2p(l)+2Z2(g).下列说法正确的是( )
A.原子半径:W<X<Y
B.a:b:c=3:1:2
C.X的氧化物一定是无色气体
D.m、n、p三种物质均为共价化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列变化中,不属于化学变化的是( )
A. 氯水使有色布条褪色 B. 漂白粉使某些染料褪色
C. SO2使品红溶液褪色 D. 活性炭使红墨水褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在炼油工业中常用醋酸铜氨溶液含{[Cu(NH3)2]+、CH3COO﹣和NH3}除去H2中的CO、O2及H2S气体.
(1)已知醋酸铜氨溶液吸收CO的反应为:[Cu(NH3)2]+(aq)+CO(g)+NH3(g)[Cu(NH3)2CO]+(aq).
若反应在恒容密闭容器中进行,则能说明该反应已达到平衡状态的是 .
a.v(CO)正=v(NH3)正
b.容器内气体压强不再随时间变化
c.[Cu(NH3)2]+浓度不再随时间变化
(2)醋酸铜氨溶液吸收CO一段时间后将失效,用下列方法可回收废醋酸铜氨溶液中的铜. 
①“预处理”时,尾气中除N2、CO、O2、CO2及H2O外,还有 .
②加入硫化钠溶液时发生反应的离子方程式为 .
③加入硝酸时发生反应的化学方程式为 .
④已知上述流程中只有“沉铜”和“结晶”步骤铜元素有损耗.“沉铜”时铜元素的损耗率为4%;“结晶”时铜元素的损耗率为2%.若1L废液最终制得Cu(NO3)23H2O 363g,则1L废液中铜元素的质量为g.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com