
| A. | 回收废弃的饮料包装纸,制作成公园内的休闲长椅 | |
| B. | 大力开发丰富的煤炭资源,减少对石油的依赖 | |
| C. | 在西部和沿海地区兴建风力发电站,解决能源问题 | |
| D. | 鼓励购买小排量汽车,推广电动、混合动力汽车 |
分析 A.回收废弃的饮料包装纸,可以节约资源;
B.大力开发丰富的煤炭资源,会加重环境污染;
C.兴建风力发电站,可以减少化石燃料的使用,解决能源问题;
D.汽车会消耗大量汽油,产生废气污染环境.
解答 解:A.回收废弃的饮料包装纸,做到垃圾资源化,有利于保护环境,可以节约资源,故A正确;
B.煤炭在燃烧时会产生大量污染性气体,大力开发丰富的煤炭资源,会加重环境污染,故B错误;
C.在西部和沿海地区风能资源丰富,兴建风力发电站可以减少化石燃料的使用,能够降低二氧化碳的排放,解决能源问题,故C正确;
D.汽车会消耗大量汽油,产生废气污染环境,鼓励购买小排量汽车,推广电动、混合动力汽车可以减少化石燃料的使用,减少污染性气体的排放,故D正确.
故选B.
点评 本田考查了环境保护和能源的开发利用,题目难度不大,注意把握题目中的要求,侧重于考查学生对化学知识的应用能力.


科目:高中化学 来源: 题型:选择题
| A. | 氢氧化铁与盐酸反应:H++OH-═H2O | |
| B. | 铁与盐酸反应:2Fe+6H+═2Fe3++3H2↑ | |
| C. | 用小苏打治疗胃酸(盐酸)过多:HCO3-+H+═CO2↑+H2O | |
| D. | CaCO3溶于稀硝酸中:CO32-+2H+═CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2中有少量HCl气体(氢氧化钠溶液) | B. | CO中混有CO2(石灰水、浓硫酸) | ||
| C. | CO2中有少量CO(灼热氧化铜) | D. | Cl2中混有HCl(饱和食盐水、浓硫酸) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.05mol•L-1 | B. | 0.30 mol•L-1 | C. | 0.15 mol•L-1 | D. | 0.5 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
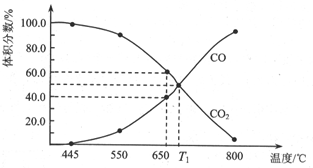 一定量的CO2与足量的C在恒容密闭容器中发生反应:C(s)+CO2(g)?2CO(g)△H.
一定量的CO2与足量的C在恒容密闭容器中发生反应:C(s)+CO2(g)?2CO(g)△H.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H+(aq)+OH-(aq)=H2O(l)△H=-a kJ/mol,故1 mol NaOH固体与足量的稀盐酸反应,放出热量为a kJ | |
| B. | 因CuSO4•5H2O(s)=CuSO4(s)+5H2O(1)△H=+b kJ/mol,故1 mol CuSO4( s)溶于足量水时,放出热量为b kJ | |
| C. | 因氢气的燃烧热为c kJ/mol,故电解水的热化学方程式为:2H2O(1)=2H2( g)+O2( g)△H=+c kJ/mol | |
| D. | 因N2( g)+3H2( g)?2NH3( g)△H=-d kJ/mol,故在某容器中投入1 mol N2与3 mol H2 充分反应后,放出热量小于d kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 达到化学平衡时,将完全转化为NH3 | |
| B. | 达到化学平衡时,N2、H2和NH3的物质的量浓度一定相等 | |
| C. | 达到化学平衡时,N2、H2和NH3的物质的量浓度不再变化 | |
| D. | 达到化学平衡时,正反应速率和逆反应速率都为零 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com