
| A. | 上述正反应为吸热反应 | |
| B. | 在5MPa、800K时,该反应的平衡常数为$\frac{{V}^{2}}{{a}^{2}}$L2•mol-2 | |
| C. | 在4MPa、1200K时,图中X点υ(H2)正>υ(H2)逆 | |
| D. | 工业上维持6MPa 1000K而不采用10MPa1000K,主要是因为前者碳的转化率高 |
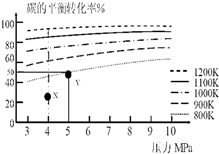
分析 A、温度越高碳的平衡转化率越大,所以平衡正向移动,由此分析热效应;
B、根据碳转化率为50%,结合三行式求平衡时各组分的浓度,然后代入平衡常数表达式计算求解;
C、根据X点反应的移动方向来确定正反应速率和逆反应速率的关系;
D、根据压强对反应速率以及平衡的移动的影响并结合生产实际来回答判断.
解答 解:A、由图观察,温度越高碳的平衡转化率越大,平衡正向移动,正反应为吸热反应,故A正确;
B、在5MPa、800K时,此时碳转化率为50%,
C(s)+2H2(g)?CH4(g)
始量量:a 2 a
转化量:0.25a 0.5a 0.25a
平衡量:0.75a 1.5a 0.25a
K=$\frac{\frac{0.25a}{V}}{(\frac{1.5a}{V})^{2}}$=$\frac{V}{10a}$,故B错误;
C、由图观察,X点是未平衡时,反应正向进行,正反应速率大于逆反应速率,故C正确;
D、该选择的原因是两者转化率相差不大,但压强增大对设备要求高,能量需求大,故D错误.
故选AC.
点评 本题考查化学平衡有关问题,注意化学平衡状态的判断以及平衡常数的有关计算是解题的关键,难度中等.


科目:高中化学 来源: 题型:实验题
| 相对原子质量 | 密度/(g•cm-3) | 沸点/℃ | 水中溶解性 | |
| 异戊醇 | 88 | 0.8123 | 131 | 微溶 |
| 乙酸 | 60 | 1.0492 | 118 | 溶 |
| 乙酸异戊醇 | 130 | 0.8670 | 142 | 难溶 |
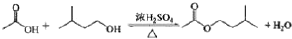
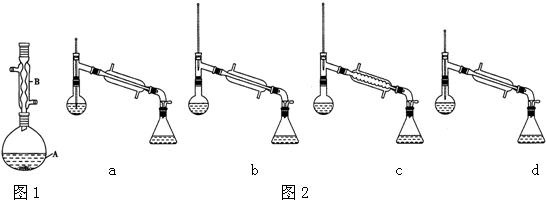
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
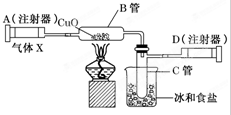 如图所示的实验装置可用来测定含两种元素的气体X的分子式.
如图所示的实验装置可用来测定含两种元素的气体X的分子式.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
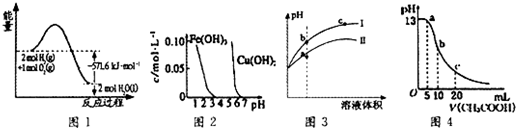
| A. | 图1表示H2与O2发生反应过程中的能量变化,H2的燃烧热为285.8 kJ/mol | |
| B. | 由图2得出若除去CuSO4溶液中的Fe3+,可采用向溶液中加入适量CuO,调节溶液的pH至4左右 | |
| C. | 图3表示用水稀释pH相同的盐酸和醋酸时溶液的pH变化曲线,其中Ⅰ表示醋酸,Ⅱ表示盐酸,且溶液导电性:c>b>a | |
| D. | 图4表示常温下向体积为10 mL0.1 mol/LNaOH溶液中逐滴加入0.1 mol/LCH3COOH溶液后溶液的pH变化曲线,则b点处有:c(CH3COOH)+c(H+)=c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 中子数为18的硫原子:1816S | B. | HClO的结构式为:H-O-Cl | ||
| C. | H2O2的电子式: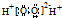 | D. | 聚乙烯的结构简式: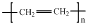 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
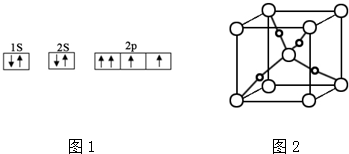
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2O2既是氧化剂,又是还原剂 | |
| B. | O2是还原产物,Mn2+是氧化产物 | |
| C. | 通常用浓盐酸酸化高锰酸钾溶液 | |
| D. | 标准状况下,产生22.4 L O2时反应转移2 mol e- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
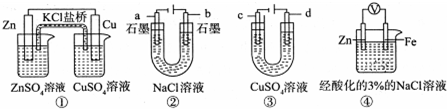
| A. | 装置①中,盐桥中的 K+移向CuSO4溶液 | |
| B. | 装置②在电解过程中,a极上得到22.4 L气体(标准状况),理论上需要转移NA个电子(NA表示阿伏加德罗常数) | |
| C. | 可以用装置③在铜上镀银,c极为银 | |
| D. | 装置④中一段时间后会有Fe(OH)2生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3CH═CH2与HBr | B. | 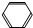 -CH3与混酸(浓HNO3和浓H2SO4,30℃) -CH3与混酸(浓HNO3和浓H2SO4,30℃) | ||
| C. | CH3CH═CHCH3与HBr | D. | 光照条件下CH3CH3与Cl2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com