
 ŅŃÖŖĖ®ŌŚ25”ęŗĶ95”ꏱ£¬ĘäµēĄėĘ½ŗāĒśĻßČēĶ¼ĖłŹ¾£ŗ
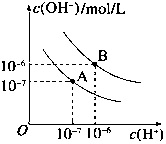
ŅŃÖŖĖ®ŌŚ25”ęŗĶ95”ꏱ£¬ĘäµēĄėĘ½ŗāĒśĻßČēĶ¼ĖłŹ¾£ŗ·ÖĪö £Ø1£©ŗįÖįŹĒĒāĄė×ÓÅØ¶Č£¬×ŻÖįŹĒĒāŃõøłĄė×ÓÅØ¶Č£¬Ė®µÄĄė×Ó»ż³£ŹżKw=c£ØH+£©”Įc£ØOH-£©¼ĘĖć³öAĒśĻßµÄKwÖµ£»
£Ø2£©øł¾ŻĖ®µÄĄė×Ó»ż³£ŹżKw=c£ØH+£©”Įc£ØOH-£©¼ĘĖć£»
£Ø3£©95”ꏱĖ®µÄµēĄė²śÉśµÄĒāĄė×ÓŗĶĒāŃõøłĄė×ÓµÄÅضČĻąµČ£¬ĖłŅŌĮ½ÕßÅØ¶Č¶¼ĪŖ10-6mol/L£»
£Ø4£©øł¾ŻČÜŅŗµÄpH¼ĘĖć³öČÜŅŗÖŠĒāĄė×Ó”¢ĒāŃõøłĄė×ÓÅØ¶Č£¬ŌŁĮŠŹ½¼ĘĖć³öĒāŃõ»ÆÄĘČÜŅŗŗĶĮņĖįČÜŅŗµÄĢå»ż£»
£Ø5£©Ėį”¢¼ī¶¼ŹĒĒæµē½āÖŹ£¬ČÜŅŗ³ŹÖŠŠŌĖµĆ÷ĒāĄė×ÓŗĶĒāŃõøłĄė×ÓµÄĪļÖŹµÄĮæĻąµČ£¬½įŗĻĖ®µÄĄė×Ó»ż³£ŹżČ·¶ØĒæĖįµÄpH1ÓėĒæ¼īµÄpH2Ö®¼äÓ¦Āś×ćµÄ¹ŲĻµ£»
£Ø6£©øł¾ŻĒśĻßB¶ŌÓ¦ĪĀ¶ČĻĀpH=5£¬ĖµĆ÷ČÜŅŗĻŌŹ¾ĖįŠŌ£¬·“Ó¦ŗóĒāĄė×Ó¹żĮæ·ÖĪö£®
½ā“š ½ā£ŗ£Ø1£©ĒśĻßAĢõ¼žĻĀKw=c£ØH+£©”Įc£ØOH-£©=10-7”Į10-7=10-14£¬ĒśĻßBĢõ¼žĻĀc£ØH+£©=c£ØOH-£©=10-6 mol/L£¬Kw=c£ØH+£©•c£ØOH-£©=10-12 £¬¹Ź“š°øĪŖ£ŗ1.0”Į10-12£»
£Ø2£©95”ꏱ£¬0.01mol/LNaOHČÜŅŗÖŠĒāŃõøłĄė×ÓµÄÅضČĪŖ0.01mol/L£¬ĖłŅŌČÜŅŗÖŠĒāĄė×ÓµÄÅضČĪŖ£ŗ10-10mol/L£¬ĖłŅŌČÜŅŗµÄPH=10£¬¹Ź“š°øĪŖ£ŗ10£»
£Ø3£©95”ꏱĖ®µÄµēĄė²śÉśµÄĒāĄė×ÓŗĶĒāŃõøłĄė×ÓµÄÅضČĻąµČ£¬ĖłŅŌĮ½ÕßÅØ¶Č¶¼ĪŖ10-6mol/L£¬Ė®µÄµēĄėŹĒĪüČČ¹ż³Ģ£¬ĪĀ¶ČÉżøßµēĄė³Ģ¶ČŌö“ó£¬C£ØH+£©”¢C£ØOH-£©¾łŌö“󣬹ŹŃ”£ŗB£»Ė®µÄµēĄėŹĒĪüČČ¹ż³Ģ£¬ĪĀ¶ČÉżøßµēĄė³Ģ¶ČŌö“ó£¬C£ØH+£©”¢C£ØOH-£©¾łŌö“ó£»
£Ø4£©25”ꏱĖłµĆ»ģŗĻČÜŅŗµÄpH=7£¬ČÜŅŗ³ŹÖŠŠŌ¼“Ėį¼īĒ”ŗĆÖŠŗĶ£¬¼“n£ØOH-£©=n£ØH+£©£¬ŌņV£ØNaOH£©•10-5 mol•L-1=V£ØH2SO4£©•10-4 mol•L-1£¬µĆV£ØNaOH£©£ŗV£ØH2SO4£©=10£ŗ1£¬¹Ź“š°øĪŖ£ŗ10£ŗ1£»
£Ø5£©ŅŖ×¢ŅāµÄŹĒ95”ćCŹ±£¬Ė®µÄĄė×Ó»żĪŖ10-12£¬¼“Ėį”¢¼īÅضČĻąµČŹ±pH£ØĖį£©+pH£Ø¼ī£©=12£¬ĻÖĒæ¼īµÄOH-ÅØ¶ČŹĒĒæĖįH+ÅØ¶ČµÄ100±¶£¬ĖłŅŌpH£ØĖį£©+pH£Ø¼ī£©=14£¬¼“pH1+pH2=14£¬»ņa+b=14£¬
¹Ź“š°øĪŖ£ŗpH1+pH2=14£Ø»ņa+b=14£©£»
£Ø6£©ŌŚĒśĻßB¶ŌÓ¦ĪĀ¶ČĻĀ£¬ŅņpH£ØĖį£©+pH£Ø¼ī£©=12£¬æɵĆĖį¼īĮ½ČÜŅŗÖŠc£ØH+£©=c£ØOH-£©£¬ČēŹĒĒæĖį¼ī£¬Į½ČÜŅŗµČĢå»ż»ģŗĻŗóČÜŅŗ³ŹÖŠŠŌ£»ĻÖ»ģŗĻČÜŅŗµÄpH=5£¬¼“µČĢå»ż»ģŗĻŗóČÜŅŗĻŌĖįŠŌ£¬ĖµĆ÷H+ÓėOH-ĶźČ«·“Ó¦ŗóÓÖÓŠŠĀµÄH+²śÉś£¬Ėį¹żĮ棬ĖłŅŌĖįHAŹĒČõĖį£¬
¹Ź“š°øĪŖ£ŗĒśĻßB¶ŌÓ¦95”ę£¬“ĖŹ±Ė®µÄĄė×Ó»żĪŖ10-12£¬HAĪŖČõĖį£¬HAÖŠŗĶNaOHŗ󣬻ģŗĻČÜŅŗÖŠ»¹Ź£Óą½Ļ¶ąµÄHA·Ö×Ó£¬æɼĢŠųµēĄė³öH+£¬Ź¹ČÜŅŗpH=5£®
µćĘĄ ±¾Ģāæ¼²éĮĖĖ®µÄµēĄėĘ½ŗā”¢Ė®µÄĄė×Ó»ż³£ŹżµÄÓ°ĻģŅņĖŲŅŌ¼°¼ĘĖćµČÖŖŹ¶£¬×¢ŅāÖŖŹ¶µÄ¹éÄÉŗĶŹįĄķŹĒ¹Ų¼ü£¬ÄѶČÖŠµČ£®


 ĢōÕ½100µ„ŌŖ¼ģ²āŹŌ¾ķĻµĮŠ“š°ø
ĢōÕ½100µ„ŌŖ¼ģ²āŹŌ¾ķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
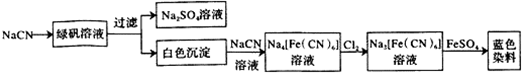
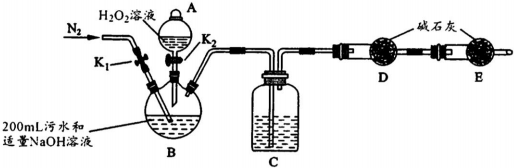
| ²½Öč1 | ¹Ų±ÕK1£¬“ņæŖK2£¬µĪČė×ćĮæH2O2ČÜŅŗ£¬¶ŌB¼ÓČČ£®³ä·Ö·“Ó¦ŗó£¬Ķ£Ö¹¼ÓČČ£® |
| ²½Öč2 | ĄäČ“ŗó£¬ÓĆ×¢ÉäĘ÷“©¹żB×°ÖĆµÄ½ŗČū×¢ČėĻ”H2S04ČÜŅŗ£® |
| ²½Öč3 | “ņæŖK1£¬ĶØČėN2£® |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
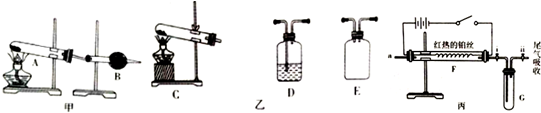
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ”÷H2£¾”÷H1£¬”÷H4£¾”÷H3 | B£® | ”÷H1£¾”÷H2£¬”÷H4£¾”÷H3 | C£® | ”÷H1£¾”÷H2£¬”÷H3£¾”÷H4 | D£® | ”÷H2£¾”÷H1£¬”÷H3£¾”÷H4 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | 0.5 LøĆČÜŅŗÖŠÄĘĄė×ÓµÄĪļÖŹµÄĮæÅضČĪŖ0.1 mol/L | |
| B£® | 1 LøĆČÜŅŗÖŠŗ¬ÓŠNa2CO3µÄÖŹĮæĪŖ10.6 g | |
| C£® | “Ó1 LøĆČÜŅŗÖŠČ”³ö100 mL£¬ŌņČ”³öČÜŅŗÖŠNa2CO3µÄĪļÖŹµÄĮæÅضČĪŖ0.01 mol/L | |
| D£® | Č”øĆČÜŅŗ10 mL£¬¼ÓĖ®Ļ”ŹĶÖĮ100 mLŗó£¬Na2CO3µÄĪļÖŹµÄĮæÅضČĪŖ0.01 mol/L |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
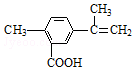
| A£® | ŌŚŅ»¶ØĢõ¼žĻĀ£¬ÄÜ·¢ÉśČ”“ś”¢Ńõ»Æ”¢Ė®½ā”¢õ„»ÆŗĶ¼Ó¾Ū·“Ó¦ | |
| B£® | øĆĪļÖŹ·Ö×ÓÖŠ×ī¶ąæÉŅŌÓŠ9øöĢ¼Ō×ÓŌŚĶ¬Ņ»Ę½ĆęÉĻ | |
| C£® | 1 moløĆĪļÖŹ×ī¶ąæÉÓė5mol H2·¢Éś¼Ó³É·“Ó¦ | |
| D£® | 1 moløĆĪļÖŹĶźČ«Ńõ»Æ×ī¶ąæÉĻūŗÄ13 molŃõĘų |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | µē³Ų¹¤×÷Ź±£¬ČÜŅŗÖŠµÄĀĮĄė×ÓĻņÕż¼«ŅĘ¶Æ | |
| B£® | øƵē³ŲæÉÄÜŹĒŅ»ÖÖæɳäµēµÄ¶ž“Īµē³Ų | |
| C£® | ĻūŗÄĻąĶ¬ÖŹĮ潚ŹōŹ±£¬ÓĆļ®×öøŗ¼«Ź±£¬²śÉśµē×ÓµÄĪļÖŹµÄĮæ±ČĀĮ¶ą | |
| D£® | øƵē³Ųøŗ¼«µÄµē¼«·“Ó¦ĪŖ£ŗAl-3e-ØTAl3+ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com